- Lithium
-
 Pour les articles homonymes, voir Lithium (homonymie).
Pour les articles homonymes, voir Lithium (homonymie).Lithium Hélium ← Lithium → Béryllium H 
3Li ↑ Li ↓ Na Table complète • Table étendue Informations générales Nom, symbole, numéro Lithium, Li, 3 Série chimique Métal alcalin Groupe, période, bloc 1, 2, s Masse volumique 0,534 g·cm-3 (20 °C)[1] Dureté 0,6 Couleur Blanc argenté / gris No CAS No EINECS Propriétés atomiques Masse atomique 6,941 ± 0,002 u [1] Rayon atomique (calc) 145 pm (167 pm) Rayon de covalence 1,28 ± 0,07 Å [2] Rayon de van der Waals 182 pm Configuration électronique [He] 2s1 Électrons par niveau d’énergie 2, 1 État(s) d’oxydation +1 Oxyde base forte Structure cristalline Cubique centré Propriétés physiques État ordinaire Solide diamagnétique Point de fusion 180,5 °C [1] Point d’ébullition 1 342 °C [1] Énergie de fusion 3 kJ·mol-1 Énergie de vaporisation 145,92 kJ·mol-1 Température critique 3 223 °C [3] Pression critique 68,9 MPa [3] Volume critique 66 cm3·mol-1 [3] Volume molaire 13,02×10-6 m3·mol-1 Pression de vapeur 1,63×10-8 Pa
à 180,54 °CVitesse du son 6 000 m·s-1 à 20 °C Divers Électronégativité (Pauling) 0,98 Chaleur massique 3 582 J·kg-1·K-1 Conductivité électrique 10,8×106 S·m-1 Conductivité thermique 84,7 W·m-1·K-1 Énergies d’ionisation[4] 1re : 5,391719 eV 2e : 75,6400 eV 3e : 122,45429 eV Isotopes les plus stables iso AN Période MD Ed PD MeV 6Li 7,5 % stable avec 3 neutrons 7Li 92,5 % stable avec 4 neutrons 8Li {syn.} 0,838 s β- 16 8Be Précautions Directive 67/548/EEC[5],[6] 
C
FPhrases R : 14/15, 34, Phrases S : (1/2), 8, 43, 45, Transport[5] X423 1415 SIMDUT[7] 
SGH[8],[6] 

DangerUnités du SI & CNTP, sauf indication contraire. Le lithium est un élément chimique, de symbole Li et de numéro atomique 3. Dans le tableau périodique des éléments, il est situé dans le groupe 1, parmi les métaux alcalins. Comme tous les métaux alcalins, il est très réactif et est généralement conservé dans de l'huile minérale pour le préserver de l'air. Le lithium pur est un métal mou, de couleur blanc argenté, qui se ternit et s'oxyde très rapidement au contact de l'air et de l'eau, prenant une teinte grise virant rapidement à l'anthracite et au noir. C'est l'élément solide le plus léger. Il est essentiellement utilisé pour réaliser des verres et des céramiques réfractaires, des alliages à la fois légers et résistants pour l'aéronautique, et surtout des piles au lithium et des batteries au lithium.
En raison de sa très grande réactivité chimique, le lithium n'existe pas à l'état natif dans le milieu naturel, et ne s'y trouve que dans des composés le plus souvent ioniques. On l'extrait de minéraux de type pegmatite, ainsi que d'argiles et de saumures. Il est produit industriellement par électrolyse d'un mélange de chlorure de lithium et de chlorure de potassium. Les réserves mondiales de lithium étaient estimées à 13 millions de tonnes fin 2010[9], dont 58 % au Chili et 27 % en Chine. La production mondiale, quant à elle, s'est élevée à 25 300 tonnes en 2010, hors États-Unis (dont les données ne sont pas rendues publiques par l'USGS), assurée essentiellement par le Chili (35 %), l'Australie (34 %), la Chine (18 %) et l'Argentine (11,5 %).
Le noyau des deux isotopes stables du lithium comptent parmi les noyaux atomiques ayant l'énergie de liaison par nucléon la plus faible de tous les isotopes stables, ce qui signifie que ces noyaux sont en fait assez peu stables comparés à ceux des autres éléments légers. C'est pourquoi ils peuvent être utilisés dans des réactions de fission nucléaire comme de fusion nucléaire. C'est également la raison pour laquelle le lithium est moins abondant dans le Système solaire que 25 des 32 éléments chimiques les plus légers[10]. Le lithium joue par conséquent un rôle important en physique nucléaire. La transmutation d'atomes de lithium en tritium a été la première réaction de fusion nucléaire artificielle, et le deutérure de lithium est le combustible de la bombe H.
Le lithium est présent à l'état de traces dans les océans et chez tous les êtres vivants. Il ne semble pas avoir de rôle biologique notable car les animaux et les végétaux peuvent vivre en bonne santé dans un milieu dépourvu de lithium. Les éventuelles fonctions non vitales du lithium n'ont pas non plus été élucidées, cependant l'administration d'ions Li+ sous forme de sels de lithium s'est révélée efficace comme thymorégulateur, notamment en cas de trouble bipolaire.
Sommaire
Histoire
Le lithium (du grec lithos signifiant « pierre ») a été découvert par Johan August Arfwedson en 1817.
Arfwedson découvrit un nouveau sel en analysant des minéraux de pétalite, de spodumène et de lépidolite en provenance de l'île de Utö, commune de Haninge en Suède.
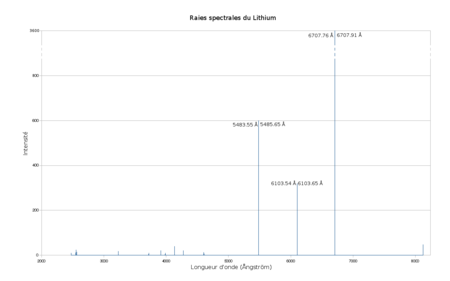
En 1818, Christian Gmelin (1792 - 1860) fut le premier à observer que ces sels (de lithium) donnaient une flamme rouge et brillante.
Toutefois, les deux hommes cherchèrent à isoler l'élément de son sel mais n'y parvinrent pas. L'élément fut isolé par électrolyse d'un oxyde de lithium par William Thomas Brande et Sir Humphry Davy. On lui donna le nom de lithium pour rappeler qu'il fut découvert dans le règne minéral.
La production commerciale de lithium commença en 1923 par la firme allemande Metallgesellschaft AG qui utilisa l'électrolyse d'un mélange de chlorure de lithium et de chlorure de potassium fondu.
Propriétés
Le lithium est le métal ayant la plus faible masse molaire et la plus faible densité, avec une masse volumique inférieure de moitié à celle de l'eau. Conformément à loi de Dulong et Petit, c'est le solide ayant la plus grande chaleur massique.
Comme les autres métaux alcalins, le lithium réagit facilement au contact de l'eau ou de l'air (cependant moins que le sodium) ; il n'existe pas à l'état natif.
Lorsqu'il est placé au-dessus d'une flamme, celle-ci prend une couleur cramoisie mais lorsqu'il commence à brûler, la flamme devient d'un blanc très brillant. En solution, il forme des ions Li+.
Utilisation
Le lithium est souvent utilisé comme anode de batterie du fait de son grand potentiel électrochimique. Les batteries lithium sont très utilisées dans le domaine des systèmes embarqués du fait de leur grande densité énergétique aussi bien massique que volumique.
Autres usages :
- les sels de lithium, comme le carbonate de lithium, le citrate de lithium ou l'orotate de lithium sont utilisés comme régulateur de l'humeur pour le traitement des troubles bipolaires (anciennement psychose maniaco-dépressive)[11] ;
- aussi utilisé avec certains antidépresseurs tel la fluoxétine* pour traiter les troubles obsessifs compulsifs ;
- le gluconate de lithium est utilisé en dermatologie comme anti-allergénique ;
- le lithium est utilisé dans les troubles du sommeil et l'irritabilité en oligothérapie (en l'absence d'activité spécifiquement démontrée);
- le lithium pourrait ralentir la progression de la sclérose latérale amyotrophique (SLA), selon les résultats d'une étude pilote publiés dans Proceedings of the National Academy of Sciences (Pnas).
- le chlorure de lithium et le bromure de lithium sont extrêmement hygroscopiques et sont utilisés comme dessiccatifs ;
- le lithium est un agent réducteur et/ou complexant utilisé pour la synthèse de composés organiques ;
- le lithium est parfois utilisé dans les verres et les céramiques à faible expansion thermique, comme par exemple pour le miroir de 200 pouces du télescope Hale du Mont Palomar [12] ; par ailleurs, il a une faible interaction avec les rayons X, les verres au lithium (méta- et tétraborate de lithium) sont donc utilisés pour dissoudre des oxydes (méthode de la perle fondue) en spectrométrie de fluorescence X ;
- l'hydroxyde de lithium est employé pour extraire le CO2 de l'air dans les milieux confinés comme les capsules spatiales et les sous-marins ;
- les organolithiens sont utilisés dans la synthèse et la polymérisation des élastomères ;
- les alliages haute performance lithium-aluminium, cadmium, cuivre et manganèse servent à la fabrication de pièces pour aéronefs ;
- les sels de lithium sont utilisés pour le transfert de chaleur par convection ;
- pour la production de tritium par réaction nucléaire ; le tritium est utilisé pour la fusion nucléaire ;
- le lithium est, avec le potassium, un de deux alcalins possédant un isotope fermionique stable, d'où son intérêt pour l'étude des gaz ultrafroids fermioniques dégénérés.
Le lithium 6 est une matière nucléaire dont la détention est réglementée (Article R1333-1 du code de la défense).
Article détaillé : Contrôle des matières nucléaires.Biologie
Le lithium est trouvé à l'état de traces dans le plancton, dans de nombreuses plantes et invertébrés à des concentrations variant de 69 ppb à 5760 ppb. Dans les tissus et fluides vitaux des vertébrés, la concentration varie de 21 à 763 ppb[13]. Les organismes marins accumulent davantage de lithium dans leurs tissus que leurs homologues terrestres[14]. Le rôle du lithium dans le vivant est encore assez obscur[13] mais des études nutritionnelles chez les mammifères l'impliquent comme facteur de bonne santé et suggèrent qu'il doit être considéré comme un élément-trace essentiel avec une DJA de l'ordre de 1 mg/jour[15]. Une étude épidémiologique observationnelle récente (2011) indiquerait un lien entre entre le taux de lithium dans l'eau de boisson et la longévité[15].
Gisements
Le lithium est bien moins abondant que les alcalins et alcalino-terreux usuels (Na, K, Mg, Ca) même s'il est largement distribué dans la nature (ce n'est que le 33e élément le plus abondant sur Terre[16]).
On ne le trouve pas sous sa forme métallique à cause de sa grande réactivité, et il n'existe, en concentration permettant une exploitation économique rentable qu'en très peu d'endroits sur Terre. On le trouve principalement comme impureté dans les sels d'autres métaux alcalins, sous forme principalement de :
- chlorures (LiCl), essentiellement dans les saumures de certains vieux lacs salés continentaux et mélangé à d'autres sels de métaux alcalins ;
- silicates, dont spodumène, LiAl (Si2O6)) ou petalite (Li(AlSi4O10)) dans la pegmatite ;
- l’hectorite, une sorte d'argile de formule Na0,4Mg2,7Li0,3Si4O10 (OH)2, issue de l'altération de certaines roches volcaniques ;
- jadarite, Li Na Si B3 O7 (OH) qui est un borate.
L'USGS évaluait en 2009 les ressources mondiales exploitables à 11 millions de tonnes (USGS)[17].
Le plus grand gisement au monde est le Salar de Uyuni, dans le département de Potosí, au sud-ouest de la Bolivie. Ce gisement représente un tiers des ressources mondiales et intéresse beaucoup le groupe Bolloré[18]. Le Chili possède le deuxième plus grand gisement avec le salar d'Atacama. L'Argentine possède également un gisement de lithium, avec le salar del Hombre Muerto, à une centaine de kilomètres au nord d'Antofagasta de la Sierra, dans le nord-ouest du pays. Ce gisement est difficile d'accès, il n'y a que des pistes en terre naturelle pour y parvenir.
D'autres gisements sont exploités notamment des lacs salés au Tibet ainsi que des mines en Australie, en Russie et aux États-Unis. Le Chili est devenu le premier exportateur mondial depuis 1997, la compagnie allemande Chemettall en étant l'opérateur principal[18]. En mars 2008, la Bolivie a autorisé l'exploitation du lithium sur le lac salé fossile d'Uyuni et la création d'une usine d'extraction[18].
Les eaux géothermiques de Salton Sea (Californie) sont aussi riches en lithium que les lacs salés boliviens et chiliens. Un procédé original et récent a permis d'en extraire du lithium pur. Le premier prototype de démonstration espère produire environ 1 tonne de métal de lithium par mois [19],[20]; Un gisement a été découvert en 2010 dans les environs de la Baie James au Canada.
De très importantes réserves en Afghanistan ont été récemment (juin 2010) évoquées dans la presse [21],[22].
Économie
Les principaux producteurs sont le Chili, avec le Salar d'Atacama (39,3 % de la production mondiale), la Chine (13,3 %) et l'Argentine (9,8 %), selon les statistiques du Meridian International Research[23].
La production annuelle est estimée en 2007 à 25000 tonnes selon le service de géologie des États-Unis (USGS)[18],[24].
La demande ayant explosé, notamment pour la production de batteries en lithium-ion pour le marché de l'informatique et de la téléphonie, le prix du lithium est passé d'environ 310 €/tonne à 2 000 €/tonne (350 $/tonne à près de 3 000 $/tonne) entre 2003 et 2008[18].
Les réserves mondiales de lithium étaient estimées par l'USGS à plus de 11 millions de tonnes[25]. Ces chiffres sont contestés par le cabinet Meridian International Research, qui pense que les réserves actuelles pourraient ne pas suffire pour une utilisation massive dans les batteries lithium-ion[26].
Environnement
Le lithium métallique réagit avec l'azote, l'oxygène et la vapeur d'eau dans l'air. Par conséquent, la surface de lithium devient un mélange d'hydroxyde de lithium (LiOH), de carbonate de lithium (Li2CO3) et de nitrure de lithium (Li3N), l'hydroxyde de lithium étant corrosif du fait de son pH fortement basique. Une attention spéciale devrait être portée aux organismes aquatiques (toxicité de l'ion lithium en milieu aquatique).[réf. nécessaire]
Notes et références
- (en) David R. Lide, CRC Handbook of Chemistry and Physics, CRC Press Inc, 2009, 90e éd., Relié, 2804 p. (ISBN 978-1-420-09084-0)
- (en) Beatriz Cordero, Verónica Gómez, Ana E. Platero-Prats, Marc Revés, Jorge Echeverría, Eduard Cremades, Flavia Barragán et Santiago Alvarez, « Covalent radii revisited », dans Dalton Transactions, 2008, p. 2832 - 2838 [lien DOI]
- « Lithium, elemental » dans la base de données Hazardous Substances Data Bank, consulté le 1 mai 2010
- "Ionization Energies of Atoms and Atomic Ions," in CRC Handbook of Chemistry and Physics, 91st Edition (Internet Version 2011), W. M. Haynes, ed., CRC Press/Taylor and Francis, Boca Raton, FL., p. 10-203
- Entrée de « Lithium » dans la base de données de produits chimiques GESTIS de la IFA (organisme allemand responsable de la sécurité et de la santé au travail) (allemand, anglais), accès le 26 mars 2011 (JavaScript nécessaire)
- SIGMA-ALDRICH
- « Lithium » dans la base de données de produits chimiques Reptox de la CSST (organisme québécois responsable de la sécurité et de la santé au travail), consulté le 25 avril 2009
- Numéro index dans le tableau 3.1 de l'annexe VI du règlement CE N° 1272/2008 (16 décembre 2008)
- (en) USGS Minerals « Lithium. »
- (en) Katharina Lodders, « Solar System Abundances and Condensation Temperatures of the Elements », dans The Astrophysical Journal, vol. 591, no 2, 2003, p. 1220 [texte intégral, lien DOI (pages consultées le 7 février 2011)]
- Dr Elie Hantouche (psychiatre) et Régis Blain, La Cyclothymie, pour le pire et le meilleur, éditions Robert Lafont, 254 pages. Dr Christian Gay (psychiatre), Vivre avec un maniaco-dépressif, Hachette Littératures, 211 pages.
- http://education.jlab.org/itselemental/ele003.html
- Some Facts about Lithium, ENC Labs. Consulté le 2010-10-15
- C Chassard-Bouchaud, « Bioaccumulation of lithium by marine organisms in European, American, and Asian coastal zones: microanalytic study using secondary ion emission », dans Comptes rendus de l'Academie des sciences. Serie III, Sciences de la vie, vol. 299, no 18, 1984, p. 719–24 [lien PMID]
- K.Zarse et al., Low-dose lithium uptake promotes longevity in humans and metazoans, European Journal of Nutrition, 2001, vol.50(5), pp. 387-389. DOI:10.1007/s00394-011-0171-x, résumé.
- http://www.enerzine.com/14/4503+le-lithium-du-tibet+.html
- http://minerals.usgs.gov/minerals/pubs/commodity/lithium/mcs-2008-lithi.pdf Chiffres de la production de lithium à l'échelle mondiale, USGS, 7 janvier 2009
- http://www.lemonde.fr/planete/article/2008/10/07/les-ressources-limitees-de-lithium-pourraient-freiner-l-essor-des-voitures-electriques_1103972_3244.html Les ressources limitées de lithium pourraient freiner l'essor des voitures électriques, Le Monde, 7 octobre 2008
- http://www.enerzine.com/4/8869+les-centrales-geothermiques-fourniront-aussi-du-lithium+.html
- http://www.physorg.com/news179999592.html
- http://www.nytimes.com/2010/06/14/world/asia/14minerals.html U.S. Identifies Vast Mineral Riches in Afghanistan
- http://www.alterinfo.net/L-Afghanistan-est-riche-en-matieres-premieres-et-en-mineraux-Qui-va-les-exploiter_a43028.html L’Afghanistan est riche en matières premières et en minéraux - Qui va les exploiter?
- http://www.lefigaro.fr/international/2009/09/08/01003-20090908ARTFIG00367-la-bolivie-futur-moyen-orient-du-lithium-.php
- http://minerals.usgs.gov/minerals/pubs/commodity/lithium/mcs-2008-lithi.pdf Chiffres de la production de lithium à l'échelle mondial, USGS, 7 janvier 2009
- Données sur le lithium, source USGS
- The trouble with lithium, étude du cabinet Meridain International Resarch]
Voir aussi
Articles connexes
s1 s2 g f1 f2 f3 f4 f5 f6 f7 f8 f9 f10 f11 f12 f13 f14 d1 d2 d3 d4 d5 d6 d7 d8 d9 d10 p1 p2 p3 p4 p5 p6 1 H He 2 Li Be B C N O F Ne 3 Na Mg Al Si P S Cl Ar 4 K Ca Sc Ti V Cr Mn Fe Co Ni Cu Zn Ga Ge As Se Br Kr 5 Rb Sr Y Zr Nb Mo Tc Ru Rh Pd Ag Cd In Sn Sb Te I Xe 6 Cs Ba La Ce Pr Nd Pm Sm Eu Gd Tb Dy Ho Er Tm Yb Lu Hf Ta W Re Os Ir Pt Au Hg Tl Pb Bi Po At Rn 7 Fr Ra Ac Th Pa U Np Pu Am Cm Bk Cf Es Fm Md No Lr Rf Db Sg Bh Hs Mt Ds Rg Cn Uut Uuq Uup Uuh Uus Uuo 8 Uue Ubn * Ute Uqn Uqu Uqb Uqt Uqq Uqp Uqh Uqs Uqo Uqe Upn Upu Upb Upt Upq Upp Uph Ups Upo Upe Uhn Uhu Uhb Uht Uhq Uhp Uhh Uhs Uho ↓ g1 g2 g3 g4 g5 g6 g7 g8 g9 g10 g11 g12 g13 g14 g15 g16 g17 g18 * Ubu Ubb Ubt Ubq Ubp Ubh Ubs Ubo Ube Utn Utu Utb Utt Utq Utp Uth Uts Uto Métalloïdes Non-métaux Halogènes Gaz rares Métaux alcalins Métaux alcalino-terreux Métaux de transition Métaux pauvres Lanthanides Actinides Superactinides Éléments non classés Catégories :- Produit chimique corrosif
- Produit chimique facilement inflammable
- Produit chimique qui réagit avec l'eau
- Élément chimique
- Métal alcalin
- Lithos
Wikimedia Foundation. 2010.