- 106-51-4
-
1,4-benzoquinone
1,4-benzoquinone 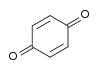
Général Nom IUPAC cyclohexa-2,5-diene-1,4-dione Synonymes p-benzoquinone
p-quinoneNo CAS No EINECS PubChem SMILES InChI Apparence cristaux jaunes ou solide jaune, d'odeur âcre. peut sublimer même à température ambiante[1]. Propriétés chimiques Formule brute C6H4O2 [Isomères] Masse molaire 108,0948 g∙mol-1
C 66,67 %, H 3,73 %, O 29,6 %,Propriétés physiques T° fusion 115,7 °C[2] T° ébullition +/- 108 °C[1] Solubilité 10 g∙l-1 (eau, 25 °C)[2] Masse volumique 1,32 g∙cm-3 à 20 °C[2] T° d’auto-inflammation 560 °C[2] Point d’éclair 38 à 93 °C[2] Thermochimie ΔfH0solide -186,8 kJ∙mol-1[3] ΔfusH° 18,45 kJ∙mol-1 à 112,9 °C[3] Cp 126,4 J∙K-1∙mol-1 (25 °C, solide)
107,37 J∙K-1∙mol-1 (25 °C, gaz)[3]PCI -2 725,8 kJ∙mol-1[3] Précautions Directive 67/548/EEC 
T
NPhrases R : 23/25, 36/37/38, 50, Phrases S : (1/2), 26, 28, 45, 61, Transport 60 2587 NFPA 704 SGH[5] 

DangerClassification du CIRC Groupe 3 : Inclassable quant à sa cancérogénicité pour l'Homme[4] Écotoxicologie DL50 8.5 mg/kg (souris, oral)
130 mg/kg (rat, oral)[6]LogP 0.2[1] Composés apparentés Isomère(s) 1,2-benzoquinone Autres composés Plastoquinone Unités du SI & CNTP, sauf indication contraire. La 1,4-benzoquinone ou cyclohexa-2,5-diène-1,4-dione est une cétone de formule brute C6H4O2. C'est un des deux isomères de la quinone, l'autre étant la 1,2-benzoquinone. Ce composé non aromatique est le dérivé oxydé de l'hydroquinone (benzène-1,4-diol)[7]. Cette molécule présente les propriété d'une cétone et d'un alcène.
Utilisation
Cette molécule est utilisée en synthèse organique comme accepteur de proton et comme agent oxydant[8]. Elle peut aussi être utilisée comme diénophile dans les réactions de Diels-Alder[9]. Est utilisé comme intermédiaire pour la synthèse des substances suivantes
- 1,4-Naphtoquinone, obtenue par oxydation du naphtalène en présence de trioxyde de chrome[10].
- 2,3-dichloro-5,6-dicyano-1,4-benzoquinone (ou DDQ), un puissant agent oxydant et déshydrogénant
- Ubiquinone-1
- Chloro-p-benzoquinone[11]
- Chloranile, 1,4-C6Cl4O2, un puissant agent oxydant et déshydrogénant
Production et synthèse
Notes et références
- ↑ a , b et c p - BENZOQUINONE, fiche de sécurité du Programme International sur la Sécurité des Substances Chimiques, consultée le 9 mai 2009
- ↑ a , b , c , d et e Entrée de « p-Benzoquinone » dans la base de données de produits chimiques GESTIS de la BGIA (organisme allemand responsable de la sécurité et de la santé au travail) (allemand, anglais), accès le 11 février 2009 (JavaScript nécessaire)
- ↑ a , b , c et d p-Benzoquinone sur http://www.nist.gov/. Consulté le 11 février 2009
- ↑ IARC Working Group on the Evaluation of Carcinogenic Risks to Humans, « Evaluations Globales de la Cancérogénicité pour l'Homme, Groupe 3 : Inclassables quant à leur cancérogénicité pour l'Homme » sur http://monographs.iarc.fr, 16 janvier 2009, CIRC. Consulté le 22 août 2009
- ↑ Numéro index dans le tableau 3.1 de l'annexe VI du règlement CE N° 1272/2008 (16 décembre 2008)
- ↑ (en) « 1,4-Benzoquinone » sur ChemIDplus, consulté le 11 février 2009
- ↑ H. W. Underwood, Jr. & W. L. Walsh, Org. Synth 1943, Coll. Vol. 2, p 553
- ↑ Yang, T.-K.; Shen, C.-Y. ”1,4-Benzoquinone” in Encyclopedia of Reagents for Organic Synthesis (Ed: L. Paquette) 2004, J. Wiley & Sons, New York. DOI:10.1002/047084289
- ↑ Oda, M., Kawase, T., Okada, T., Enomoto, T., Org. Synth. 1998, Coll. Vol. 9, p186
- ↑ Braude E. A., Fawcett J. S., Org. Synth. 1963, Coll. Vol. 4, p698
- ↑ Harman R. E., Org. Synth. 1963, Coll. Vol. 4, p148
- Portail de la chimie
Catégories : Produit chimique toxique | Produit chimique dangereux pour l'environnement | Quinone
Wikimedia Foundation. 2010.


