- 1,4-dioxane
-
1,4-Dioxane 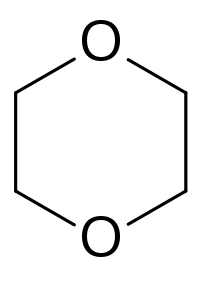
1-4-Dioxane Général Nom IUPAC 1-4-Dioxane
1,4-DioxacyclohexaneSynonymes Dioxyde de diéthylène
Oxyde diéthylénique
p-DioxaneNo CAS No EINECS SMILES InChI Apparence liquide incolore, d'odeur caractéristique[1]. Propriétés chimiques Formule brute C4H8O2 [Isomères] Masse molaire[2] 88,1051 ± 0,0044 g·mol-1
C 54,53 %, H 9,15 %, O 36,32 %,Propriétés physiques T° fusion 12 °C[1] T° ébullition 101 °C[1] Solubilité dans l'eau : miscible[1] Masse volumique 1,03 g·cm-3[1] T° d'auto-inflammation 180 °C[1] Point d’éclair 12 °C[1] Limites d’explosivité dans l’air 2–22,5 % vol[1] Pression de vapeur saturante 38 mbar à 20 °C
68 mbar à 30 °C
159 mbar à 50 °CPoint critique 52,1 bar, 313,85 °C [3] Précautions Directive 67/548/EEC 
Xn
FPhrases R : 11, 19, 36/37, 40, 66, Phrases S : (2), 9, 16, 36/37, 46, Transport 33 1165 NFPA 704 SIMDUT[5] 

SGH[6] 

DangerClassification du CIRC Groupe 2B : Peut-être cancérogène pour l'homme[4] Inhalation Maux de tête. Nausées.
Toux. Mal de gorge.
Douleurs abdominales. Vertiges.
Somnolence. Vomissements.
Perte de conscience.Peau PEUT ETRE ABSORBE ! Rougeur. Yeux Rougeur. Douleur. Larmoiement. Ingestion (Voir Inhalation). Écotoxicologie LogP -0,42[1] Seuil de l’odorat bas : 0,8 ppm
haut : 172 ppm[7]Unités du SI & CNTP, sauf indication contraire. Le 1,4-dioxane est l'un des trois isomères du dioxane.
Sommaire
Propriétés
- Concentration à saturation : 38 000 ppm
- Coefficient de partage (eau/huile) : 2,6
- Limite de détection olfactive : 24,00 ppm
- Facteur de conversion (ppm→mg/m³) : 3,603
- Taux d'évaporation (éther=1) : 5,8
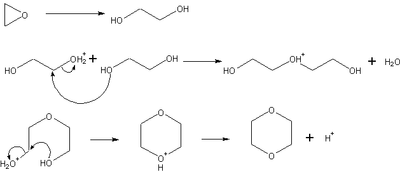
Synthèse
Le 1,4-dioxane peut être synthétisé à partir de l'époxyéthane.
Dans un premier temps, l'époxyéthane subit une hydratation (catalysée par un acide fort, acide sulfurique concentré par exemple) pour former de l'éthan1,2-diol (glycol). La deuxième étape est une substitution nucléophile bimoléculaire (SN2), catalysée par un acide fort, entre deux molécules de glycol. La dernière étape est une SN2 intramoléculaire, toujours catalysée par un acide fort, suivie d'une déprotonation.
Utilisations
Le 1,4-dioxane est avant tout utilisé dans des solvants pour le secteur de la manufacture. On le trouve aussi dans les fumigènes et dans les liquides de refroidissement. Il est aussi utilisé comme agent moussant. C'est un sous-produit accidentel des procédés d'éthoxylation dans la fabrique de cosmétiques. Il peut ainsi contaminer des produits comme les déodorants, shampoings, dentifrice ou liquide pour bain de bouche.
Il est aussi utilisé comme solution-étalon pour calibrer des appareils de RMN, comme le tétraméthylsilane.
Toxicté
Effet cancérogène
Le 1,4-dioxane est cancérogène chez l'animal, il produit des tumeurs hépatiques et nasales. Il est classé cancérogène catégorie 3 par l'UE et dans le groupe 2B (cancerogène possible pour l'homme) par le CIRC[8].
Notes et références
- 1, 4 - DIOXANNE, fiche de sécurité du Programme International sur la Sécurité des Substances Chimiques, consultée le 9 mai 2009
- Masse molaire calculée d’après Atomic weights of the elements 2007 sur www.chem.qmul.ac.uk.
- Properties of Various Gases sur flexwareinc.com. Consulté le 12 avril 2010
- IARC Working Group on the Evaluation of Carcinogenic Risks to Humans, « Evaluations Globales de la Cancérogénicité pour l'Homme, Groupe 2B : Peut-être cancérogènes pour l'homme » sur http://monographs.iarc.fr, CIRC, 16 janvier 2009. Consulté le 22 août 2009
- « Dioxane » dans la base de données de produits chimiques Reptox de la CSST (organisme québécois responsable de la sécurité et de la santé au travail), consulté le 23 avril 2009
- Numéro index dans le tableau 3.1 de l'annexe VI du règlement CE N° 1272/2008 (16 décembre 2008)
- 1,4-Dioxane sur hazmap.nlm.nih.gov. Consulté le 14 novembre 2009
- Fiche toxicologique n°28: 1,4-dioxane, INRS
Catégories :- Produit chimique nocif
- Produit chimique facilement inflammable
- Cancérogène chimique
- Dioxane
- Cancérogène du groupe 2B du CIRC
Wikimedia Foundation. 2010.