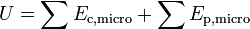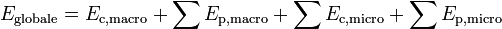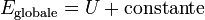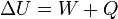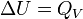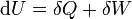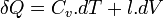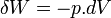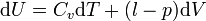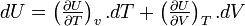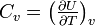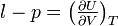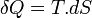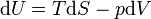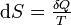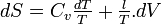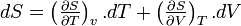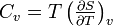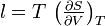- Energie interne
-
Énergie interne
Potentiels thermodynamiques Énergie interne U(S,V,N) Énergie libre F(T,V,N) = U − TS Enthalpie H(S,p,N) = U + pV Enthalpie libre G(T,p,N) = U + pV − TS modifier Un système thermodynamique est un objet constitué de molécules ou d’atomes qui possède une énergie totale pouvant être décomposée en deux parties:
- une énergie cinétique correspondant au mouvement de l’objet dans son ensemble ainsi qu’aux mouvements des particules qui le constituent,
- une énergie potentielle due aux interactions de l’objet avec le milieu extérieur par l’intermédiaire de champs, gravitationnel, électriques ou magnétiques mais aussi due aux interactions entre les molécules, ions, atomes, électrons, noyaux, nucléons… qui constituent ce système.
Il existe donc deux niveaux de réalité pour l’énergie totale du système :
- Un niveau macroscopique, sensible à nos sens c’est-à-dire à notre échelle humaine, correspondant à l’énergie cinétique macroscopique du système en mouvement dans un référentiel donné :
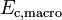 et aux énergies potentielles macroscopiques du système placé dans des champs de gravitation, électriques ou magnétiques :
et aux énergies potentielles macroscopiques du système placé dans des champs de gravitation, électriques ou magnétiques : 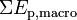 .
. - Un niveau microscopique inaccessible à nos sens, correspondant aux énergies cinétiques microscopiques que l’on peut assimiler à l’agitation thermique des particules :
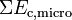 et à toutes les énergies potentielles d’interactions microscopiques que l’on peut assimiler, entre autres, aux énergies de liaison chimique et aux énergies d’interactions entre les nucléons (énergies nucléaires) :
et à toutes les énergies potentielles d’interactions microscopiques que l’on peut assimiler, entre autres, aux énergies de liaison chimique et aux énergies d’interactions entre les nucléons (énergies nucléaires) : 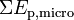 .
.
L’énergie interne U d'un système thermodynamique correspond à la somme de ses énergies microscopiques.
Sommaire
Énergie globale et énergie interne d'un système
L’énergie globale d'un système peut s’écrire :
Énergie interne
Par définition, la somme des énergies microscopiques constitue l’énergie interne U du système, c’est-à-dire son énergie propre :
Étant donné la complexité des interactions au niveau microscopique, l’énergie interne U n’est pas calculable et c’est ce qui explique que la plupart des fonctions d’état du système, qui en dépendent (exceptée l’entropie S), ne sont pas connues de façon absolue. On peut uniquement calculer leur variation. L’énergie interne est une fonction d'état du système. Sa variation ne dépend que de l’état final et de l’état initial d’équilibres et non pas de la nature de la transformation. Sa différentielle dU est une différentielle totale exacte.
Application aux systèmes physico-chimiques
Dans le cas d’une réaction chimique, le système réactionnel sera au repos à l’échelle macroscopique (le réacteur n’est pas en mouvement dans les champs de gravitation, électriques et magnétiques). Son énergie macroscopique reste donc constante.
La variation d’énergie du système au cours de la réaction chimique est donc égale à la variation de son énergie interne :
Le premier principe de la thermodynamique indique qu’il y a conservation de l’énergie et dans ce cas si l’énergie interne du système varie c’est qu’il y a échange d’énergie avec le milieu extérieur soit sous forme de travail
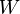 soit sous forme de chaleur
soit sous forme de chaleur 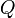 . On suppose bien évidemment que le système est fermé et donc qu'il n'y a pas d'échange de matière.
. On suppose bien évidemment que le système est fermé et donc qu'il n'y a pas d'échange de matière.On peut écrire :
Cette expression est la plus utilisée pour résumer l'énoncé du premier principe de la thermodynamique.
Si le système est isolé c’est-à-dire s'il n'y a aucun échange avec le milieu extérieur,
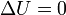 : l'énergie interne reste constante.
: l'énergie interne reste constante.
Si la transformation est cyclique, le système revient à son état initial et comme l'énergie interne est une fonction d'état,
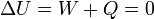 : l'énergie interne reste constante et
: l'énergie interne reste constante et 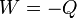 .
.
Si le volume
 est constant (transformation isochore) et si le travail mis en jeu n'est dû qu'aux forces de pression, alors le travail est nul. D'où :
est constant (transformation isochore) et si le travail mis en jeu n'est dû qu'aux forces de pression, alors le travail est nul. D'où :Dans ces conditions la chaleur mise en jeu devient égale à la variation de la fonction d'état
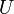 et ne dépend plus du chemin suivi. Cette propriété est à la base de la calorimétrie à volume constant pratiquée dans une bombe calorimétrique.
et ne dépend plus du chemin suivi. Cette propriété est à la base de la calorimétrie à volume constant pratiquée dans une bombe calorimétrique.Formes différentielles de l'énergie interne et coefficients calorimétriques
- D'après le premier principe de la thermodynamique
or
Dans le cas où seules des forces de pression sont en jeu :
donc
- Coefficients calorimétriques
L'énergie interne est une fonction d'état et sa différentielle est totale exacte.
Donc
- D'après le second principe de la thermodynamique
d'où
- Coefficients calorimétriques
Or l'entropie est une fonction d'état et sa différentielle totale est exacte.
Il s'ensuit que
Voir aussi
Articles connexes
- Portail de la physique
- Portail de la chimie
Catégories : Thermodynamique | Thermochimie
Wikimedia Foundation. 2010.