- 87-66-1
-
Pyrogallol
Pyrogallol 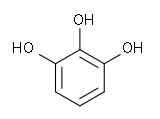
structure du pyrogallol Général Nom IUPAC 1,2,3-Trihydroxybenzène Synonymes acide Pyrogallique
C.I. 76515No CAS No EINECS PubChem SMILES InChI Apparence sans odeur poudre cristalline blanche. devient gris, expose à la lumiere et à l'air.[1] Propriétés chimiques Formule brute C6H6O3 [Isomères] Masse molaire 126,11 g∙mol-1
C 57,14 %, H 4,8 %, O 38,06 %,Propriétés physiques T° fusion 131 à 134 °C[1] T° ébullition 309 °C[1] Solubilité dans l'eau : bonne (60 g/100 ml à 20 °C)[1] Masse volumique (eau = 1) : 1.45[1] Point d’éclair < 55 °C Pression de vapeur saturante à 168 °C : 1.33 kPa[1] Précautions Directive 67/548/EEC 
XnPhrases R : 20/21/22, 52/53, 68, Phrases S : (2), 36/37, 61, SIMDUT[2] 
SGH[3] 
AttentionInhalation Bleuissement des ongles ou des lèvres. Bleuissement de la peau. Toux. Vertiges. Maux de tête. Respiration difficile. Nausées. Essoufflement. Mal de gorge. Peau Peut être absorbée. Décoloration locale. Rougeur. Douleur. Yeux Rougeur. Douleur. Ingestion Nausées. Douleurs abdominales. Vomissements. Faiblesse. Composés apparentés Isomère(s) Phloroglucinol Unités du SI & CNTP, sauf indication contraire. Le pyrogallol ou benzène-1,2,3-triol est un solide cristallin de couleur blanche utilisé comme réducteur en photographie.
Sommaire
Préparation
Il a été préparé pour la première fois par Carl Wilhelm Scheele en 1786 en chauffant de l'acide gallique. Une autre préparation possible est le chauffage de l'acide para-chlorophénoldisulphonique en présence de potasse.
Propriétés
En solution basique, il absorbe facilement l'eau, teintant une solution à l'origine incolore en violet. Le pyrogallol possède aussi des propriétés antiseptiques.
Utilisations
- En chimie, du fait qu'il absorbe l'oxygène, il peut être utilisé pour piéger des traces d'oxygène résiduel dans un système devant rester anoxique, ou parfois encore pour mesurer le taux d'oxygène dans un mélange gazeux.
- Il a été et est encore parfois utilisé dans certaines teintures pour cheveux, mais cet usage est a présent restreint, le pyrogallol étant soupçonné d'être toxique.
- Historiquement, le pyrogallol a servi de révélateur pour les tirages en noir et blanc. A quelques exceptions, pour des usages spécifiques, cet usage est grandement révolu et on préfère actuellement utiliser des développeurs comme l'hydroquinone.
Utilisation en photographie
Bien que populaire agent de développement photographique au XIXe siècle et début du XXe siècle, le pyrogallol est largement tombé en désuétude dans les années 1920, bien que toujours utilisé par quelques grands photographes, tels Edward Weston. Il avait en effet la réputation d'avoir un comportement erratique et d'être peu fiable en raison probablement de ses propriétés rédox. Le pyrogallol a connu un renouveau à partir des années 1980, largement grâce aux efforts de Gordon Hutchings. Hutchings a passé plus d'une décennie sur des formules de pyrogallol, et en produisit une qu'il nomma PMK (pour ses principaux ingrédients, Pyrogallol, Métol, et Kodalk (métaborate de sodium de la marque Kodak)).
Voir aussi
- Stéréoisomères :
- phloroglucinol (benzène-1,3,5-triol)
- benzène-1,2,4-triol (2-hydroxy 1,4-benzoquinone)
- Phénol
- Polyphénol
- Pyrocatéchol
Notes et références
- ↑ a , b , c , d , e et f ACIDE PYROGALLIQUE, fiche de sécurité du Programme International sur la Sécurité des Substances Chimiques, consultée le 9 mai 2009
- ↑ « Pyrogallol » dans la base de données de produits chimiques Reptox de la CSST (organisme canadien responsable de la sécurité et de la santé au travail), consulté le 25 avril 2009
- ↑ Numéro index dans le tableau 3.1 de l'annexe VI du règlement CE N° 1272/2008 (16 décembre 2008)
- Portail de la chimie
- Portail de la photographie
Catégories : Produit chimique nocif | Produit chimique dangereux pour l'environnement | Polyphénol | Réducteur | Technique photographique
Wikimedia Foundation. 2010.
