- Atome D'hydrogène
-
Atome d'hydrogène
Pour consulter un article plus général, voir : atome.L'atome d'hydrogène est un atome composé d'un proton et d'un électron. C'est l'atome le plus simple qui existe et le premier élément de la classification périodique. L'électron et le proton sont liés par la force de Coulomb, étant donné que leurs charges sont opposées.
La compréhension de la théorie quantique de cet atome fut très importante car elle a notamment permis de développer la théorie des atomes à N électrons, mais aussi de valider les théories de la physique quantique au fur et à mesure des progrès accomplis : d'abord l'ancienne théorie des quanta[1], la mécanique quantique non relativiste, puis la mécanique quantique relativiste de Dirac, et enfin la théorie quantique des champs.
Dans le cadre de la mécanique quantique, l'atome d'hydrogène est modélisé comme un problème à deux corps, et est soluble analytiquement. Il est ainsi possible d'en déduire les niveaux d'énergie, et de les comparer aux mesures des raies spectrales.
Sommaire
Note d'histoire : la période 1913-1925
L'étude du spectre de l'atome d'hydrogène avait déjà été effectuée de façon empirique par Balmer (1825-1898) au 19e siècle. La mise en évidence de régularités dans le spectre, inexplicable par la théorie classique, fut longtemps une énigme. En 1913, la théorie de l'atome de Bohr ne put pas expliquer le cas du moment cinétique nul, mais elle introduit une hypothèse ad hoc selon laquelle les orbites était quantifiées, ce qui était inconciliable avec la théorie classique.
Ce modèle n'était pas satisfaisant, car il ne permettait pas d'expliquer la spectroscopie des éléments, comme l'hélium[2], bien que très vite, Bohr put expliquer la spectroscopie des ions He+ et Li++.
On savait qu'il existait, en spectroscopie, deux « sortes » d'hélium, mais l'énigme restait entière, et ne relevait pas du tout de l'astuce de l'hydrogène de Pickering[3]. L'apport de Sommerfeld en introduisant la théorie des ellipses de Rutherford permit bien d'introduire la notion de moment cinétique orbital, mais fut une impasse. La théorie de Bohr fut contredite par l'effet Zeeman, et par la théorie du moment cinétique quantique de Pauli. Il était impossible d'expliquer le spectre de l'atome d'hydrogène pour les raies très voisines, correspondant à la structure fine. Dès 1924, Pauli comprend la notion de spin de l'électron et introduit son incompréhensible principe d'exclusion de Pauli qui ne deviendra un théorème que dans la théorie quantique relativiste. Grâce à ce principe et à l'« Aufbau-prinzip », la classification périodique commence à recevoir un statut plus théorique.
L'équation de Schrödinger d'évolution ou dépendant du temps
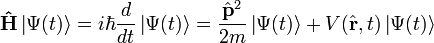
L'observable position
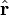 est réduite, ici, à la distance au noyau. Et l'observable impulsion est
est réduite, ici, à la distance au noyau. Et l'observable impulsion est 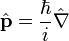 , d'après l'explication magistrale (postérieure) de Dirac. Et on rappelle que d'après Born, Ψ(r,t) est l'amplitude de probabilité de présence de l'électron (1927). Cela lui donnera le prix Nobel en 1954.
, d'après l'explication magistrale (postérieure) de Dirac. Et on rappelle que d'après Born, Ψ(r,t) est l'amplitude de probabilité de présence de l'électron (1927). Cela lui donnera le prix Nobel en 1954.Cette théorie avait pour fondement la notion mathématique des opérateurs linéaires dits observables (de l'opérateur hermitien, complet) dans un espace vectoriel abstrait, muni de la structure d'espace de Hilbert;
de ce fait la théorie fut autrefois appelée : mécanique des matrices, inventée dès 1925 par Heisenberg et utilisée brillamment par Pauli pour trouver le spectre de l'hydrogène, dès 1925. Mais cette théorie de Pauli était trop en avance sur son temps.
- Schrödinger, dès 1926, montra que la théorie d'Heisenberg se réduisait à la sienne, et que sa théorie donnait, grâce à sa fameuse fonction d'onde Ψ(r,t),(encore incomprise en 1926), TOUT sur l'état stationnaire de l'électron « autour du noyau », SANS TRAJECTOIRE (mais ceci ne fut compris qu'en 1929/1930 grâce à Born, Jordan et Von Neumann, puis Dirac).
- On se doit de noter, ici, l'absence de deux grands physiciens : Einstein et Bohr. Leurs correspondances de 1926 à 1935 montrent qu'ils auraient tellement voulu que cette théorie soit pleinement compréhensible !
- Cela étant, la Théorie de Pauli de l'atome d'hydrogène était pourtant vraiment la plus profonde, et cela est maintenant reconnu par tous les récents ouvrages (environ depuis 1964).
Complètement acquise au XXIe siècle, via le vecteur de Runge-Lenz quantique, la théorie de Pauli est ENFIN en pleine lumière, après plus de quatre-vingt ans ! C'est dire que le progrès de l'interdisciplinarité (ici théorie mathématique de l'intégrabilité et symétrie en chimie) est lent.
Ainsi, Schrödinger put donc déduire en 1926 le spectre de l'hydrogène à partir des valeurs propres de l'opérateur linéaire
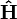 , appelé « hamiltonien » :
, appelé « hamiltonien » :- ses valeurs propres redonnaient exactement les valeurs de l'énergie trouvées dans l'ancienne théorie de l'atome de Bohr (1913),
mais il obtint bien plus :
- les fonctions d'onde de chaque valeur propre, c’est-à-dire la probabilité de trouver l'électron à telle ou telle position en régime stationnaire (cf orbitale de l'atome d'hydrogène).
Cela dit, résoudre l'équation précédente est un effort mathématique très difficile pour tout physicien non rompu à la pratique des équations aux dérivées partielles. Mais plus encore, la disparition de la notion de trajectoire et le concept d'électronde remplaçant celui d'un électron fut TRÈS difficile à admettre (cf mécanique quantique). C'est CELA qui explique la "réticence" d'Einstein. Et, c'est une heureuse chance que l'équation pour l'atome d'hydrogène fût intégrable !
Equation de Schrödinger stationnaire ou indépendante du temps
Cette équation, la plus utilisée en pratique, ne découle pas de façon évidente de la précédente, nous ne la démontrerons donc pas ici. L'expression de l'équation de Schrödinger indépendante du temps est
où
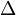 est le laplacien. V est le potentiel coulombien du proton, indépendant du temps et E-V l'énergie cinétique de l'électron :
est le laplacien. V est le potentiel coulombien du proton, indépendant du temps et E-V l'énergie cinétique de l'électron :Le laplacien, en coordonnées sphériques, s'écrit:
La résolution complète de l'équation de Schrödinger de l'atome d'hydrogène est compliquée mais on peut la simplifier sachant que les niveaux d'énergie de type s, de symétrie sphérique, sont les mêmes que ceux qu'on obtient avec la théorie de Bohr. La théorie de Schrödinger la complète en faisant apparaître les modes de vibration angulaires en plus des modes radiaux: ce sont les harmoniques sphériques. On en trouvera la résolution chez Feynman[4].
État fondamental
En fait, dans le cas de l'atome d'hydrogène, on peut trouver la solution de l'état fondamental (c'est-à-dire de plus basse énergie) rigoureusement, en s'aidant uniquement du principe d'incertitude d'Heisenberg. C'est une façon très élégante de procéder, sans beaucoup de mathématiques.
En effet, très vite, (en 1929), Werner Heisenberg fait comprendre un des points-clefs de la mécanique quantique : Les grandeurs physiques ne sont plus des fonctions
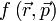 de l'espace de la position et de la vitesse (appelé en mécanique classique hamiltonienne, l'espace des phases) : cet espace n'est pas pertinent en mécanique quantique. Les grandeurs physiques
de l'espace de la position et de la vitesse (appelé en mécanique classique hamiltonienne, l'espace des phases) : cet espace n'est pas pertinent en mécanique quantique. Les grandeurs physiques 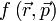 doivent être remplacées par des opérateurs linéaires observables sur un espace vectoriel (de Hilbert) et les valeurs propres, réelles, de ces matrices seront les valeurs expérimentalement mesurées. Comme l'opérateur position
doivent être remplacées par des opérateurs linéaires observables sur un espace vectoriel (de Hilbert) et les valeurs propres, réelles, de ces matrices seront les valeurs expérimentalement mesurées. Comme l'opérateur position 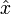 et l'opérateur impulsion
et l'opérateur impulsion 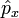 ne commutent pas, il en résulte le théorème d'inégalité de Heisenberg) :
ne commutent pas, il en résulte le théorème d'inégalité de Heisenberg) :![[\hat p,\hat x] = i\hbar](/pictures/frwiki/54/680d0305ad707a49bc0017dcc45dc25b.png) => variance (p) . variance (x) (>ou égal)
=> variance (p) . variance (x) (>ou égal) 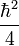 .
.
Alors, dans le cas d'égalité stricte - on dit que l'inégalité a été saturée à sa limite - la saturation des inégalités d'Heisenberg donne un moyen rigoureux de calculer la fonction d'onde,Ψ1s(x,y,z), de l'état fondamental de l'atome d'hydrogène.Ce problème de valeur propre et de vecteur propre est donc résolu, dans l'article Saturation des inégalités d'Heisenberg, pour la plus basse énergie (cf. atome de Bohr) ; et cela donne:
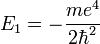
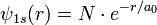
N' étant la constante, réelle, dite de normalisation de la probabilité.
Vérification
On va se contenter, ici, de vérifier que ceci est vrai en insérant directement cette solution dans l'équation de Schrödinger.
Premièrement, dans cette équation, la variable temps se sépare immédiatement :
dans ce cas dit stationnaire, cela amène à trouver les valeurs propres de l'opérateur linéaire H dans l'espace L2 des fonctions des trois variables ƒ(x, y, z) à valeur complexe, de carré sommable :
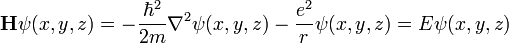 .
.
Or, dans ce cas, cette fonction uniquement de r a pour Laplacien, la valeur usuelle
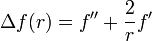 .
.De plus, on se sert évidemment des unités atomiques, qui a été introduit à cet usage. Cela revient à faire
![[ \hbar = m = e^2 = 1]](/pictures/frwiki/50/22cdd9d7aee4dde71b88888fa61fbd4b.png) dans les calculs ; Landau (p142) appelle ce système d'unités coulombiennes :
dans les calculs ; Landau (p142) appelle ce système d'unités coulombiennes :- ƒ = ƒ, ƒ' = - ƒ ;
donc il s'agit de vérifier si :
- -1/2·(ƒ + 2/r·(-ƒ)) + 1/r·ƒ = -1/2·ƒ
qui est vrai.
Densité de probabilité de présence
0n en déduit aussitôt la probabilité dp de trouver l'électron à une distance du noyau comprise entre r et r+dr : elle est donnée par dp = P(r)·dr :
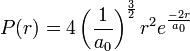 .
.
Sur le graphique de la densité de probabilité, la distance au noyau est donnée en multiple du premier rayon de Bohr, on voit immédiatement que la probabilité est maximale au premier rayon de Bohr :
Orbitale 1s
Cette solution s'appelle en chimie l'orbitale 1s.
On pourra vérifier le théorème du viriel :
- moyenne de 1/r = 1/a0
et le théorème d'Ehrenfest :
- moyenne de 1/r² = 2/a²
La moyenne de r n'est pas a, mais (3/2)·a ; [de manière générale, l'inverse de la moyenne n'est pas la moyenne de l'inverse ].
Et la moyenne de r² vaut : 3a², donc la variance de r vaut (3-9/4)·a² = 0,75·a² ; soit un écart-type = 0,866·a², ce qui est très grand.
L'électronde est dite délocalisée dans un espace, qui malgré tout reste de volume fini, au sens physique : au bout de 3a, la probabilité de détecter l'électronde est très faible (on parle d'orbitale sphérique), typiquement en chimie quantique, on convient formellement de tracer la méridienne de la surface qui englobe en gros 98 % de chance d'y trouver l'électron :
- ici r = 3/2 + 1,732 ~ 3,2·a. Ceci est très conventionnel.
Note : espace des impulsions
L'opérateur impulsion a évidemment une moyenne nulle (symétrie sphérique), mais l'opérateur P² vaut 2m·Ec, dont la valeur moyenne est par le théorème du viriel
- <P²> = -2m·Ec, soit en unités atomiques +2·1/2 = 1.
Donc la variance de P vaut
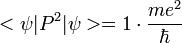 .
.On retrouve bien (heureusement!) ce dont on était parti dans l'article Saturation des inégalités d'Heisenberg.
Mais, on peut aller un peu plus loin [ ne jamais perdre de vue que l'espace des impulsions joue un rôle égal à celui des positions, bien qu'il soit moins étudié en chimie] :
Remarque : représentation dite des impulsions
- La transformée de Fourier de
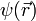 est
est 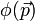 , avec la même règle de Born bien sûr :
, avec la même règle de Born bien sûr : 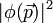 donne la densité de probabilité dans l'espace des impulsions. Le calcul de la transformée de Fourier de exp-r donne 1/(1+p²)² et donc on peut calculer de même la distribution des impulsions et retrouver la variance de p, et la valeur moyenne de l'énergie cinétique : il est très important de faire ces calculs pour bien comprendre que l'électronde, bien que dans un état stationnaire, ne cesse de « bouger » : il est aussi délocalisé en impulsion.
donne la densité de probabilité dans l'espace des impulsions. Le calcul de la transformée de Fourier de exp-r donne 1/(1+p²)² et donc on peut calculer de même la distribution des impulsions et retrouver la variance de p, et la valeur moyenne de l'énergie cinétique : il est très important de faire ces calculs pour bien comprendre que l'électronde, bien que dans un état stationnaire, ne cesse de « bouger » : il est aussi délocalisé en impulsion. - En fait, ce n'est pas une particule, ce n'est pas une onde, c'est une entité nouvelle, la « particlonde », qui ne satisfait plus les équations de la mécanique classique (dans la version dite d'Hamilton), ni l'équation des ondes de l'optique, ni l'équation de la diffusion, mais cette drôle d'équation, l'équation de Schrödinger qui ne se laisse appréhender concrètement que dans la vision lagrangienne de Dirac et Feynman(on parle d'intégrale de chemins ( et parfois l'équation de Schrödinger est appelée équation de cheminement)). Si bien que l'énergie cinétique n'est pas du tout négligeable, puisqu'égale à 50% de l'énergie potentielle en module.
Remarque : Kleinert, élève de Feynman, a réussi à donner l'interprétation du « cheminement » dans le cas de l'atome d'hydrogène, mais cela reste une prouesse. En ce sens , pour les chimistes, le seul vrai progrès notable depuis Hartree-Fock et Clementi a été (pour l'atome à N électrons), la notion de densité fonctionnelle de Kohn (Nobel de chimie 1998).
Conclusion
Il faut garder en mémoire toujours ces deux aspects, le couple [Ψ(r),Φ(p)], pour bien comprendre l'aspect non statique, mais stationnaire de cette délocalisation de l'électronde. Beaucoup de livres proposent comme règle empirique : si l'électronde est localisé dans une région de l'ordre de r = a, lui donner une énergie cinétique de l'ordre de
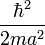 . Dans le cas présent, cela, donne une énergie totale
. Dans le cas présent, cela, donne une énergie totale 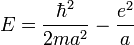 dont le minimum est bien
dont le minimum est bien 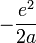 , où a est le rayon de Bohr :
, où a est le rayon de Bohr :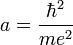 .
.
C'est une façon simple et élégante d'introduire les OdG ( ordre de grandeur)de l'atome, souvent reprise dans les bons ouvrages.
Orbitales
Résonance acoustique
Nous allons obtenir la structure de l'atome d'hydrogène en dénombrant les modes de vibration de la sphère. Le mode de vibration fondamental, dont la fréquence est la plus élevée, est toujours sphérique. Lorsque la vitesse des ondes est constante, il correspond à une longueur d'onde égale à deux fois le diamètre, comme pour une corde vibrante où le fondamental a une longueur d'onde double de la longueur de la corde lorsqu'elle est encastrée ou libre à chacune de ses extrémités.
Dans un cube, les résonances apparaissent lorsque les demi-longueurs d'onde sont des fractions entières du côté du cube avec un ventre au centre du cube. Le premier harmonique du cube présente un nœud au milieu, comme pour la corde vibrante. Son nombre quantique principal est n=2. Il y a trois façons de le placer, selon les trois directions de l'espace, ce qui donne trois modes de vibration de même énergie, autrement dit dégénérés. Il peut aussi y avoir un noeud au centre du cube. Il y a donc 4 possibilités.
Résonance de l'atome
Il en est de même pour la sphère qui aura un nœud au centre soit un nombre quantique secondaire l=1. Comme pour le cube, il y a trois façons de le placer, selon les trois directions de l'espace, ce qui donne trois modes de vibration de même énergie, autrement dit dégénérés. Il peut aussi y avoir un noeud de symétrie sphérique, en son centre. Il y a donc 4 possibilités comme pour le cube.
Lorsqu'on augmente la fréquence de vibration, c'est-à-dire l'énergie de vibration, le nombre de nœuds augmente d'une unité à chaque fois. On obtient ainsi les harmoniques successifs qui ne sont généralement pas des harmoniques au sens musical du terme. Les harmoniques, au sens mathématique, du tambour, par exemple, ne sont pas des harmoniques au sens musical car ils ne sont pas des multiples entiers du fondamental. Il en est de même dans l'atome.
Dans l'atome d'hydrogène où la vitesse des ondes de de Broglie est fonction du potentiel électrostatique du noyau, le mode fondamental correspond au nombre quantique principal n=1. La théorie de Schrödinger fait apparaître deux nombres quantiques supplémentaires, le nombre quantique secondaire l et le nombre quantique magnétique m, nuls pour le mode fondamental n=1.
On n'utilise pas les coordonnées cartésiennes pour la sphère, mais la colatitude θ et la longitude
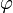 . On peut se passer de la variable r grâce à Bohr car la théorie de Schrödinger prévoit les mêmes niveaux d'énergie. L'axe principal est vertical, celui pour lequel θ = 0. Pour le premier harmonique, n = 2, on a trois orientations possibles pour le nœud, un nœud selon l'équateur, les deux autres des méridiens. On pourrait prendre des méridiens perpendiculaires, mais il revient au même de n'en prendre qu'un seul et de le faire tourner dans un sens ou dans l'autre, ce qui correspond au nombre quantique magnétique m = ± 1. On fait donc varier m entre - 1 et + 1.
. On peut se passer de la variable r grâce à Bohr car la théorie de Schrödinger prévoit les mêmes niveaux d'énergie. L'axe principal est vertical, celui pour lequel θ = 0. Pour le premier harmonique, n = 2, on a trois orientations possibles pour le nœud, un nœud selon l'équateur, les deux autres des méridiens. On pourrait prendre des méridiens perpendiculaires, mais il revient au même de n'en prendre qu'un seul et de le faire tourner dans un sens ou dans l'autre, ce qui correspond au nombre quantique magnétique m = ± 1. On fait donc varier m entre - 1 et + 1.En résumé, le nombre quantique principal n donne le nombre de nœuds. Le nombre quantique secondaire l < n donne le nombre de configurations possibles pour les nœuds et m les numérote de - (l - 1) à l - 1.
Les orbitales sont d'abord représentées de façon simplifiée avec les nœuds des harmoniques sphériques sans les ventres (les « larmes »). La représentation est polaire, comme la Terre, en coordonnées sphériques. On donne ensuite une représentation sous forme de « larmes » puis un tableau récapitulatif. Il y a deux fois plus d'états quantiques que de modes de vibration en vertu du principe d'exclusion de Pauli.
Couche K
1 orbitale sphérique (1s)
C'est l'état fondamental, de symétrie sphérique 1s, un nœud de vibration sphérique, qu'on peut placer soit sur la périphérie, à l'infini, soit sur le noyau. Les nombres quantiques correspondants sont :
Il n'y a qu'un mode de vibration car les valeurs m = + 0 = m = - 0. En vertu du principe d'exclusion de Pauli, la couche K n'a qu'une seule orbitale et ne peut contenir que deux électrons au maximum. Avec un électron, on a l'hydrogène. Avec deux, on a l'hélium.
Couche L
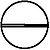
1 orbitale sphérique (2s)
Elle comprend une orbitale sphérique 2s, soit un nœud de vibration sphérique et deux états quantiques, donc deux éléments (Li et Be) :
3 orbitales (2p)
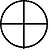
Une orbitale de symétrie de révolution et deux autres avec un méridien, de symétrie axiale. Le méridien pouvant tourner dans un sens ou dans l'autre,il y a deux valeurs du nombre quantique magnétique m :
En additionnant les orbitales des couches K et L, on a 5 orbitales soit, en vertu du principe de Pauli, 10 électrons et un numéro atomique N=10 correspondant au néon. Cela permet non seulement de comprendre l'atome d'hydrogène mais aussi de construire la table de Mendeleiev.
Couche M
1 orbitale (3s) sphérique
3 orbitales (3p)
Comme pour la couche L sauf qu'il y a un nœud sphérique en plus.
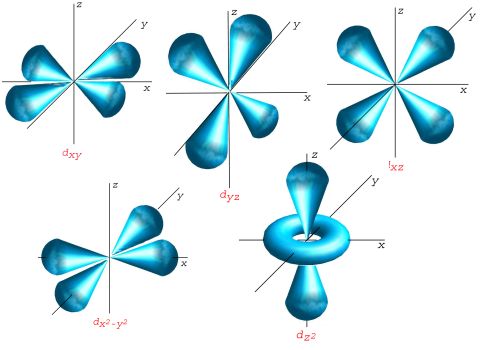
5 orbitales (3d)
Les orbitales m ≠ 0 sont doubles.
On peut aussi représenter les orbitales d de la couche M, en larmes d'eau :
Pour plus de détails voir harmoniques sphériques. On remarquera l'anneau sur l'orbitale
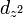 de révolution qu'on retrouve sur les atomes hydrogénoïdes ou atome de Rydberg.
de révolution qu'on retrouve sur les atomes hydrogénoïdes ou atome de Rydberg.Récapitulatif des couches K, L, M
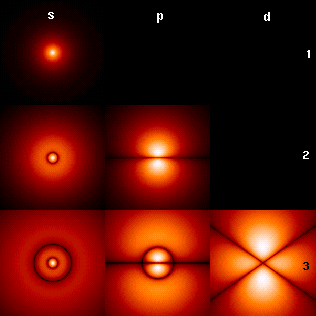
Cette figure résume les modes de vibration qu'on rencontre dans les trois couches K, L, M. Chaque couche reprend la couche précédente avec un nœud de plus.
Les orbitales de gauche, sphériques, sont simples. Les orbitales p sont triples avec un nœud plan et les orbitales d quintuples avec deux nœuds plans.
Chaque couche contient les couches inférieures, par exemple en-dessous de la sous-couche 3p, on a les sous-couches 1s,2s,2p et 3s. D'après le principe d'exclusion de Pauli, le nombre maximal d'électrons dans une sous-couche doit être pair. Considérons le cas du sodium Na. Toutes les couches seront remplies jusqu'à la sous-couche 3s avec un électron célibataire. Sa structure électronique s'écrit 1s22s22p63s1 ou [Ne]s1, ce qui fait un total de Z = 11 électrons, numéro atomique du sodium Na qui suit immédiatement Ne. On marie l'électron célibataire du sodium pour obtenir le magnésium. On remplit la couche 3p avec six électrons pour obtenir l'argon Ar. Tous les gaz rares ont une sous-couche externe de type p sauf l'hélium avec une sous-couche s.
Au-delà de l'argon, il y a une anomalie due à la répulsion électrostatique entre les électrons : le mode 4s se met à la place de 3d. Le modèle de l'atome d'hydrogène ne s'applique donc que jusqu'à l'argon. Au-delà, l'ordre des sous-couches diffère de celui prévu par le modèle de la cavité sphérique comme de celui de Schrödinger. Pour prévoir l'ordre réel on a des règles empiriques (Aufbau, Hund, Klechkowski ou Madelung). Connaissant ces anomalies, on peut construire la Table périodique des éléments ou [1]
Notes et références
- ↑ par l'intermédiaire de l'atome de Bohr
- ↑ Élément avec seulement deux électrons
- ↑ c. f. atome de Bohr
- ↑ Feynman, R, Le Cours de physique de Feynman, tome 3 : Mécanique quantique, Dunod, 2003
Voir aussi
Articles connexes
- Atome
- Atome de Bohr
- Saturation des inégalités d'Heisenberg
- Théorie de Schrödinger de l'atome d'hydrogène
- Orbitale atomique
- Orbitale de l'atome d'hydrogène
- Harmoniques sphériques
- Théorie de Pauli de l'atome d'hydrogène
- Atome à N électrons
- Classification périodique
- Dihydrogène
- Raie à 21 centimètres
- (en) Quantum mechanics
Bibliographie
- E. Hansch, A. Schawlaw & G. Series ; Le spectre de l'hydrogène atomique, Pour La Science 19 (Mai 1979) 46.
- J. L. Basdevant, J. Dalibard, Mécanique quantique [détail des éditions]
- C. Cohen-Tannoudji, B. Diu et F. Laloë, Mécanique quantique [détail des éditions]
- Albert Messiah, Mécanique quantique [détail des éditions]
- S.G. Karshenboim et al. (éditeurs) ; The hydrogen atom - Precision physics of simple atomic systems, Lecture Notes in Physics 570, Springer-Verlag (2001). Recueil d'articles de revue sur l' état de l'art en spectroscopie atomique, mesures de fréquences, et mesures de constantes fondamentales. Niveau troisième cycle universitaire.
- Victor Guillemin & Shlomo Sternberg ; Variations on a Theme by Kepler, Providence RI, American Mathematical Society (1990), ASIN 0821810421. Très beau livre.
- Bruno Cordani ; The Kepler Problem - Group Theoretical Aspects, Regularization and Quantization, with Application to the Study of Perturbations, Progress in Mathematical Physics 29, Birkhäuser (2003), ISBN 3-7643-6902-7.
- Stephanie F. Singer, Linear Symmetry and Predictions in Hydrogen Atom, Undergraduate Text in Mathematics, Springer-Verlag (2005), ISBN 0387246371 . De niveau plus simple, mais très moderne et beaucoup de références web.
- Portail de la physique
Catégories : Article à recycler (physique) | Article à désacadémiser | Atome | Hydrogène
Wikimedia Foundation. 2010.

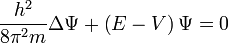
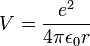
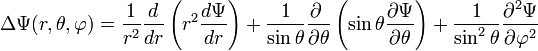
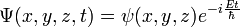

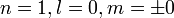
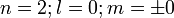
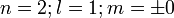

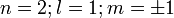
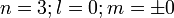
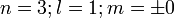
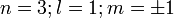
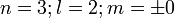 (
( 
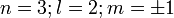 (trèfle à quatre lobes
(trèfle à quatre lobes 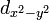 )
)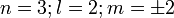 (trèfle à quatre lobes
(trèfle à quatre lobes