- 137-05-3
-
Cyanoacrylate
2-cyanoacrylate de méthyle 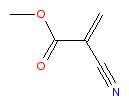
Monomère du cyanoacrylate, le 2-cyanoacrylate de méthyle Général Synonymes Mecrylate No CAS No EINECS SMILES InChI Apparence liquide incolore.[1] Propriétés chimiques Formule brute C5H5NO2 [Isomères] Masse molaire 111,0987 g∙mol-1
C 54,05 %, H 4,54 %, N 12,61 %, O 28,8 %,Propriétés physiques T° fusion -40 °C[1] T° ébullition 66 °C[1] Masse volumique (eau = 1) : 1.1[1] Point d’éclair 79 °C[1] Pression de vapeur saturante à 25 °C : 24 Pa[1] Précautions Directive 67/548/EEC 
XiPhrases R : 36/37/38, Phrases S : (2), 23, 24/25, 26, SIMDUT[2] 
SGH[3] 
AttentionUnités du SI & CNTP, sauf indication contraire. Le cyanoacrylate est le nom communément utilisé pour dénommer le 2-cyanoacrylate de méthyle, une substance adhésive très puissante habituellement vendue sous la marque déposée Superglue et Krazy Glue.
Sommaire
Histoire
Le Cyanoacrylate a été découvert durant la Seconde Guerre mondiale en cherchant un moyen de remplacer la soie d'araignée dans la fabrication des réticules de lunettes de visée. Il n'a pas résolu le problème, car il collait à tous les équipements utilisés pour le manipuler. Plus tard, il fut développé en une forme plus utile par la compagnie Eastman Kodak en 1958. Le terme est maintenant utilisé pour désigner une vaste gamme d'adhésifs basé sur un composant chimique similaire.
Propriétés
Dans sa forme liquide, le cyanoacrylate consiste en des monomères de molécules de cyanoacrylates, CH2=C(CN)COOCH3 (Formule brute : C5H5NO2), et a un poids moléculaire de 111,1 g/mol. Son point d'éclair se situe à 79 ºC et sa densité est 1,1 par rapport à l'eau (H2O).
C'est une résine acrylique qui polymérise rapidement en présence d'anions (la polymérisation démarre avec un amorceur anionique, tel que l'hydroxyde, les amines, les alcools, ...). Dans ce cas précis de polymérisation anionique, l'eau suffit à amorcer la polymérisation, l'intermédiaire réactionnel étant stabilisé par la présence du groupement carbonyle et du groupement cyano en alpha du carbanion. Lors de la polymérisation, il y a formation de longues et solides chaînes, joignant les surfaces à coller.
Un autre trait important est que le cyanoacrylate colle rapidement, souvent en moins d'une minute, face a un collage normal qui obtient sa solidité maximale en deux heures ; et est résistant à l'eau. Des accélérants permettent d'obtenir le collage en 2 ou 3 secondes, au prix d'une perte de solidité. Deux centimètres carrés de surface de collage supportent aisément le poids d'une masse supérieure à une tonne.
L'acétone (que l'on retrouve dans le dissolvant pour vernis à ongles), est un solvant facilement disponible, capable de ramollir le cyanoacrylate polymérisé.
Utilisation
Le Cyanoacrylate est un adhésif tenace, particulièrement lorsqu'il est utilisé pour coller des matériaux non poreux. Ainsi il est très efficace pour coller les tissus corporels, et tandis que cet effet peut être une nuisance, (ou même dangereux), il a été exploité pour bénéficier de chirurgie sans sutures. Son produit secondaire de polymérisation, l'acide acétique, est biocompatible. Le cyanoacrylate est utilisé dans la chirurgie orthopédique pour coller les objets métalliques aux os. Par exemple, rotules artificielles aux fémurs.
Les cyanoacrylates sont utilisés en criminalistique pour la détection des empreintes digitales. La colle liquide est vaporisée et la vapeur passée sur les objets suspectés de posséder des empreintes digitales. Les traces d'eau infimes causent la polymérisation de la vapeur, qui, durcie, forme une version solide de l'empreinte, qui est rendue bien plus visible et robuste.
Les cyanoacrylates sont souvent utilisés pour assembler des prototypes de circuit électroniques (voir wire wrap) (câblage), modèles réduits, bloquer des boulons ou écrous en mécanique.
En bricolage il et destiné au collage du verre et aux réparations de petites surfaces. Elle possède 2 composants, 2 liquides parfaitement incolore: la résine et l'activateur ne demandant pas de mélange. Elle a une bonne résistance à l'humidité et à la chaleur.
Il existe des colles cyanoacrylates pour les matériaux poreux, ainsi qu'une version destinée aux métaux possédant uen résistance aux chocs.
Application pour le bricolage
- Appliquer une couche d'activateur sur une face de la cassure
- Laisser sécher environ une minute
- Appliquer ensuite une couche de résine sur l'autre face
- Mettre en contact les deux parties, attention la prise de colle est immédiate
- Presser fortement pendant une minute
- Enlever les bavures immédiatement avec un chiffon imbibé d'alcool à 90°
- Laisser sécher une demi-heure sans y toucher
Sécurité
Attention à la manipulation de ce produit: une goutte serrée entre ses doigts les collerait l'un sur l'autre et une intervention chirurgicale risquerait d'être nécessaire.
Il est possible de les décoller sous eau du robinet, à la chaleur maximale.
Conservation
Après usage, conserver le produit dans un endroit frais et sec et à l'abri de la lumière ( raison pour laquelle, ils sont déconseillé pour recoller le verre)
Synonyme
- alpha-cyanoacrylate de méthyle
- MCA
- Mécrylate
- Mécrilate
- Loctite
- Ergo Kisling
Voir aussi
Références
- ↑ a , b , c , d , e et f 2 - CYANOACRYLATE DE METHYLE, fiche de sécurité du Programme International sur la Sécurité des Substances Chimiques, consultée le 9 mai 2009
- ↑ « Cyano-2 acrylate de méthyle » dans la base de données de produits chimiques Reptox de la CSST (organisme canadien responsable de la sécurité et de la santé au travail), consulté le 25 avril 2009
- ↑ Numéro index dans le tableau 3.1 de l'annexe VI du règlement CE N° 1272/2008 (16 décembre 2008)
- Portail de la chimie
Catégories : Produit chimique irritant | Polymère | Adhésif | Nitrile
Wikimedia Foundation. 2010.

