- 521-31-3
-
Luminol
Luminol 
Général Nom IUPAC 5-Amino-2,3-dihydro-1,4-phthalazinedione Synonymes o-Aminophthaloyl hydrazide
3-Aminophthalhydrazide[1]No CAS No EINECS PubChem Apparence cristaux brillants,
jaune verdâtrePropriétés chimiques Formule brute C8H7N3O2 [Isomères] Masse molaire 177,1601 g∙mol-1
C 54,24 %, H 3,98 %, N 23,72 %, O 18,06 %,Propriétés physiques T° fusion 319 à 320 °C Solubilité Soluble dans l'éthanol
et l'acétone.
Insoluble dans l'eauPrécautions Directive 67/548/EEC 
XnPhrases R : 22, 36/37/38, Phrases S : 26, 37/39, Écotoxicologie DL50 rats, peroral 500 mg/kg Unités du SI & CNTP, sauf indication contraire. Le luminol est un produit chimique présentant une chimiluminescence, avec un éclat bleu caractéristique, lorsqu'il est mélangé avec un oxydant adéquat. Il s'agit d'un solide cristallin, blanc à légèrement jaune qui est soluble dans la plupart des solvants organiques polaires, mais insoluble dans l'eau.
Le luminol est utilisé en criminalistique pour détecter les faibles traces de sang laissées sur les scènes de crime. Il est également utilisé par les biologistes pour détecter le cuivre, le fer et le cyanure.
Sommaire
Histoire
Bien que le luminol soit connu depuis 1902, ce n'est qu'en 1913 qu'a été découvert sa chimiluminescence. Curtuis et Semper, deux scientifiques, l'ont découvert par hasard après l'avoir dissout dans de l'hydroxyde de sodium et ensuite oxydé avec du péroxyde d'hydrogène ou de l'hypochlorite de sodium, le mélange a alors émit une forte lumière verte plus intense que n'importe quelle autre réaction chimique connue[2].
Le luminol a été synthétisé pour la première fois en 1934[3] pour démontrer la chimiluminescence.
Le luminol a ensuite été utilisé comme agent de test pour observer l'apparition de peroxyde d'hydrogène lors d'une réaction[4].
Chimie
Synthèse
Le luminol peut être synthétisé à partir de l'acide 3-nitrophtalique. De l'hydrazine (N2H4) est d'abord chauffée avec l'acide 3-nitrophtalique dans un solvant à haut point d'ébullition tel que le triéthylène glycol. Une réaction de condensation avec perte d'eau se produit, formant du 3-nitrophtalhydrazide[5]. La réduction du groupe nitrate en un groupe amine avec du dithionite de sodium (Na2S2O4) produit du luminol[6].
Chimiluminescence
Un oxydant est nécessaire afin de provoquer la luminescence du luminol. Habituellement, une solution de péroxyde d'hydrogène (H2O2) et un sel hydroxyde aqueux est utilisé comme activateur. En présence d'un catalyseur - comme un composé ferreux – le péroxyde d'hydrogène est décomposé en eau et en dioxygène :
2H2O2→O2+2H2O
Dans le cadre d'un laboratoire, le catalyseur utilisé est souvent du ferricyanide de potassium. Pour la détection criminologique de sang, le catalyseur est le fer présent dans l'hémoglobine. Les enzymes de beaucoup de systèmes biologiques sont également susceptibles de catalyser la décomposition de péroxyde d'hydrogène.
Lorsque le luminol réagit avec le sel hydroxyde, un dianion se forme. L'oxygène issu de la décomposition du peroxyde d'hydrogène réagit alors avec ce dianion. Le produit de cette réaction, un peroxyde organique, est très instable et se décompose immédiatement avec une perte d'azote pour produire de l'acide 3-aminophtalique possédant des électrons dans un état excité. La désexcitation des électrons provoque l'émission d'énergie sous forme d'un photon de lumière bleue visible.
Utilisation en criminalistique
 Sang mélangé à du luminol
Sang mélangé à du luminol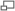
Théorie
Le luminol est utilisé par la police scientifique pour repérer les traces de sang même si celles-ci ont été nettoyées. L'enquêteur prépare une solution de luminol et d'activateur et la pulvérise sur toute la surface du lieu des investigations. Le fer présent dans le sang va alors catalyser la réaction chimique qui provoque la luminescence, révélant l'emplacement du sang. La quantité de catalyseur nécessaire à la réaction est très faible par rapport à la quantité de luminol, ce qui permet la détection de quantités de sang infinitésimales. L'éclat est bleu et dure environ 30 secondes. La pièce doit être assez sombre afin de détecter celui-ci. Toute émission de lumière doit être archivée par une photographie à temps de pose élevé.
Inconvénients
Le luminol possède des inconvénients pouvant limiter son utilisation dans les enquêtes criminelles :
- le luminol réagit en présence de cuivre ou d'un alliage de cuivre, de raifort, et de certains décolorants. Ainsi, si une scène de crime est patiemment nettoyée à l'aide d'une solution diluée d'eau de Javel, celle-ci va devenir entièrement fluorescente, camouflant les éventuelles traces organiques comme le sang ;
- le luminol va également détecter les petites quantités de sang présentes dans l'urine et il peut également réagir si du sang animal était présent dans une pièce testée ;
- le luminol réagit aux matières fécales, produisant le même éclat que s'il s'agissait de sang ;
- la présence de luminol peut empêcher de pratiquer d'autres tests. Cependant, il a été montré que l'ADN peut être extrait avec succès d'échantillons traités avec du luminol[7];
- le luminol est depuis longtemps réputé cancérigène, bien que la preuve n'en ait pas encore été apportée (des études ont infirmé ce postulat).
Autres utilisations
- Médicale : Utilisé pour procéder à des (essais / tests ?) biochimiques
- Éducation : Permettre aux jeunes de s'intéresser aux sciences
- Loisir et sécurité : Enfermé dans des baguettes que l'on craque en pliant pour mélanger les réactifs. Les bâtonnets lumineux servent lors d'une fête (décoration) ou pour une signalisation de sécurité (évacuation, accident) ou en milieu aquatique (plongée).
Notes et références de l'article
- ↑ (en) Luminol RN: 521-31-3 Base de donné NLM ChemIDplus
- ↑ (en) R.E.D Clark, “Chemiluminescence”, School Sci. Rev., 1937/38, 19, 489.
- ↑ (en) EH Huntress, LN Stanley and AS Parker (1934), The preparation of 3-aminophthalhydrazide for use in the demonstration of chemiluminescence, J. Am. Chem. Soc., 56, 241.
- ↑ (en) HH Roetorfer and MJ Cornier (1957). Formation of “hydrogen peroxide” in the reaction of oxyhemoglobin with methemoglobin forming agents. Arch. Biochem. 71: 235, 1957.
- ↑ (en) 5-NITRO-2,3-DIHYDRO-1,4-PHTHALAZINEDIONE Organic Syntheses, Coll. Vol. 3, p.656 (1955); Vol. 29, p.78 (1949).
- ↑ (en) 5-AMINO-2,3-DIHYDRO-1,4-PHTHALAZINEDIONE Organic Syntheses, Coll. Vol. 3, p.69 (1955); Vol. 29, p.8 (1949).
- ↑ P. de Brem (2007) Police scientifique : des recherches tous azimuts - 02/ Biologie : faire parler le sang. Banques des savoirs. Lundi 8 octobre 2007.
Voir aussi
Articles connexes
Liens externes
- Portail de la chimie
Catégories : Produit chimique nocif | Médecine légale | Hydrazine | Aminobenzène | Amide | Test chimique
Wikimedia Foundation. 2010.


