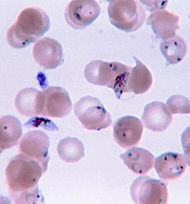
- Paludisme
-
Classifications CIM du Paludisme
Classification et ressources externesFrottis sanguin révélant la présence du parasite Plasmodium falciparum ayant la forme d'anneaux à l'intérieur d'hématies humaines. CIM-10 B50. CIM-9 084 OMIM 248310 DiseasesDB 7728 MedlinePlus 000621 eMedicine med/1385 emerg/305ped/1357 MeSH C03.752.250.552  Un Anopheles gambiae (une des espèces d'anophèles, hôtes définitifs du parasite responsable du paludisme).
Un Anopheles gambiae (une des espèces d'anophèles, hôtes définitifs du parasite responsable du paludisme).
Le paludisme (du latin paludis, « marais »[1]), aussi appelé malaria (de l'italien mal'aria, « mauvais air »[2], terme privilégié par les Anglo-saxons), est une maladie infectieuse due à un parasite du genre Plasmodium, propagée par la piqûre de certaines espèces de moustiques anophèles.
Avec 225 millions de personnes malades et 781 000 décès en 2009[3], le paludisme demeure la parasitose la plus importante et concerne majoritairement les enfants de moins de cinq ans et les femmes enceintes. 80 % des cas sont enregistrés en Afrique subsaharienne (cf. section détaillée : « Épidémiologie »).
Le parasite du paludisme est principalement transmis lors de la piqûre par une femelle moustique du genre Anopheles, elle-même contaminée après avoir piqué un animal homéotherme impaludé. Le parasite infecte les cellules hépatiques de la victime puis circule dans le sang, en colonisant les hématies et en les détruisant. Cinq espèces de Plasmodium sont impliquées en pathologie humaine. La forme la plus grave du paludisme est causée par Plasmodium falciparum, responsable d'une grande majorité des décès. Plasmodium vivax, Plasmodium ovale, Plasmodium malariae et Plasmodium knowlesi provoquent des formes de paludisme « bénignes » qui ne sont généralement pas mortelles (cf. section détaillée : « Causes »).
La cause de la maladie a été découverte le 6 novembre 1880 à l'hôpital militaire de Constantine (Algérie) par un médecin de l'armée française, Alphonse Laveran, qui reçut le prix Nobel de physiologie ou médecine en 1907. C'est en 1897 que le médecin anglais Ronald Ross (prix Nobel en 1902) prouva que les moustiques anophèles étaient les vecteurs de la malaria (jusqu'à cette date, le mauvais air émanant des marécages était tenu responsable de la propagation de la maladie).
Histoire
Depuis les origines de l'Homme
 Artemisia annua (Armoise annuelle), utilisée en Chine depuis plus de 2 000 ans pour soulager les fièvres.
Artemisia annua (Armoise annuelle), utilisée en Chine depuis plus de 2 000 ans pour soulager les fièvres.
Le paludisme affecte les êtres humains depuis plus de 50 000 ans et aurait été un pathogène depuis le début de l'histoire de notre espèce[4]. On trouve ainsi des parasites proches de celui de la malaria chez les chimpanzés, l'espèce la plus proche de l'Humain [5]. Les chimpanzés abritent un parasite du paludisme, le Plasmodium reichenowi, proche parent du Plasmodium falciparum ; les gorilles abritent quant à eux le Plasmodium falciparum qui pourrait être à l'origine du parasite humain (le séquençage de l'ADN du Plasmodium falciparum dans des féces de gorille infecté montre par analyse phylogénétique que ce parasite primatophile serait l'ancêtre de la souche qu'on retrouve chez l'homme)[6]. Il y a environ 10 000 ans, le paludisme commence à avoir un impact majeur sur la survie humaine, ce qui coïncide avec le début de l'agriculture (révolution néolithique) donc à la sédentarisation. Une des conséquences (impact + modification du mode de vie) en est la sélection naturelle des gènes de la drépanocytose, des thalassémies, du déficit en glucose-6-phosphate déshydrogénase, de l'elliptocytose héréditaire (appelée dans certains cas ovalocytose). Ces maladies qui touchent les globules rouges du sang, donnent un avantage sélectif envers le paludisme (cf. section détaillée : « Les facteurs génétiques »).
Des fièvres mortelles - dont probablement le paludisme - ont été rapportées depuis les premiers écrits. On trouve ainsi des références à des périodes de fièvre paludique dès 2 700 avant J.-C. en Chine[7]. Le plus ancien écrit concernant les infections dues à un parasite est le papyrus Ebers rédigé à Louxor en 1 500 avant J.-C. ; la découverte dans les momies de cette époque d'œufs calcifiés d'helminthes confirme le bien fondé des observations[7]. En janvier 2010, une équipe de scientifiques égyptiens et américains ont prouvé, par l'analyse de l'ADN, que Toutânkhamon était atteint de paludisme au moment de son décès (v. -1327)[8],[9]. En Inde, dès l'antiquité, les Veda (« Textes de la connaissance ») font état des fièvres paludiques et les médecins Charaka et Sushruta (probablement Ve siècle av. J.‑C.) en font une description et lui associent, déjà, la piqûre de moustique. Les symptômes de fièvre intermittente ont été décrits par Hippocrate; il lie ces fièvres à certaines conditions climatiques et environnementales, et les divise en trois types : febris tertiana (tous les deux jours), quartana (tous les trois jours), et quotidiana ou continua (maintenant appelée tropica). Vers 186 avant J.-C. apparaît, dans certaines régions de Chine, l'utilisation, en tisane, du qing hao su (青蒿素) appelé plus tard artémisinine en Occident et extrait d'une plante médicinale utilisée comme antipyrétique appelée qing hao (青蒿) (Artemisia annua ou « Armoise annuelle »).
Le paludisme était commun dans des endroits du monde où il est inconnu maintenant, comme en Europe et en Amérique du Nord. Dans certains endroits d'Angleterre, la mortalité due à la malaria était comparable à celle de l'Afrique subsaharienne d'aujourd'hui. Même si William Shakespeare est né au début d'une période plus froide appelée le « petit âge glaciaire », il connaissait suffisamment les ravages de cette maladie pour les citer dans huit de ses pièces. En France métropolitaine, la malaria n'a disparu que relativement récemment. Elle était encore présente en 1931, dans le marais poitevin, le golfe du Morbihan et en Camargue. Elle a été éradiquée de Corse, en 1973. Inconnu du temps de la présence romaine, le paludisme fut introduit lors des raids vandales. L'île connaîtra sa dernière épidémie de cas non importés à Plasmodium vivax de 1970 à 1973. Fait notable, en 2006 est survenu un cas autochtone à Plasmodium vivax sur l'île. Depuis, la quasi totalité des cas observés en France sont des paludismes d'importation. Plasmodium vivax a sévi jusqu'en 1958 dans les zones de Polder de Belgique et des Pays-Bas.
Dans les années 1500, ce sont les colons européens et leurs esclaves qui ont probablement amené le paludisme sur le continent américain (on sait que Christophe Colomb était atteint de cette maladie avant son arrivée dans les terres nouvelles). Les jésuites missionnaires espagnols virent que les Indiens riverains du lac de Loxa au Pérou utilisaient de la poudre d'écorce de Cinchona pour soigner les fièvres. Cependant, on ne trouve aucune référence au paludisme dans les ouvrages médicaux des Maya ou des Aztèques. L'utilisation de l'écorce de « l'arbre à fièvre » a été introduite dans la médecine européenne par les missionnaires jésuites dont Barbabe de Cobo qui l'expérimente en 1632 et l'exporte également; si bien que la précieuse poudre s'appela également « poudre des jésuites »[10].
Les facteurs critiques affectant la propagation ou l'éradication de la maladie ont été les comportements humains (déplacements de population, méthodes d'agriculture, etc.), le niveau de vie (la pauvreté était et reste la principale cause de mortalité) et la densité de la population (plus la densité humaine est grande et plus la densité de moustiques sera grande).
XVIIIe et XIXe siècles : premières études scientifiques
En 1717, la pigmentation post-mortem au graphite de la rate et du cerveau est publiée par Giovanni Maria Lancisi, le médecin du pape Clément XI, dans un ouvrage, édité en 1717, sur le paludisme De noxiis paludum effluviis eorumque remediis. Il y présente des preuves que la maladie est transmise par les mouches. Lancisi introduit le mot mal'aria, « mauvais air ».
En 1820, Pierre Joseph Pelletier et Joseph Bienaimé Caventou séparent les alcaloïdes cinchonine et quinine de la poudre de l'écorce de « l'arbre à fièvre », permettant la création de doses standardisées des composants actifs[11].
En 1848, Johann Friedrich Meckel von Helmsbach (surnommé Meckel le jeune) note un grand nombre de granules noir-bruns dans le sang et la rate d'un patient qui venait de mourir dans un hôpital psychiatrique. Meckel était probablement en train de voir des parasites de malaria sans le comprendre, car il ne mentionne pas le paludisme dans son rapport, en pensant que le pigment était de la mélanine.
En 1856, lors des essais, sans succès, pour synthétiser la quinine de façon commercialement viable, William Henry Perkin produit de la mauvéine par l'oxydation de l'o-toluidine. Avant cette découverte, les colorants et les peintures étaient issus de racines, de feuilles, d'insectes ou, dans le cas du pourpre, de mollusques. La découverte de Perkin des colorants artificiels permit de grandes avancées dans le domaine de médecine, de la photographie et d'autres domaines.
En 1865, Charles Ledger et un indien nommé Manuel font littéralement le trafic des graines de quinquina (Cinchona calisaya aussi appelé Cinchona Ledgeriana) en provenance de l'Équateur, du Pérou et de Bolivie. Des plantations sont alors établies sur l'île de Java par les Hollandais, après avoir acheté des graines aux Anglais, qui établissent, ainsi, un monopole mondial sur la quinine.
 Plaque commémorative à Strasbourg
Plaque commémorative à Strasbourg
En 1880, Charles Louis Alphonse Laveran établit, en Algérie, la relation entre les observations faites par Meckel "le jeune" et le parasite qu'il observe pour la première fois dans les globules rouges de 44 personnes souffrant du paludisme. En voyant l'exflagellation se produire, il devient convaincu que les flagelles mobiles sont des micro-organismes parasites (minuscules êtres vivants unicellulaires qui se multiplient végétativement par mitose). Or bien des médecins de l'époque pensaient encore que les protozoaires n'étaient en fait que des globules rouges altérés. Laveran devra se battre pour faire admettre sa théorie car restait à trouver comment ces organismes s'introduisaient dans le corps humain. N'ayant pas obtenu un poste lui permettant de poursuivre ses recherches, Laveran prend sa retraite et poursuit ses recherches sur les protozoaires à l'Institut Pasteur en tant que bénévole. C'est en 1898 qu'il va publier son Traité du paludisme. Il voit aussi l'effet de la quinine, qui détruit ces parasites. Il suggère que le paludisme est causé par ce protozoaire. C'est la première fois qu'un protozoaire est identifié comme étant la cause d'une maladie[12]. Cette découverte lui vaut l'attribution du prix Nobel de médecine en 1907. Les études scientifiques sur le paludisme viennent de faire leur première avancée significative.
En 1880, Ettore Marchiafava et Angelo Celli, à la demande d'Alphonse Laveran, étudient, au microscope, le cycle de reproduction du protozoaire dans le sang humain et observent qu'ils se divisent à peu près simultanément à intervalles réguliers et que la division coïncide avec les attaques de fièvre. En 1885, ils appellent ce protozoaire Plasmodium[13].
En 1881, Carlos Finlay, un médecin cubain qui traite les patients atteints de la fièvre jaune à La Havane, affirme que ce sont les moustiques qui transmettent cette maladie aux humains.
En 1884 le Dr Patrick Manson émet le premier l'hypothèse qu'il doit s'agir d'un moustique qui absorbe le parasite et pond dans l'eau que l'homme ingurgite.
En 1886 et 1892, Camillo Golgi publie ses découvertes sur la fréquence et la périodicité des fièvres dues à la malaria et montre qu'il existe plusieurs types de paludisme causés par des organismes protozoaires différents..
En 1891, Paul Ehrlich remarquent que le bleu de méthylène a une grande affinité pour certaines cellules et que ce colorant a de faibles propriétés antipaludéennes. Ehrlich veut promouvoir le développement de médicaments en exploitant les différences biochimiques.
En 1895, l'expédition française de Madagascar fut un « désastre sanitaire » : sur 21 600 hommes débarqués, 5 731 sont morts du paludisme et 25 sont morts au combat[14]. À noter que ce genre de « désastre » se reproduira souvent comme pendant la guerre du Vietnam pour les soldats Nord-vietnamiens (voir l'article sur l'artémisinine).
En 1898, Amico Bignami réussit à transmettre expérimentalement le paludisme grâce à des moustiques. Il n’hésite pas à se faire piquer lui-même et à contracter la maladie.
 Ronald Ross, prix Nobel de médecine 1902.
Ronald Ross, prix Nobel de médecine 1902.
En 1898, c'est le Britannique Ronald Ross, travaillant en Inde et correspondant régulièrement avec Laveran et Manson mais qui a du mal à imaginer pourquoi l'insecte ne transmet pas directement le parasite par piqûre, qui prouvera finalement que le paludisme est transmis par cette piqûre. Pour confirmer sa théorie, il dissèquera pendant deux ans des oiseaux paludéens qu'il faisait piquer par des centaines de variétés de moustiques et ce n'est qu'après ces deux ans, au bord du découragement, qu'il remarque une espèce de moustique qui ne se développe que dans les eaux de surface et ne se voit que la nuit : l'anophèle. Il continue alors ses recherches, il récolte et élève les larves et retrouve des protozoaires de Laveran vers le septième jour dans l'estomac de l'anophèle. La preuve est établie, c'est bien cet insecte qui transmet le parasite vivant à ses dépens. Il constate qu'une période d'incubation de 10 à 14 jours est nécessaire entre la piqûre et l'apparition des parasites dans le sang. Il venait de prouver que certaines espèces de moustiques transmettent le paludisme aux oiseaux, en isolant les parasites des glandes salivaires des moustiques qui se nourrissent des oiseaux affectés[15]. Ceci lui vaut le prix Nobel de médecine en 1902. Après avoir démissionné des services médicaux indiens, Ross travaille pour l'école de médecine tropicale de Liverpool alors récemment créée, et dirige les efforts d'éradication du paludisme en Égypte, au Panama, en Grèce et sur l'île Maurice[16].
En 1899, le zoologiste italien Giovanni Battista Grassi, se basant sur les travaux de Ross (sur les oiseaux), fit de même pour le vecteur chez les humains et prouva que le cycle vital du Plasmodium a besoin du moustique comme étape nécessaire.
L'année suivante, les découvertes de Finlay et Ross sont confirmées par une équipe médicale dirigée par Walter Reed et les recommandations sont mises en place par William C. Gorgas lors de la construction du canal de Panama. Les mesures de santé publique ainsi adoptées ont sauvé les vies de milliers d'ouvriers (alors que plusieurs milliers d'autres y étaient morts auparavant) et ont aidé à développer les futures méthodes de lutte contre la maladie.
XXe et XXIe siècles : à la recherche de traitements
Au début du XXe siècle, avant les antibiotiques, les patients atteints de syphilis étaient volontairement « traités » en les infectant avec le paludisme, pour leur donner de la fièvre. Dans les années 1920, Julius Wagner-Jauregg commence à traiter les neurosyphilitiques avec le paludisme induit par P. vivax. Trois ou quatre accès de fièvre se révèlent assez pour tuer les bactéries de syphilis, tandis que l'infection de paludisme est arrêtée avec la quinine. En contrôlant précisément la fièvre avec la quinine, les effets des deux maladies peuvent alors être maîtrisés. Bien que certains patients soient morts de la malaria, cette paludothérapie valait mieux qu'une mort certaine de la syphilis[17]. Afin de minimiser les risques létaux induits par Plasmodium falciparum, des essais furent même conduits avec les espèces simiennes Plasmodium richenowi, Plasmodium schwetzi et Plasmodium rodhaini[18]. La malariathérapie fut également utilisée pour traiter schizophrénie, oligophrénie avec schizophrénie greffée et grande agitation, psychoses affectives, chorée[19].
Le traitement thérapeutique par le paludisme fut également l'occasion d'accroître considérablement les connaissances sur la malaria ; il ouvrit la voie aux recherches en chimiothérapie et resta pratiqué jusque vers 1950. En 1974 , deux centres pratiquaient encore l'impaludation thérapeutique (l'un à Socola-Jassy en Roumanie, l'autre à Chamblee-Atlanta dans l'État de Georgie aux États-Unis).
En 1922, Stephens, identifia le 4e parasite connu du paludisme chez l'homme, P. ovale.La structure de la plasmoquine, ou paraquine, premier médicament antipaludique dérivé des aminoquinoloéines, découvert par les Allemands, n'est divulguée qu'en 1928. Les chercheurs britanniques, français et russes ont déjà remarqué l'action antipaludique des molécules de la série des amino-8 quinoléines. Ils se mettent à la recherche d'autres composés actifs[20]. En 1930, Ernest Fourneau et son équipe mettent au point à l'Institut Pasteur la rhodoquine[21],[22], efficace à des doses très inférieures à celles de la plasmoquine[23].
Dans les mêmes années 1930, aux laboratoires Elberfield de IG Farben en Allemagne, Hans Andersag et ses collègues synthétisent et testent environ 12 000 composants différents et arrivent à produire la Resochine®[24], un substitut de la quinine. Elle est liée à la quinine car elle possède un noyau de quinoline. Cette Resochine® (RESOrcinate d'un 4-aminoCHINoline : 7-chloro-4-[[4-(diethylamino)-1-methylbutyl]amino]quinoline) et un composant similaire, la Sontonchine (3-methyl Resochine) sont synthétisés en 1934 en coopération avec des entreprises américaines, grâce à plus de 2 000 accords entre IG Farben et des compagnies étrangères, comme Standard Oil of New Jersey, DuPont, Alcoa, Dow Chemical, Agfa, Winthrop Chemical Company et d'autres compagnies américaines[25]. Ce médicament est plus tard appelé Chloroquine. C'est un inhibiteur de la biocristallisation des pigments et un des meilleurs antimicrobiens jamais créés[26]. La quinine comme la chloroquine affectent les parasites de la malaria au début de leur cycle de vie, quand les parasites forment des pigments d'hématine, dérivant de la dégradation de l'hémoglobine.
Les propriétés insecticides du DDT (dichloro diphényl trichloro-éthane) sont établies, en 1939 par Paul Hermann Müller travaillant à Geigy Pharmaceutical à Bâle en Suisse grâce au Pyrethrum fait de Pyrèthre de Dalmatie (plante de la famille des chrysanthèmes) écrasée, l'épandage de DDT est une méthode standard de protection contre les insectes. Cependant, en raison de l'impact environnemental du DDT et de la résistance développée par les moustiques, le DDT est de moins en moins utilisé, surtout dans les zones où le paludisme n'est pas endémique (cf. section détaillée : « Les moyens de combattre le moustique ou de s'en protéger »).
En 1949, J.B.S. Haldane suggère que les thalassémiques hétérozygotes seraient plus résistants au paludisme. En novembre, Linus Pauling, Harvey Itano, S. J. Singer et Ibert Wells publient dans le journal Science la première preuve d'une maladie humaine causée par une protéine anormale[27]. En utilisant l'électrophorèse, ils démontrent que les individus atteints de drépanocytose ont une hémoglobine modifiée, et que les hétérozygotes, qui ont à la fois des formes normales et anormales d'hémoglobine, sont plus résistants aux infections de paludisme. C'est aussi ainsi que l'on démontre que les lois de Mendel déterminent les propriétés physiques des protéines, et non pas seulement leur absence ou présence : c'est le début de la génétique moléculaire.
Pendant la guerre du Vietnam, en réponse à une demande expresse des « Việt Cộng », une étude systématique de plus de 200 plantes médicinales chinoises est entreprise sous la direction de la pharmatologue Youyou Tu et de son groupe de recherche à Pékin en 1972. Le qing hao su (青蒿素), appelé artémisinine en Occident, est extrait à faible température dans un milieu neutre (pH 7) de plantes de qing hao (青蒿) séchées, d'après les instructions de Ge Hong. Celui-ci était le premier, au IVe siècle à recommander l'utilisation de qing hao pour le traitement de « fièvres intermittentes » dans son livre Handbook of Prescriptions for Emergencies. Il recommande de faire tremper les feuilles et les branches de l'armoise pendant une nuit, d'extraire le jus amer et de le boire directement.
Les premières cultures du parasite à leur phase sanguine sont réalisées en 1976 par Trager et Jensen, dans des jarres à bougies, ce qui facilite considérablement le développement de nouveaux médicaments[28].
Bien que les différentes étapes sanguines et le vecteur du paludisme (l'anophèle) aient été identifiés dès le XIXe siècle, ce n'est qu'en 1980 que la forme latente (cycles exo-érythrocytaires secondaires qui vont entretenir dans le foie la parasitose pendant 3 à 5 ans ou plus pour P. Vivax, 2 ou 3 pour P. Ovale et pendant la vie entière pour P. Malariae) du parasite dans le foie est observée[29]. La découverte de cette forme latente du parasite explique enfin pourquoi des individus apparaissent guéris du paludisme mais rechutent plusieurs années après que le parasite a disparu de leur sang (cf. section détaillée : « Phase hépatique »).
Présent
Voir la section détaillée : « Traitements actuels ».
Futur
Pharmacologie
- En 2004, l'équipe du Dr Jonathan Vennerstrom de l'université du Nebraska d'Omaha réussit à synthétiser de l'acide artémisinique pouvant être converti en artémisinine plus efficace (in vitro) que celle produite naturellement. Cette molécule (OZ-277 ou RBx11160) n'a à ce jour (avril 2011) produit aucune résistance connue de la part de Plasmodium.
- En mars 2006, deux équipes internationales[30] montrent l'efficacité de diverses plantes dont le Quassia. À la même date, des chercheurs de l'université de Lille I développent une molécule, la « ferroquine », en greffant à un endroit précis de la molécule de chloroquine un ferrocène. La ferroquine serait jusqu'à 30 fois plus efficace que la chloroquine. Aucun cas de résistance chez P. falciparum n'est apparu (tant sur des isolats de terrain que sur des lignées de parasites entretenues en laboratoire) (avril 2011).
- En septembre 2006, une équipe française[31] isole un principe antipaludique (la simalikalactone D) de la tisane de Quassia amara utilisée en Guyane contre le paludisme[32].
- En 2008, des biologistes du Georgia Institute of Technology d'Atlanta révélent que certains composés fongicides naturels de l'algue rouge Callophycus Serratus inhibent l'action du Plasmodium ; bien que le lien entre activité antifongique, antibactérien[33] ,[34] et antipaludique ne soit alors pas encore compris[35].
- En 2009 (publiation février 2010), des chercheurs de l'institut de technologie d'Atlanta identifient des composés anti-infectieux dits « bromophycolides » très efficaces in vitro contre des mycoses et contre le plasmodium falciparum [36].
- En janvier 2010, GlaxoSmithKline annonce rendre gratuitement accessible à la communauté scientifique une liste de plus de 13 500 molécules - ainsi que leurs structures chimiques - potentiellement actives contre P. falciparum afin de stimuler le développement de nouveaux traitements contre la maladie[37].
- En 2010, des chercheurs de l'école de santé pubique Johns Hopkins Bloomberg de Baltimore ont découvert qu'une bactérie appartenant au genre Enterobacter et vivant dans la flore intestinale d'Anopheles gambiae tue Plasmodium falciparum au moyen de radicaux libres. Environ 25 % des anophèles capturés près du Johns Hopkins Malaria Research Institute à Macha (sud de la Zambie) contenait cette souche bactérienne. L'étude a démontré que la bactérie inhibe la croissance de P.falciparum en culture in vitro d'origine humaine jusqu'à 99 % tout comme elle le fait dans le système digestif des anophèles[38],[39].
Vaccins
Le premier vaccin antipaludéen, le SPf66[40], basé sur un peptide synthétique, fut mis au point en janvier 1986 par Manuel Elkin Patarroyo. Son efficacité était toutefois assez faible voire nulle pour P.falciparum.
Actuellement trois types de recherche de deuxième génération sont basées sur les antigènes issus des différents stades du cycle évolutif parasitaire :
- vaccins anti-stade exo-érythrocytaire : ils visent à empêcher le sporozoïte de pénétrer ou de se développer dans les cellules hépatiques ;
- vaccins anti-stade sanguin asexué (antimérozoïte) : ils empêchent les mérozoïtes de pénétrer ou de se développer dans les hématies ;
- vaccins bloquant la transmission : ils induisent des anticorps empêchant la maturation des stades sexués du parasite chez l'anophèle.
Depuis 1992, un vaccin antimérozoïte prometteur appelé RTS, S/AS02A[41] est en développement chez GlaxoSmithKline Biologicals à Rixensart en Belgique. En décembre 2005, le professeur Alonso de l'université de Barcelone publie des résultats encourageants car il s'avèrerait efficace, dès la 1re injection, dans 30 % des cas et éviterait la moitié des crises graves[42]. Depuis le 26 mai 2009, il est au stade de la phase III des essais cliniques et les tests montrent que son efficacité sera supérieure aux espoirs[43]. Il est préparé à partir de peptides parasitaires de synthèse et de protéines recombinantes (capable d'échanger des informations génétiques avec une autre protéine) ou d'ADN (découvert dans les mitochondries et les apicoplastes de Plasmodium). Sachant que le parasite, pour pénétrer les hématies, prend la forme d'une protéine et est capable de muter une soixantaine de fois pour tromper le système immunitaire, cette piste utilise deux protéines recombinantes qu'elle fusionne :
- une partie de la protéine circumsporozoïtaire (CSP = Circum Sporozoïte Protein) de P. falciparum (RTS);
- l'antigène de surface du virus de l'hépatite B (S);
- un adjuvant qui est composé de 250 µl d'émulsion d'huile dans l'eau, de 50 µg de saponine QS21 et de 50 µg de (MPL™) lipide monophosphoryque immunostimulant A (AS02A).
C'est le vaccin de deuxième génération le plus avancé. Si toutes les études et les tests continuent à se dérouler normalement, il pourra être commercialisé au début de 2012, en conformité avec l'article 58 de l'Agence européenne des médicaments[44],[45], et entrer en phase IV des essais cliniques.
D'autres chercheurs visent une solution vaccinale :
- Depuis 2002, la Faculté de biologie et de médecine (FBM) de l'Université de Lausanne en Suisse étudie un vaccin antimérozoïte appelé PfCS102/AS02A[46] basé sur une peptide de synthèse circumsporozoïtaire (PfCS = Peptide Circum Sporozoïte Protein) de P. falciparum (PfCS102) renforcée par un adjuvant. Au départ, cet adjuvant fut le Montanide ISA 720 remplacé depuis par l'AS02A de GSK Bio car donnant une meilleure réponse du système immunitaire. Les résultats obtenus sont comparables au RTS, S/AS02A. Il est, depuis 2005, dans le stade de la phase II des essais cliniques.
- En novembre 2005, l'Institut Pasteur annonçait le début de la phase I des essais cliniques sur l'être humain d'un prototype de vaccin antimérozoïte basé sur les antigènes et appelé MSP3[47]. Pour le concevoir, les chercheurs ont étudié les mécanismes des personnes naturellement immunisées.
- En 2006, le Département de la Défense des États-Unis (DoD) demande à l'Institut de Médecine (IOM) de l'Académie nationale des Sciences (NAS) de reprendre le programme de recherche qu'il avait entamé en 1986 visant un vaccin pour les militaires contre P.falciparum[48].
- De novembre 2006 à décembre 2007, la faculté de médecine de l’université du Maryland et l'université de Bamako testaient ensemble en phase I des essais cliniques un vaccin FMP2.1/AS02A. Sa substance active est une protéine issue de P.falciparum (FMP2.1) et elle est renforcée par l'adjuvant AS02A. Un test effectué à Bandiagara au Mali sur 100 enfants âgés de 1 à 6 ans a démontré que l'accoutumance pharmacodynamique à la substance active était sans danger et que la réponse immunitaire 1 an après la vaccination restait élevée[49],[50]. Sur cette base, la même équipe est passée à phase II des essais cliniques de mai 2007 à juillet 2009 sur 400 enfants[51].
- En janvier 2010, L'University of Central Florida d'Orlando a annoncé un candidat-vaccin oral ou injectable à la fois efficace contre le paludisme et le choléra[52],[53]. Il cible l'immunité systémique et mucosale, via une construction antigénique fusionnant les épitopes de la sous-unité B (CTB) de la toxine cholérique avec des antigènes de la membrane apicale (AMA1) et d'une protéine de surface (MSP1) des mérozoïtes de P. falciparum.
Les chloroplastes d'un tabac et d'une laitue transplastomiques[54] ont été testés comme réacteurs pour produire ces protéines.
Selon l'étude, ces dernières, extraites et injectées à des souris se sont montrées capables de les protéger durant 300 jours contre la pénétration du parasite dans les globules rouges, et contre la toxine cholérique. La réponse immunitaire serait de type Tr1/Th2. Ce procédé a été breveté et pourrait permettre - s'il se montre aussi efficace chez l'Homme - de produire un vaccin peu cher, et ne nécessitant pas de stockage réfrigéré en cas d'usage oral.
Génétique
Les généticiens visent plutôt à combattre le parasite, non chez l'homme, mais chez son vecteur (moustique).
En 2000, l'équipe du Professeur Andrea Crisanti[55] de l'Imperial College London parvient a créer le premier moustique génétiquement modifié. En 2003, elle reconnait que si le gène marqueur persiste pendant une trentaine de générations lors de la fécondation entre moustiques modifiés, celui-ci ne subsiste que sur 4 à 16 générations lors d'une fécondation avec un moustique non modifié[56].
Depuis avril 2001, un consortium international visent le séquençage complet du génome d’Anopheles gambiae. Il est patronné par le Tropical Disease Research (TDR). Ce séquençage a été confié au Genoscope d'Évry et au Celera Genomics d'Alameda[57]. Le but est d'identifier les gènes impliqués dans l’immunité du moustique vis-à-vis des parasites des Plasmodium ou dans ses récepteurs olfactifs et gustatifs avec, à terme, la conception de molécules attractives ou répulsives pour le moustique ainsi que cibler les protéases impliquées dans sa réponse immunitaire[58],[59].
Le 15 juillet 2010, le professeur d'entomologie Michael Riehle annonce avoir réussi à créer avec son équipe à l'université d'Arizona, un Anopheles Stephensi femelle génétiquement modifié capable de détruire les parasites dans son corps et donc incapable de transmettre la maladie. Les chercheurs étudient maintenant le moyen de remplacer, dans la nature, les populations d'anophèles « normales » par celles issues du laboratoire[60], en espérant que ces moustiques ne deviennent pas invasifs en transmettant d'autres maladies, ou que le parasite ne contourne pas cette résistance.
Épidémiologie
Répartition dans le monde
Chaque année, le paludisme est la cause de 400 à 900 millions de cas de fièvres, et entre un et trois millions de morts[61], soit en moyenne un mort toutes les 30 secondes[62]. La grande majorité des victimes sont des enfants de moins de 5 ans[63], les femmes enceintes étant aussi particulièrement vulnérables car le placenta constitue une cible où les parasites (Plasmodium falciparum) peuvent s'accumuler. Malgré les efforts entrepris pour réduire la transmission de la maladie et améliorer son traitement, il y a eu peu d'évolution depuis le début des années 1990[64]. Il y a plus grave : si la prévalence du paludisme continue à son rythme actuel, le taux de mortalité pourrait doubler dans les vingt prochaines années[61]. Les statistiques précises sont difficiles à obtenir, en raison de la prévalence de la maladie dans les zones rurales, où les gens n'ont pas accès à un hôpital ou les moyens de se soigner. La plupart des cas ne sont pas documentés[61].
La co-infection avec le VIH n'accroît pas la mortalité, et pose moins de problème que la co-infection paludisme / tuberculose, les deux maladies s'attaquant habituellement à des tranches d'âge différentes : le paludisme est plus fréquent chez les jeunes tandis que la tuberculose atteint davantage les personnes âgées[65]. Cependant, la paludisme et le VIH contribuent à leur propagation mutuelle : le paludisme accroît la charge virale et l'infection du VIH augmente la probabilité d'une infection de paludisme[66].
Le paludisme est endémique dans les zones intertropicales dans les Amériques, dans de nombreux endroits d'Asie, et dans la plupart de l'Afrique. C'est toutefois dans l'Afrique sub-saharienne que l'on trouve 85 à 90 % des morts du paludisme[67]. La distribution géographique de la maladie au sein de grandes régions est complexe, et l'on trouve ainsi des zones paludiques et non-paludiques proches l'une de l'autre[68]. Dans les régions sèches, les périodes de paludisme peuvent être prédîtes sans trop d'erreurs en utilisant les cartes de précipitation[69]. À l'opposé de la dengue, le paludisme est davantage présent dans les campagnes que dans les villes[70]. Par exemple, les villes du Viêt Nam, du Laos et du Cambodge sont pratiquement exemptes de paludisme, mais celui-ci reste présent dans les campagnes[71]. En Afrique en revanche, le paludisme est présent aussi bien dans les zones rurales qu'urbaines, même si le risque est diminué dans les grandes villes[72]. Les niveaux endémiques mondiaux de la maladie n'ont pas été cartographiés depuis les années 1960. Cependant, le Wellcome Trust britannique finance le Malaria Atlas Project[73] afin de rectifier ceci et d'évaluer le poids de cette maladie à l'avenir.
Au final, le paludisme est la maladie parasitaire la plus répandue dans le monde. Elle est au 1er rang des priorités de l'OMS tant par ses ravages directs que par ses conséquences socio-économiques dont : une improductivité aboutissant à la sous-alimentation et au sous-développement.[réf. nécessaire]
L'être humain est loin d'être le seul hôte à subir le paludisme. Par exemple, nombreux sont les oiseaux qui sont porteurs de ces parasites, notamment de Plasmodium relictum.
En France
Jusqu'au XIXe siècle des épidémies de paludisme pouvaient se produire jusque dans le nord de l'Europe. La régression du paludisme en Europe est principalement due à l'assèchement des marais et au drainage des zones humides[74]. La disparition du paludisme en France a étonné les chercheurs à tel point qu'on a pu parler à ce propos de disparition spontanée, voire de disparition mystérieuse. Il semblerait que cette disparition ait eu de multiples causes. Dans des régions comme la Sologne par exemple, diverses innovations agronomiques portant notamment sur les pratiques culturales ont pu à cet égard jouer un rôle appréciable en cumulant chacune leur effet [1]. L'utilisation de la quinine, excellent antipaludéen, comme antithermique, bien avant celle de l'aspirine, a joué un grand rôle.
Actuellement la présence d'individus atteints de paludisme en France métropolitaine est due aux voyages. En 2008, la France a connu 4 400 cas. Une quarantaine de personnes en France en vingt ans ont été contaminées dans des aéroports[75] à cause de moustiques qui auraient voyagé dans des avions, depuis des zones empaludées.
Sur l'île de la Réunion et la République de Maurice, le paludisme était la première cause de mortalité, il y a encore 60 ans. L'éradication de la maladie a été confirmée par l’Organisation mondiale de la santé en 1979[76].
Régions à risques
Après avoir sévi dans la presque totalité du monde habité, le paludisme touche 90 pays[77], essentiellement les plus pauvres d'Afrique, d'Asie et d'Amérique latine. Dans les années 1950, le paludisme avait été éradiqué de la majeure partie de l'Europe et d'une grande partie de l'Amérique centrale et du sud par des pulvérisations de DDT et l'assèchement des marais.
En 2006, l'Europe a connu de très nombreux cas de paludisme d'importation principalement en France (5.267 cas), au Royaume-Uni (1.758 cas) et en Allemagne (566 cas)[78]. En France, 558 cas sont des militaires, mais la maladie touche également les touristes : sur cent mille d'entre eux se rendant dans une zone impaludée, trois mille rentrent dans leur pays infectés par l'une des formes connues de Plasmodium, le reste sont des cas importés par des immigrants.
- L'Afrique est un continent particulièrement touché par le paludisme ; il concerne 95 % des cas importés en France. Le danger est quasi-nul en Afrique du Nord mais majeur en Afrique de l'Est, en Afrique subsaharienne et en Afrique équatoriale aussi bien en zone rurale qu'en zone urbaine.
- En Asie, le paludisme est absent des grandes villes et plutôt rare dans les plaines côtières. Le danger est majeur dans les zones rurales du Cambodge, de l'Indonésie, du Laos, de la Malaisie, des Philippines, de la Thaïlande, du Viêtnam et en Chine dans le Yunnan et à Hainan.
- Dans les Antilles, le paludisme sévit à Haïti et près de la frontière dominicaine.
- En Amérique centrale, il existe quelques micro-zones, mais le risque est relativement faible.
- En Amérique du Sud, le risque est faible dans les grandes villes, mais réel dans les zones rurales en Bolivie, en Colombie, en Équateur, au Pérou et au Venezuela, et majeur dans toute la zone amazonienne.
L'altitude et la température ambiante sont des facteurs importants dans l'impaludation ou non dans une zone.
- Certains anophèles (comme Anopheles gambiae) ne peuvent vivre guère au-delà de 1.000 m d'altitude mais d'autres (comme Anopheles funestus) sont parfaitement adaptés pour vivre jusqu'à 2.000 m[79]
- La maturation de Plasmodium à l'intérieur de l'anophèle ne peut s'opérer que dans une fourchette de température ambiante allant de 16 à 35 C°
Impact socio-économique
Le paludisme est communément associé à la pauvreté, mais il représente aussi une cause majeure de la pauvreté et un frein important au développement économique et humain. La maladie a des effets économiques négatifs dans les régions où elle est répandue. Une comparaison du PIB par habitant en 1995, ajustée par parité à pouvoir d'achat, entre les pays touchés par le paludisme et ceux non touchés, montrait des écarts de 1 à 5 (1 526 USD contre 8 268 USD). De plus, dans les pays où le paludisme est endémique, le PIB pays habitant a cru de 0,4 % par an en moyenne de 1965 à 1990, contre 2,4 % pour les autres pays[80]. Cette corrélation ne montre toutefois pas que la causalité, et la prévalence du paludisme dans ces pays est aussi en partie dû aux capacités économiques réduites pour combattre la maladie.
Le coût économique du paludisme est estimé à 12 milliards de USD par an pour l'Afrique seule[81]. Un cas exemplaire est celui de la Zambie. Si le budget que le pays consacrait pour lutter contre cette maladie en 1985 était de 25 000 USD. Depuis 2008, grâce à l'aide internationale et au PATH (Program for Appropriate Technology in Health), il est de 33 millions répartis sur une période de 9 ans avec, comme 1er objectif la fourniture, à toute la population, de moustiquaires[82].
Au niveau individuel, l'impact économique inclut les frais de soins et d'hospitalisation, les jours de travail perdus, les jours de présence à l'école perdus, la baisse de productivité due aux dommages cérébraux créés par la maladie ; pour les états, à ces impacts s'ajoutent des baisses d'investissement et du tourisme[63]. Dans certains pays particulièrement touchés par le paludisme, la maladie peut être responsable de 40 % des dépenses publiques de santé, 30 à 50 % des patients admis à l'hôpital, et jusqu'à 50 % des consultations[83].
Causes
Le paludisme est causé par des parasites de l'espèce Plasmodium, eux-mêmes transmis par les moustiques du genre Anopheles.
Plasmodium, parasite du paludisme
 Un sporozoïte de Plasmodium se déplaçant dans le cytoplasme d'une cellule de l’épithélium de l'estomac (boyaux médians) d'un Anopheles stephensi. Micrographie électronique en fausses couleurs.
Un sporozoïte de Plasmodium se déplaçant dans le cytoplasme d'une cellule de l’épithélium de l'estomac (boyaux médians) d'un Anopheles stephensi. Micrographie électronique en fausses couleurs. Article détaillé : Plasmodium.
Article détaillé : Plasmodium.Le paludisme est causé par un parasite protozoaire du genre Plasmodium (Phylum apicomplexa). Chez les humains, le paludisme est, essentiellement, causé par P. falciparum (prépondérant en régions tropicales), P. malariae, P. ovale (espèce la plus rare, hormis l'Afrique de l'Ouest) et P. vivax (espèce la moins exigeante en température).
P. falciparum est la cause la plus commune des infections et responsable d'environ 80 % de tous les cas de paludisme ainsi que 90 % des décès[84]. Les Plasmodium infectent également les oiseaux, les reptiles, les singes, les chimpanzés et les rongeurs (animaux à sang chaud)[85]. On a rapporté des cas d'infections humaines avec des espèces simiesques du paludisme, dont P. knowlesi, P. inui, P. cynomolgi[86], P. simiovale, P. brazilianum, P. schwetzi et P. simium. Cependant, à l'exception de P. knowlesi, ces infections restent limitées et sans importance en termes de santé publique. Le paludisme aviaire peut tuer les poulets et les dindes, mais cette maladie ne cause pas de dommages économiques notables à l'agriculture[87]. Cependant, depuis qu'il a été introduit par les humains, le paludisme a décimé les espèces endémiques d'oiseaux d'Hawaii, qui avaient évolué, en son absence, sans défense contre celui-ci[88].
Le Plasmodium se présente sous la forme d'un protozoaire très petit (1 à 2 µm selon les formes). La coloration au May-Grünwald-Giemsa montre qu'il est constitué d'un cytoplasme bleu pâle entourant une vacuole nutritive claire et contenant un noyau rouge et du pigment brun-doré ou noir (hémozoïne).
Le cycle évolutif du Plasmodium est assez complexe et nécessite deux hôtes, un hôte intermédiaire : l'homme et un hôte définitif : la femelle hématophage d'un moustique du genre Anopheles (du grec anôphelês signifiant : inutile). D'un point de vue strictement biologique, le véritable hôte définitif est le moustique (la reproduction sexuée parasitant l'anophèle). L'homme ne serait qu'un hôte intermédiaire dans son cycle réplicatif. Néanmoins, pour des raisons anthropocentriques, on considère que le vecteur n'est pas l'homme mais le moustique et par conséquent que cette zoonose est du type zooanthroponose.
Anophèle, vecteur du paludisme
Article détaillé : Anophèle.Technique de chasse de l'anophèle
Seules les femelles sont hématophages. Les mâles dont les seules activités sont la reproduction de l'espèce et voler de-ci de-là pour se nourrir de jus de plantes et de nectar ne transmettent pas la maladie.
Les femelles anophèles se nourrissent de préférence la nuit, et commencent à chercher leur repas au crépuscule, en continuant pendant la nuit jusqu'à ce qu'elles l'aient trouvé.
Lorsque les humains ou les animaux respirent, ils produisent du CO2 et leur corps dégage constamment de la chaleur et de l'humidité (transpiration) ainsi que beaucoup d'autres substances attractives comme l'acide lactique ou le sébum[89]. Les moustiques, ainsi que d'autres insectes piqueurs, sont capables de détecter toutes ces émanations depuis de longues distances (± 20 m pour le CO2) et sont immédiatement attirés par ces sources. Les moustiques sont également attirés par les vapeurs d'alcool ou par les couleurs foncées et plus spécialement le noir. Ils se déplacent (maximum 2 km) en utilisant leurs capteurs.
Ne pas confondre les différents moustiques vecteurs Nom de la zoonose Cause Transmission Vecteur Le jour
La nuit
femelle Aedes
femelle Anopheles funestus
Virus
Le jour
femelle Aedes
Virus
La nuit
femelle Culex
Virus
Le jour
femelle Aedes
Parasite
La nuit
femelle Anopheles
Virus
La nuit
femelle Anopheles
Paludisme
Parasite
La nuit
femelle Anopheles
Cycle du parasite chez l'anophèle
Le vecteur du parasite ainsi que son hôte primaire est la femelle d'un moustique du genre Anophèle. Les jeunes moustiques ingèrent le parasite pour la première fois lorsqu'ils se nourrissent du sang (nécessaire à cette femelle pour sa production d'œufs) d'un sujet humain infecté. Une fois ingérés, les gamétocytes de Plasmodium se différencient en gamètes mâles et femelles puis s'unissent pour former un zygote mobile, appelé ookinète, qui pénètre la paroi stomacale du moustique pour devenir un oocyste sphérique, dont le noyau va se diviser à de multiples reprises pour former des sporozoïtes. La durée de cette maturation est étroitement dépendante de la température extérieure. Par exemple pour P. falciparum : pas de maturation en dessous de 18 °C ou au-dessus de 35 °C, elle est maximale vers 24 °C. Quand l'oocyste rompt, il relâche les sporozoïtes qui migrent dans le corps du moustique jusqu'aux glandes salivaires d'où ils peuvent, lors d'un nouveau repas de sang, infecter un nouvel hôte humain, en traversant la peau avec la salive[90],[91].
Cycle du parasite chez l'humain
Phase hépatique
Mince fuseau de 12 µm / 1 µm, le sporozoïte infectieux injecté à l'homme, lors de cette piqûre par une femelle d'anophèle infectée, circule rapidement (moins d'une demi-heure) dans le sang jusqu'au foie dans lequel il est séquestré en grande partie grâce aux motifs adhésifs de la protéine majoritaire de son enveloppe (protéine circumsporozoïte ou CSP = Cysteine String Protein), pour ensuite infecter les hépatocytes. Cette crise pré-érythrocytaire hépatique qui va durer de 7 à 15 jours pour P. falciparum, de 15 jours à 9 mois pour P. vivax, de 15 jours à X mois pour P. ovale et 3 semaines pour P. malariae permettra au parasite de poursuivre son cycle. Les sporozoïtes qui n'atteindront pas le foie seront soit éliminés par les phagocytes, soit incapables de poursuivre leur évolution s'ils atteignent d'autres organes.
Une première transformation arrondit cette forme « cryptozoïte » (du grec κρυπτός (kruptos) signifiant « caché ») en un élément uninucléé (avec un seul noyau) appelé trophozoïte qui est l'occasion pour le parasite de se multiplier directement (il en est toujours ainsi pour P. falciparum), par schizogonie, pendant une semaine à quinze jours aboutissant à un énorme schizonte (nom donné au protozoaire lorsqu'il devient actif après la phase d'incubation) de 40 à 80 µm. Ce corps bleu (parce que constitué d'un cytoplasme bleu pâle lorsqu'il est coloré au May-Grünwald-Giemsa) bourgeonne, tout en perdant de sa mobilité, de manière à émettre des vésicules, contenant les jeunes mérozoïtes qui seront transférés dans le sang, initiant ainsi le stade érythrocytaire, c'est-à-dire l'infection des globules rouges.
Cependant, certains mérozoïtes de P. ovale ou P. vivax peuvent rester cachés dans le foie plusieurs années, voire la vie entière pour P. malariae, avant de se réactiver en vagues successives. Cette phase du parasite est appelée « phase dormante » : le Plasmodium ne se réplique pas mais dort, d'où les noms qui lui sont donnés à ce moment-là : « hypnozoïte » (du grec Ὕπνος qui est Hypnos l'antique dieu grec du sommeil).
Phase de transfert
Les vésicules sont libérées dans les sinusoïdes hépatiques (vaisseaux capillaires du foie faisant la jonction entre celui-ci et le réseau sanguin) pour rejoindre ensuite la circulation sanguine et y répandre un flot de jeunes mérozoïtes « pré-érythrocytaires » prêts à infecter les globules rouges. Chaque cellule de foie infectée contient environ 100 000 mérozoïtes (chaque schizonte est capable de produire 20 000 mérozoïtes). C'est une véritable technique de « Cheval de Troie » qui est ici utilisée pour passer des cellules hépatiques au sang. L'imagerie in vivo a montré en 2005-2006 chez des rongeurs que les mérozoïtes étaient capables de fabriquer des cellules mortes leur permettant de quitter le foie pour la circulation sanguine en échappant ainsi au système immunitaire). Ils semblent à la fois guider ce « véhicule » et s'y cacher en masquant les signaux biochimiques qui alertent normalement les macrophages. Il y a peut-être là une piste nouvelle pour des médicaments actifs ou un vaccin anti-stade exo-érythrocytaire avant le stade de l'invasion des globules rouges.
Phase sanguine
Au début de la longue phase sanguine[92] : les mérozoïtes s'accolent aux globules rouges, les envahissent, s'y développent en trophozoïtes puis s'y divisent (schizontes). En se diffusant, les mérozoïtes font éclater les globules rouges (c'est l'hémolyse). Ce sont ces éclatements brutaux et synchrones qui sont à l'origine des accès de fièvre. Le temps qui s'écoule entre la pénétration d'un parasite dans un globule rouge et l'éclatement de celui-ci est assez constant et atteint chez l'être humain 48 heures pour P. vivax, P. ovale et P. falciparum (fièvres tierces) et 72 heures pour P. malariae (fièvre quarte). La destruction des globules rouges provoque une anémie et, dans le cas du paludisme cérébral (voir le sous titre sur ce sujet), la mort intervient à la suite d'une obstruction des vaisseaux sanguins du cerveau par les globules rouges infectés. Cette destruction de globules rouges s'accompagne de la libération d'hémozoïne, qui va perturber le fonctionnement de l'hypothalamus (production de cytokine comme le TNFα)[93] et causer de très fortes fièvres qui peuvent aller jusqu'à l'hyperpyrexie.
L'éclatement des schizontes mûrs ou « rosaces » termine le premier cycle schizogonique érythrocytaire en libérant dans le sang, avec les déchets du métabolisme plasmodial (pigments et débris cellulaires du globule rouge), une nouvelle génération de plasmodiums, les mérozoïtes « érythrocytaires » capables de réinfecter d'autres globules rouges.
Une succession régulière de cycles semblables va suivre, qui seront progressivement remplacés (les défenses immunitaires s'organisant) par des cycles érythrocytaires gamogoniques préparant les formes sexuées. Les trophozoïtes arrêtent de se diviser et modifient leur rapport nucléo-plasmatique. Ces formes de trophozoïtes avec un noyau volumineux et un cytoplasme densifié sont des gamétocytes mâles et femelles, qui vont demeurer en attente dans le sang.
Les parasites lors de cette phase n'ont aucune chance de survie dans l'être humain : ils restent vivants une vingtaine de jours puis disparaissent. Ils ne pourront poursuivre leur évolution que chez le moustique. À ce moment si un anophèle femelle pique une personne malade, il absorbe des gamétocytes contenus dans le sang, et un nouveau cycle, sexué cette fois, débute dans le moustique. Les sporozoïtes produits par cette reproduction passent dans la salive du moustique, qui peut infecter un nouvel hôte, et ainsi de suite…
Remarque
Pour P. Falciparum c'est là tout le cycle de vie. Avec les autres Plasmodium, certains mérozoïtes pré-érythrocytaires, ne gagnent pas le sang directement, mais s'attaquent à de nouveaux hépatocytes : c'est le début des cycles exo-érythrocytaires secondaires qui vont entretenir dans le foie la parasitose pendant deux ou trois ans pour P. Ovale, 3 à 5 ans ou plus pour P. Vivax et pendant la vie entière pour P. Malariae.
Animation et schéma du cycle parasitaire du Plasmodium
- Animation Adobe Flash Player
- Schéma

Autres causes de transmission
Les parasites peuvent aussi être transmis par voie placentaire de la mère au fœtus (paludisme congénital), par partage d'une seringue souillée ou par transfusion sanguine, bien que ce dernier moyen de transmission soit assez rare[94].
Diagnostic
Symptômes
- Fatigue généralisée,
- Perte d'appétit,
- Vertiges,
- Céphalées,
- Troubles digestifs (embarras gastrique), nausées, vomissements, douleurs abdominales,
- Diarrhée,
- Myalgies.
Signes cliniques
- Fièvre,
- Tremblements intermittents,
- Arthralgies,
- Signes d'anémie causée par l'hémolyse,
- Hémoglobinurie,
- Convulsions,
- Ictère.
Des sensations de picotements peuvent aussi apparaitre dans la peau, notamment quand le paludisme est causé par P. falciparum. Le symptôme le plus classique du paludisme est la répétition cyclique d'une sensation de froid soudaine suivie de frissons avec fièvre et hyperhidrose durant quatre à six heures, survenant toutes les 48 heures lors des infections dues à P. falciparum, P. vivax et P. ovale, ou toutes les 72 heures pour celles dues à P. malariae[95] (cependant, P. falciparum peut entrainer des fièvres toutes les 36 à 48 heures ou une fièvre continue et moins prononcée). Le paludisme grave[96] est causé quasi exclusivement par les infections de P. falciparum et survient généralement 6 à 14 jours après l'infection[97]. Ce type de paludisme peut entrainer le coma et la mort s'il n'est pas traité, surtout chez les jeunes enfants et les femmes enceintes qui sont particulièrement vulnérables. Des céphalées sévères, qui seront corroborées par une ischémie cérébrale, constituent un autre symptôme aspécifique du paludisme. D'autres signes cliniques incluent une splénomégalie, une hépatomégalie, de l'hypoglycémie ainsi qu'une altération de la fonction rénale lors des examens cliniques. Si les reins cessent de fonctionner, une fièvre particulière peut survenir, lorsque l'hémoglobine des globules rouges fuit dans l'urine.[réf. souhaitée] Le paludisme sévère peut progresser extrêmement rapidement et causer la mort en quelques jours voire quelques heures[97] d'où l'intérêt d'un diagnostic réellement empirique et rapide . Dans les cas les plus graves, le taux de mortalité peut dépasser 20 %, même avec des soins importants[98].
Pour des raisons encore peu comprises, mais pouvant être liées à la pression intracrânienne, les enfants atteints du paludisme ont parfois une posture anormale en extension (posture opisthotonique), indiquant un paludisme cérébral[99]. Ce paludisme peut entrainer des retards cognitifs car il cause une anémie générale pendant une période de développement cérébral rapide induisant des dommages neurologiques auxquels les enfants sont plus vulnérables[100],[101] et, ainsi, causer, à plus long terme, des problèmes de développement[102].
Anamnèse
Dans de nombreux endroits, même un simple diagnostic en laboratoire n'est pas possible et l'historique des fièvres est utilisé comme indication pour poursuivre un traitement antipaludique ou non. Mais cette méthode n'est pas la plus efficace : au Malawi, l'utilisation de frottis sanguin colorés par Giemsa a montré que les traitements antipaludiques inutiles ont diminué quand les indicateurs cliniques (température rectale, pâleur du lit des ongles, splénomégalie) ont été utilisés plutôt que l'historique des fièvres (la sensibilité s'est accrue de 21 à 41 %)[103].
Le paludisme concernant les enfants est trop souvent soit mal diagnostiqué (mauvaise anamnèse, mauvaise interprétation des tests de terrain) en 1re ligne par les auxiliaires médicaux locaux (« Community Health Workers » aussi appelés « Barefoot doctors » en anglais)[104], à la place d'autres maladies, soit mal évalué, par ceux-ci, en termes de dose médicamenteuse empêchant, ainsi, un traitement efficace[105].
Examen clinique
Les manifestations cliniques du paludisme n'apparaissent qu'au cours de la multiplication asexuée des plasmodiums à l'intérieur des hématies faisant du paludisme, au sens propre, une érythrocytopathie parasitaire. Cette dernière aboutit à :
- des accès fébriles violents et rythmés ;
- une destruction massive d'hématies (directe et indirecte) qui entraîne une anémie hémolytique et réaction du SRH (splénomégalie progressive)[réf. souhaitée] ;
- une biligénie pigmentaire, d'où subictère (et hépatomégalie de reprise)[réf. souhaitée] ;
- une détérioration de l'état général pouvant aboutir à la cachexie[réf. souhaitée].
L'étude des cycles (voir plus haut) permet de comprendre le déroulement d'un paludisme non traité.
Les 6 à 10 accès constituant l'atteinte de primoinvasion seront suivis d'atteintes semblables de recrudescence tant que durera l'état latent la parasitémie responsable de la première atteinte, soit de deux mois à deux ans selon le plasmodium. Pour P. Falciparum les choses s'arrêteront là[réf. souhaitée].
Pour les plasmodiums récurrents (P. Vivax, P. Ovale et P. Malariae) de nouvelles atteintes de récurrence dues à des réinfestations sanguines au départ des cycles hépatiques exoérythrocytaires secondaires peuvent prolonger l'affection dans les délais déjà indiqués . Les atteintes typiquement rythmées de la forme classique, n'apparaissent plus guère aujourd'hui, même dans la zone d'endémie à cause de l'emploi généralisé des drogues chimiothérapiques et chimioprophylactiques. Elles se rencontrent encore dans les « paludismes à la seringue » dont on respecte l'évolution normale dans un but thérapeutique (malariathérapie) et dans les paludismes récurrents[réf. souhaitée].
Des enquêtes récentes suggèrent que la rétinopathie malariale pourrait être meilleure que les autres méthodes pour distinguer le coma paludique et non-paludique[106].
Signes cliniques concernant les accès de fièvre Espèce Période d'incubation Type de fièvre Intervalles entre les fièvres P. falciparum 7–30 jours
plus (10 %)*Fièvre tierce maligne (« Malaria tropica ») ± 48 heures P. malariae 16–50 jours Fièvre quarte bénigne 72 heures P. ovale 12–18 jours
plus (10 %)*Fièvre tierce bénigne 48 heures P. vivax 12–18 jours
plus (10 %)*Fièvre tierce bénigne 48 heures (* en cas d'insuffisance de prophylaxie anti-malarique) Examens complémentaires
Examen sanguin au microscope
La méthode de diagnostic la moins chère (entre 0,40 et 0,70$US par lame), la plus fiable et la plus répandue est l'examen au microscope optique d'un frottis sanguin et d'une goutte épaisse de sang. Le frottis permet d'identifier les caractéristiques uniques de chacune des quatre espèces du parasite d'Homo sapiens car l'aspect du parasite est mieux conservé avec ce prélèvement. La goutte de sang épaisse permet de parcourir un volume sanguin plus large pour faire le diagnostic et de ne pas passer à côté de Plasmodium. La sensibilité de la goutte épaisse est environ 11 fois plus élevée que la méthode par plaque fine (frottis). Les deux préparations peuvent être faites sur la même lame pour autant que l'on débute par le frottis[107].
Des niveaux d'infection plus bas peuvent être détectés avec la goutte épaisse mais l'apparence du parasite est déformée et il est plus difficile de distinguer les espèces. Les deux méthodes sont donc utilisées pour un diagnostic complet[108]. Avec cette goutte épaisse, un opérateur expérimenté peut, dans de bonnes conditions (éclairage direct électrique), détecter des niveaux de parasitémie très bas (de l'ordre de 0,0001 % des globules rouges)[109]. De nombreuses tentatives ont été faites pour améliorer l'examen microscopique, mais aucune ne s'est avérée supérieure à la méthode classique de coloration Giemsa et d'examen en immersion d'huile (la lentille frontale du microscope baigne dans un liquide d'indice de réfraction proche de celui du verre comme l'huile de cèdre ou une huile de synthèse).
Le diagnostic au microscope peut, en outre, être difficile car les premiers trophozoïtes (« en anneau ») des quatre espèces ont une apparence presque identique. L'identification de l'espèce doit, alors, toujours se baser sur plusieurs trophozoïtes.
Tests de terrain
Lorsqu'un microscope n'est pas disponible ou qu'il y a trop peu de personnel médical formé au diagnostic du paludisme, il est possible d'utiliser des tests de détection rapide d'antigènes, qui n'ont besoin que d'une goutte de sang[110]. Ces tests immunochromatographiques (également appelés tests de diagnostic rapide du paludisme ou TDR)[111] peuvent se présenter sous la forme d'une cassette, d'une bandelette réactive ou d'un « dipstick ». Ces tests utilisent une goutte de sang du doigt ou d'une veine, ils durent 15 à 20 minutes si l'utilisateur a été préalablement formé à leur maniement et à l'interprétation du résultat sinon, ils devront être transportés en caisson réfrigéré vers un laboratoire. La limite de détection avec ces tests est de l'ordre de 100 parasites par microlitre (µl) de sang, contre 5 par le dépistage au microscope.
Les premiers tests rapides utilisaient le glutamate déhydrogénase (GluDH) de P. falciparum comme antigène cible (PGluDH)[112] mais il a été vite remplacé par le lactate déshydrogénase (LDH) de P. falciparum (PLDH). C'est la dernière enzyme du parcours glycolytique (essentielle pour la génération d'ATP) et une des plus abondantes générées par P. falciparum. La concentration de PLDH sanguin est assez étroitement corrélée à la présences des parasites. La disparition de l'antigène après le traitement permet d'utiliser le test pLDH pour prédire le succès ou non d'un traitement.
Il existe des dizaines de TDR ayant chacun leur(s) spécificité(s) :
- l'Optimal IT® permet de distinguer P. falciparum et P. vivax grâce aux différences antigéniques entre les isoenzymes pLDH ; ce test permet de détecter P. falciparum jusqu'à une parasitémie de 0,01 %, et les non-falciparum jusqu'à 0,1 % ;
- le ParaCheck Pf® peut détecter des parasitémies de 0,002 % mais ne distingue pas les espèces ;
- d'autres comme ICT Malaria® ou ParaHIT® sont centrés sur l'antigène HRP2[113].
Méthode moléculaire en laboratoire
Des méthodes moléculaires sont disponibles dans certains laboratoires. Ces méthodes d'analyse en temps réel (comme la PCR en temps réel, basée sur la réaction en chaîne par polymérase) sont en développement dans l'espoir de les mettre en place dans les zones endémiques[114].
Les acides nucléiques des parasites sont détectés par réaction en chaîne par polymérase (PCR), une technique plus précise que la microscopie, mais aussi plus chère car demandant un laboratoire spécialisé, une parfaite maitrise de la méthode de prélèvement de l'échantillon et, s'il y a lieu, un respect de la chaine du froid irréprochable pendant le stockage et le transport. De plus, les niveaux de parasitémie ne sont pas nécessairement corrélés avec la progression de la maladie, en particulier quand le parasite peut adhérer aux parois des vaisseaux sanguins, d'où l'intérêt des méthodes moins avancées.
Différents types de paludisme
Les complications graves ne concernent en général que Plasmodium falciparum.
Le paludisme chronique peut être causé par P. vivax, P. ovale et surtout P.malariae mais pas par P. falciparum. Dans le cas du paludisme chronique, la maladie peut réapparaitre plusieurs mois ou années après l'exposition, en raison de la présence latente de parasites dans le foie. Ainsi, on ne peut pas dire qu'un sujet est guéri du paludisme simplement en observant la disparition des parasites du flux sanguin. La période d'incubation la plus longue rapportée pour P. vivax est de 30 ans[97]. Environ un cas de paludisme P. vivax sur cinq dans les zones tempérées implique l'hibernation par les hypnozoites (les rechutes commencent l'année après la piqûre du moustique)[115].
Accès palustres simples
La « crise de paludisme », appelée également « accès palustre », peut être suspectée au retour d'une zone d'endémie et est caractérisée par des accès fébriles, avec une fièvre à plus de 40 °C, des frissons, suivis d'une chute de température accompagnée de sueurs abondantes et d'une sensation de froid.
Classiquement, on distingue la fièvre tierce (c'est-à-dire survenant tous les deux jours) due à Plasmodium vivax et Plasmodium ovale (fièvre tierce bénigne) et Plasmodium falciparum (fièvre tierce maligne) de la fièvre quarte (c'est-à-dire survenant tous les 3 jours) due à Plasmodium malariae (le terme « malaria » désignait spécifiquement la fièvre quarte).
Ces accès palustres peuvent se répéter pendant des mois voire des années avec P. ovale, P. vivax et P. malariae, mais pas avec P. falciparum, s'ils sont correctement traités et en l'absence de réinfestation (cas du paludisme d'importation, en général).
Paludisme viscéral évolutif
Autrefois appelée cachexie palustre, associant fièvre intermittente modérée, anémie et cytopénie, splénomégalie modérée chez des enfants de 2 à 5 ans. Dans le paludisme viscéral évolutif, l'organisme est visiblement débordé, et il faut le défendre à tout prix en s'attaquant successivement aux formes sanguines et tissulaires :
- Chloroquine (Nivaquine*) 600 mg (2 comprimés à 0,30 g) par jour les 2 premiers jours, puis 300 mg (1 comprimé à 0,30 g) par jour les 3 jours suivants puis,
- Primaquine* 15 mg (3 comprimés à 0,5 mg) par jour pendant 15 jours, soit du 6e au 20e jour inclus.
Il faut surveiller les signes d'intolérance aux 8-ammino-quinoléïnes (vertiges, nausées, diarrhée, cyanose, hémoglobinurie, agranulocytose) bien qu'ils soient rares à cette posologie.
Néphrite quartane
Le plasmodium malariae est susceptible d'entraîner une infection à répétition (ou chronique) attaquant les glomérules, à l'origine d'un syndrome néphrotique par la dissolution de complexes immunitaires (associations anticorps-antigène). Tous les sujets présentant une infection répétée par plasmodium malariae ne présentent pas une atteinte rénale. L'examen au microscope électronique des prélèvements rénaux permet d'identifier la lésion. Cet examen met en évidence des dépôts de complément (éléments intervenant dans le système immunitaire) et d'immunoglobulines (variété de protéines jouant le rôle d'anticorps). Le laboratoire détecte chez l'enfant des antigènes de plasmodium malariae. Le pronostic est meilleur quand il s'agit de dépôts immunofluorescents à prédominance d'IgG3 et de granulation grossière avec protéinurie sélective (les reins ne laissent passer qu'une certaine variété de protéines et non pas toutes). Les sujets présentant des dépôts fins granuleux à prédominance d'IgG2 et une protéinurie non sélective (les reins laissent passer toutes les protéines) ont un moins bon pronostic. Traitement : la néphrite quartane ne répond pas toujours aux traitements antipaludiques ni aux corticoïdes ainsi qu'aux médicaments cytotoxiques.
Accès palustres graves à Plasmodium falciparum
Paludisme cérébral ou neuropaludisme
Cette malaria cérébrale, appelée ainsi à cause de l'obstruction des capillaires du cerveau par les débris d'hématies éclatées, associe une élévation importante de la température (40 °C) et un coma (d'une durée souvent supérieure à 30 minutes). Elle est de mauvais pronostic malgré le traitement. La mortalité s'élève parfois à 20 % chez les adultes et 15 % chez les enfants. L'apparition d'une telle malaria sévère peut être soit progressive soit brutale.
Elle débute après des convulsions instantanées et passagères d'un ou plusieurs muscles, suivies de décontractions. Ces convulsions sont localisées ou généralisées à l'ensemble du corps. Elles surviennent essentiellement chez les enfants et les femmes enceintes et dans seulement 50 % des cas chez les autres adultes. Cela est dû à un mauvais fonctionnement du foie et à une consommation exagérée de sucre par le parasite. Les femmes enceintes sont particulièrement prédisposées à l'hypoglycémie et à la surproduction d'acide lactique entrainant une augmentation de l'acidité du sang.
L'examen physique complémentaire montrera aussi (tous ou une partie) des symptômes suivants :
- un nystagmus dans le plan horizontal de façon incessante,
- quelquefois une raideur du cou et une perturbation des réflexes,
- dans environ 15 % des cas, il existe des hémorragies de la rétine,
- un ictère,
- une posture opisthotonique (en extension)n
- des urine de couleur noire,
- une hématémèse due sans doute à une atteinte de l'estomac par ulcération due au stress.
L'examen de laboratoire mettra en évidence :
- un œdème pulmonaire qui n'est pas bien expliqué mais peut être à l'origine d'un taux de mortalité dépassant 80 %,
- une atteinte des reins (plus rare chez l'enfant mais s'accompagnant également d'une forte mortalité). Son mécanisme n'est pas non plus éclairci,
- une anémie qui est le résultat de la destruction et de l'élimination accélérée des globules rouges par la rate, associées à un déficit de production de ces globules par la moelle osseuse (aplasie médullaire). Elle nécessite généralement une transfusion. Celle-ci pose des problèmes chez l'enfant et est à l'origine de la présence d'hémoglobine dans le sang, d'urine de coloration noire et de l'insuffisance de fonctionnement des reins.
Une autre complication susceptible de survenir au cours de cette variété de la malaria est la fièvre bilieuse hémoglobinurique.
Fièvre bilieuse hémoglobinurique
Complication actuellement rarissime survenant chez des individus anciennement atteints de la malaria à Plasmodium falciparum vivant dans les pays de forte endémie (où une grande partie de la population est touchée) et liée à la prise de quinine ou d'autres molécules de synthèse comme l'halofantrine (dérivé phénanthrène-méthanol) (Halfan®). Elle est consécutive à un éclatement des globules rouges à l'intérieur des vaisseaux (hémolyse intra-vasculaire).
L'examen clinique caractérisera :
- une fièvre élevée,
- un état de choc avec prostration,
- un ictère,
- des urines de plus en plus foncées contenant des cylindres hyalins (vitreux).
Tandis que l'examen de laboratoire mettra en évidence :
- une anémie,
- une hémoglobinurie (présence d'hémoglobine dans les urines, leur donnant une couleur porto),
et surtout
- une insuffisance rénale mortelle due à une destruction des tubules rénaux (tubes entortillés des pôles urinaires) appelée nécrose tubulaire aiguë.
C'est une urgence médicale car considérée comme un accès pernicieux. Le traitement aura 3 buts :
- maîtriser l'oligo-anurie (diminution voire disparition de l'émission d'urine par les reins),
- déparasiter le malade,
- traiter l'anémie hémolytique.
Contre l'oligo-anurie : la dialyse péritonéale permettra de franchir la phase critique en attendant le rétablissement de la diurèse.
Contre la parasitémie, un véto absolu contre la quinine, ici totalement contre-indiquée à cause de l'hémolyse ainsi que contre les sulfamidés à cause de la tubulopathie rénale (maladie affectant les néphrons). On se contentera de chloroquine (Nivaquine®) à raison d'une injection unique de 300 mg par voie intramusculaire.
Contre l'anémie hémolytique, on pratiquera au choix des transfusions, résolument isogroupes (sang de même groupe ABO), ou des exsanguino-transfusions.
Malaria de la femme enceinte
L'infection du placenta par le plasmodium falciparum se traduit par un poids de naissance faible, tout particulièrement quand il s'agit d'un premier accouchement (primipare).
Quand la quantité de parasites dans le sang est relativement peu importante (c'est le cas dans les zones de transmission stable), les femmes ne présentent pas de signes alors que les parasites qui envahissent les globules rouges de la circulation, et plus précisément de la petite circulation du placenta, sont présents. Dans les zones où la transmission est instable (on parle d'hypo ou de méso-endémie), les femmes enceintes présentent des infections sévères associées à des quantités élevées de parasites dans le sang avec une anémie, une hypoglycémie et des œdèmes des poumons. La grossesse est alors émaillée de problèmes à type de contractions prématurées, d'avortement spontané et de mortalité au moment de l'accouchement. La malaria congénitale touche environ 5 % des nouveau-nés de mères infectées et est en relation directe avec la quantité de parasites dans le placenta.
Malaria transfusionnelle
C'est une malaria transmise par l'intermédiaire d'une transfusion sanguine ou après échange d'aiguilles entre individus drogués. P. malariae et P. falciparum sont le plus souvent mis en cause. Dans ce cas, la période d'incubation est courte car il n'existe pas de cycle pré-érythrocytaire (se déroulant avant l'envahissement des globules rouges). La malaria transfusionnelle se traduit par les mêmes signes que ceux que l'on observe par le Plasmodium en cause. Néanmoins, P. falciparum est le plus souvent sévère chez les toxicomanes. Le traitement, qui utilise le primaquine quand il s'agit d'une infection à P. ovale ou P. vivax, est alors inutile, du fait de la différence du cycle de transmission de la malaria transfusionnelle[réf. souhaitée].
La malaria de l'enfant due à falciparum
À l'origine d'environ 1 à 3 millions de décès chaque année, cette variété de la malaria touche essentiellement les Africains et s'accompagne de :
- troubles neurologiques avec des convulsions pouvant aller jusqu'au coma,
- hypoglycémie,
- augmentation du taux d'acidité du sang (acidose métabolique),
- anémie sévère.
Contrairement aux autres formes de la malaria, la malaria de l'enfant ne s'accompagne pas ou peu souvent d'une atteinte rénale à type d'insuffisance de filtration des reins (insuffisance rénale) ni d'une collection liquidienne dans les poumons (œdème pulmonaire aigu). Dans cette variété de la malaria, le traitement est généralement efficace et rapide.
Splénomégalie tropicale
Dénommée actuellement splénomégalie palustre hyper-immune, cette splénomégalie se rencontre chez quelques individus qui vivent dans une zone où la malaria est endémique. Ces personnes présentent une réponse immunologique anormale aux infections dues à la malaria, ce qui se traduit, en dehors de la splénomégalie, par une hépatomégalie, l'élévation d'un certain type d'immunoglobulines dans le sang (IgM, anticorps anti-palustres) et du nombre de lymphocytes à l'intérieur des sinusoïdes hépatiques.
La biopsie du foie et l'examen au microscope optique permettent de porter le diagnostic.
Les symptômes sont :
- tiraillement abdominal,
- présence d'une masse abdominale,
- douleurs abdominales violentes (péri-spléniques : inflammation des tissus environnant la rate),
- anémie,
- le labo ne montre pas la présence de parasites dans le sang.
Infections à répétition :
Complications : taux de mortalité élevé, prolifération des lymphocytes avec apparition d'un syndrome lymphoprolifératif malin susceptible de se développer chez les individus présentant une résistance au traitement antipaludique
Des défenses pour l'hôte
Immunité
Après plusieurs années d'infections répétées, l'hôte du Plasmodium peut acquérir une immunité, appelée prémunition (symptômes atténués d'une maladie qui protège contre une infection ultérieure de type sévère). On constate une grande variabilité des réponses à l'infection palustre entre des individus vivant dans les mêmes zones d'endémie. Dans des régions où la transmission est forte, une grande proportion des enfants sont souvent porteur de parasites de P. falciparum sans déclarer aucun symptôme ; c'est l'immunité clinique. Avec l'âge et les contacts successifs être humain/parasite s'installe peu à peu cette prémunition, qui fait appel à des mécanismes de résistance à l'infection parmi lesquels les protéines « interférons » métabolisées et excrétées, entre autres, par le foie jouent un rôle majeur dans l'immunité anti-parasite. On parlera, alors, de tolérance à l'infection ou d'immunité anti-parasite. Une hypothèse est que le Plasmodium a besoin de fer pour se développer ; le déficit en fer dû à une première infection apporterait une protection relative et éviterait une « superinfection »[116].
On dit souvent que cette immunité n'est pas stérilisante car il n'a jamais été démontré de façon formelle de disparition totale des parasites de P. falciparum en l'absence de traitement. On dit aussi que cette immunité est labile car la prémunition disparait en l'absence de contacts fréquents entre l'être humain et le parasite (elle disparait après 12 à 24 mois si le sujet quitte la zone d'endémie) ainsi que chez la femme enceinte.
Par ailleurs, l'immunité dirigée contre P. falciparum est fortement spécifique de la ou des souches[117] parasitaires présentes.
Ces particularités de la réponse immunitaire contre le paludisme sont à l'origine des difficultés pour élaborer un vaccin.
Facteurs génétiques
Des facteurs génétiques peuvent protéger contre le paludisme. La majeure partie de ceux qui ont été décrits sont associés aux globules rouges. En voici quelques exemples :
 Hématies d'un drépanocytaire au microscope électronique
Hématies d'un drépanocytaire au microscope électronique
- La drépanocytose (du grec drepanos, « faucille » au regard de la forme allongée qu'ont un certain nombre d'hématies -ou globules rouges) aussi appelée hémoglobinose S, sicklémie, ou anémie falciforme : une modification dans la chaîne ß de l'hémoglobine entraîne une déformation des globules rouges, ce qui produit des hétérozygotes qui protègent mieux contre le paludisme. Les hématies sont déformées et l'hémoglobine cristallise, ce qui empêche le parasite de rentrer dans l'hématie. Ce changement entraîne cependant une mauvaise oxygénation des organes (les hématies allongées ne peuvent passer dans les fins capillaires ni la barrière que constitue le filtre de la rate où elles sont détruites) et, donc, de sévères complications, allant jusqu'au décès pour les sujets homozygotes (HbS/HbS). La prévalence de la drépanocytose (HbA/HbS) est élevée dans les populations africaines soumises a une forte pression du paludisme en raison de la résistance qu'elle procure contre les accès graves de la maladie.
- La thalassémie ou anémie héréditaire : le sujet est porteur du gène SS entraînant une modification des taux de synthèse des chaînes de globines avec pour conséquence une mauvaise circulation du sang et une fatigue constante.
- Le déficit génétique en G6PD (Glucose-6-phosphate déshydrogénase) appelé aussi favisme, qui est une enzyme antioxydante protégeant normalement contre les effets du stress oxydatif dans les globules rouges, donne une protection accrue contre le paludisme grave.
- Le HLA-B53 est associée à un faible risque de paludisme grave. Cette molécule CMH (complexe majeur d'histocompatibilité) de classe I présente dans le foie est un antigène des lymphocytes T (car situées dans le thymus) contre le stade sporozoïte. Cet antigène, encodé par IL4 (Interleukin-4), produit par les cellules T (thymus), favorise la prolifération et la différenciation de la production d'anticorps-cellules B. Une étude des Peuls du Burkina Faso, qui ont moins de deux attaques de paludisme avec des niveaux plus élevés d'anticorps antipaludiques que les groupes ethniques voisins, a constaté que l' allèle IL4-524 T était associé à des niveaux élevés d'anticorps contre le paludisme, ce qui soulève la possibilité que ce pourrait être un facteur d'augmentation de la résistance au paludisme.
- Les sujets dont les érythrocytes sont dépourvus de certains antigènes des groupes sanguins comme les sujets FY(-1,-2,-3,-6) dans la classification des systèmes immunogènes FY (anciennement système Duffy), ne peuvent être contaminés par P. vivax ni par P. knowlesi (de découverte récente et apparenté à P. malariae). Il s'agit là d'un exemple d'avantage sélectif de la population ouest-africaine, où ce groupe sanguin est très fréquent. Cependant, ce dogme pourrait être revu, P. vivax ayant réussi à s'adapter à Madagascar suite au brassage génétique entre population africaine et asiatique[118].
D'autres facteurs génétiques existent dont certains sont impliqués dans le contrôle de la réponse immunitaire[119].
Traitements
Dans les zones endémiques, les traitements sont souvent peu satisfaisants et le taux de mortalité global pour tous les cas de paludisme peut atteindre un sur dix[120][réf. souhaitée]. L'utilisation massive de thérapies dépassées[121], de faux médicaments et la mauvaise anamnèse des symptômes sont responsables du mauvais bilan clinique.
Anciens traitements
L'endoparasite peut être combattu par différentes molécules soit en traitements curatifs soit en prophylaxie. Ces différentes thérapies sont plus ou moins efficaces suivant les régions et les taux de résistances acquis car, tout comme le DDT (insecticide le plus utilisé dans les années 1960), les médicaments efficaces il y a 30 ans, comme la chloroquine, ne le sont plus aujourd'hui.
Pourtant, ces formulations obsolètes sont encore massivement utilisées dans les pays touchés[122]. Faisant partie du tiers monde, ils n'ont pas les moyens de migrer leur protocole de soins vers un outil plus onéreux comme l'utilisation des ACT (Artemisinin-based combination therapy). Pendant longtemps, les traitements faisaient appel à la chloroquine, la quinine et la SP (sulfadoxine-pyriméthamine) et dans une moindre mesure la méfloquine, l'amodiaquine et la doxycycline. Ces molécules furent des armes très efficaces pour lutter contre les parasites du paludisme mais leur prescription sans contrôle a favorisé l'émergence de souches résistantes. Selon l'OMS, un traitement est efficace si le taux d'échec est inférieur à 5 % ; s'il dépasse 25 %, il faut changer de protocole.
La chloroquine, qui fut le premier anti-malarique de synthèse, a longtemps été administrée en priorité pour soigner les patients. Le parasite en se nourrissant de l'hémoglobine divise celle-ci en acides aminés produisant de la ferritine, toxique pour lui, qu'il transforme et stocke, dans sa vacuole digestive, sous forme de cristal inerte. La chloroquine, en pénétrant la cellule infectée, stoppe la transformation protectrice de la ferritine en cristal inerte faisant accumuler ce fer toxique. Le parasite est, ainsi, tué par ses propres déchets.
C'était un médicament qui présentait de nombreux avantages, notamment son faible coût et l'absence d'effets secondaires. Aujourd'hui, les soins à base de chloroquine échouent à plus de 25 % dans les pays d'Afrique subsaharienne touchés par le paludisme. Or, ils sont toujours employés.
Cette résistance est due à l'allèle mutant PfCRT (Plasmodium falciparum Chloroquine Resistance Transporter) K76T[123]. Cette mutation draine la chloroquine hors de la cellule infectée mais entraînerait toutefois une moins bonne adaptation du parasite à son milieu[124]. Le Malawi est le premier pays africain à avoir abandonné la chloroquine dès 1993, conduisant à une réapparition des souches sensibles qui redeviennent alors hautement majoritaires[125].
Là où la chloroquine n'a plus d'effet, on utilise un médicament appelé « médicament de deuxième intention » : la SP (comme le Fansidar® produit par Roche). Cette molécule contourne la résistance à la chloroquine. Cinq ans seulement ont suffi pour que des souches résistantes apparaissent. On adapte alors le traitement en recourant à un « médicament de 3e intention » : la quinine, administrée per os dans les cas bénins ou par perfusion dans les cas aigus. Mais, ces traitements sont aussi confrontés à de nouvelles résistances de la part du parasite.
ACT
Face au paludisme, il n'existe, en 2006[126], qu'un seul traitement véritablement efficace : les ACT (Artemisinin-based combination therapy : combinaisons à base d'artémisinine) tous obligatoirement génériques. Un traitement recommandé par l'OMS mais qui reste encore cher. Bien que des résistances de Plasmodium falciparum à l'artémisinine ont pu être produites en laboratoire[127], démontrant ainsi la possibilité d'une telle complication, à l'état naturel aucune résistance n'est pour l'instant répertoriée en trithérapie associant le SP (sulfadoxine-pyriméthamine). Le principal inconvénient reste son prix, qui le rend inaccessible pour de nombreux pays en voie de développement.
L'OMS et le groupe pharmaceutique Novartis, fabricant de l'artéméther (dérivé semi-synthétique de l'artémisinine)-luméfantrine (molécule synthétique antimalarique) commercialisé sous le nom de Co-artem®, ont conclu un accord au terme duquel Novartis fournit le médicament au prix de revient (0,9 et 2,4 USD pour les traitements enfant et adulte respectivement). C'est un comprimé jaune rond et plat, aux bords chanfreinés et muni d'une barre de cassure sur une face. "N/C" est gravé sur une face et "CG" sur l'autre. Lors de la prise, il est conseillé de consommer une boisson forte en lipides (lait) et de continuer à s'alimenter pour faciliter l'absorption de la luméfantrine. Pour un sujet dont le poids est supérieur ou égal à 35 kg, une première prise de 4 comprimés immédiatement après le diagnostic, une seconde à + 8h, puis 4 comprimés 2 fois par jour pendant les 2 jours suivants. A noter que le Co-artem® est commercialisé sous le nom de Riamet® dans les pays développés. Seul le prix change (38,05 EUR la boîte de 12 comprimés - prix 2009 en Belgique).
D'autres initiatives comme la DNDi (Drugs for Neglected Diseases initiative) créée par MSF et le groupe Sanofi-Aventis ont vu le jour pour aboutir à la fabrication de l'Asaq®[128] à base d'artésunate et d'amodiaquine. La dose fixe coûte moins de 38 centimes d'euro pour les enfants de moins de 5 ans et moins de 77 centimes d'euros pour les adolescents et les adultes.
De nouveaux ACT arrivent sur le marché : dihydroartémésinine-pipéraquine commercialisé sous le nom de Eurartekin® ou Duocotexin® et l'artémésinine-pipératique commercialisé sous le nom de Artequick®.
L'artémisinine (qing hao su 青蒿素 en chinois), issue d'Artemisia annua une plante d'origine chinoise (qing hao (青蒿) en chinois), a largement prouvé son efficacité en Asie. Des études menées en laboratoire et dans de nombreux pays impaludés démontrent à la fois son efficacité et sa facilité d'administration. Elle élimine plus rapidement les parasites présents dans le sang.
La prescription d'artémisinine, sous forme d'infusions issues d'armoise annuelle (Artemisia annua) peut s'avérer très efficace.
Pour augmenter son effet, mais aussi retarder l'apparition de résistances, l'artémisinine est donc administrée en association avec une autre molécule, SP (sulfadoxine-pyriméthamine), amodiaquine ou méfloquine : ce sont les ACT (de l'anglais, artemisinin-based combination therapy), combinaisons thérapeutiques associant l'artémisinine à d'autres antipaludiques d'une classe thérapeutique différente. La faible parasitémie résistante à l'artémisinine est éliminée par le deuxième antipaludéen d'action plus durable. Dans les schémas thérapeutiques avec une prescription d'ACT pendant 3 jours, le composé d'artémisinine n'est présent dans l'organisme que durant deux cycles asexués de l'hématozoaire (autre nom donné au protozoaire) (chaque cycle durant 2 jours, sauf pour les infestations à P.malariae qui dure 3 jours). Cette exposition à 3 jours de traitement par l'artémisinine réduit le nombre de plasmodies (nom donné au protozoaire du Plasmodium) présentes dans l'organisme d'un facteur approximativement égal à 100 millions. Toutefois, l'élimination complète des plasmodies repose sur l'efficacité de la SP associée, qui doit persister à des concentrations parasiticides jusqu'à ce que tous les hématozoaires infestants aient été tués. Ainsi, ceux-ci doivent être éliminés relativement lentement. Le résultat est que le composé d'artémisinine est « protégé » de la résistance par le médicament qui l'accompagne pour autant que ce dernier soit efficace, et ce médicament d'accompagnement est lui-même partiellement protégé par le dérivé de l'artémisinine. Les schémas thérapeutiques d'ACT d'un ou deux jours ne sont pas recommandées ; ils sont moins efficaces et confèrent une protection moindre pour l'antipaludique s'éliminant lentement.
En 2002, l'OMS a publié une recommandation claire sur la nécessité d'utiliser les ACT dans les pays touchés par les résistances aux antipaludéens classiques. Sur l'avis d'experts internationaux, elle recommande l'introduction de polythérapies pour remplacer les monothérapies dans le traitement du paludisme et préconise en particulier le recours à des associations médicamenteuses contenant des dérivés d'artémisinine. Une mise à jour de ses recommandations a été éditée en mai 2010[129].
Cependant, une monothérapie (à base d'artémisinine, d'artésunate ou d'arthéméther ainsi que leur métabolite commun : la dihydroartémisinine) administrée sous forme de Rectocap™ [130] (artésunate en gel enrobé de gélatine pour former un suppositoire résistant aux manipulations et à la chaleur) de 200 mg. peut s'avérer particulièrement utile quand les patients sont incapables d'ingérer (vomissements répétés, impossibilité de manger/boire/téter, convulsions récurrentes, absence de réactions à la douleur, coma, absence de réactions psychomotrices) ou quand les présentations injectables ne sont pas disponibles ou qu'elles sont impossibles à administrer. Cette monothérapie (monodose (minimum 8,5 mg/kg) de 10 mg/kg est ce qui le plus communément conseillé) induit une réaction parasitaire dans les 12 heures et est supérieure à la quinine dans les 24 heures. Elle doit impérativement être suivie, dès que possible, par un traitement avec une association médicamenteuse d'ACT. A noter, aussi, que l'utilisation d'une capsule rectale est préférable à une injection intra-musculaire. N'importe qui est capable de l'appliquer, il n'y a aucun risque d'infection par l'aiguille et la durée de réponse du produit est plus rapide.
Produit en assez faibles quantités, les ACT sont plus chers que la chloroquine. Un traitement de première ligne chloroquine ou SP coûte actuellement entre 0,2 et 0,5 USD, alors qu'un traitement ACT oscille entre 1,2 et 2,4 USD, soit cinq à six fois plus. Pour de nombreux patients, cette différence est le prix de leur survie. Un prix que bien peu de personnes en Afrique peuvent payer. Seule une fabrication à plus grande échelle et, ou une aide financière plus importante des pays riches pourrait faire significativement baisser les coûts de production.
Faux médicaments
De faux médicaments supposément anti-paludéens circulent en Thaïlande, au Viêt Nam, au Cambodge[131] et en Chine[132] ; ils forment une cause importante de la mortalité, qui serait pourtant évitable[133]. En août 2007, la société pharmaceutique chinoise Holley-Cotec a été obligée de retirer 20 000 doses de son médicament à base d'artémisinine DUO-COTECXIN®[134] au Kenya parce que des contrefaçons, en provenance d'Asie, contenant très peu d'ingrédients actifs et incapables d'une quelconque thérapie circulaient sur le marché à un prix 5 fois moindre. Il n'existe pas de moyen simple pour les médecins comme pour les patients de distinguer un vrai médicament d'un faux, sans l'aide d'un laboratoire. Les compagnies pharmaceutiques tentent de combattre les faux médicaments en utilisant de nouvelles technologies sécurisant le produit de la source à sa distribution.
Prévention
Les méthodes utilisées pour empêcher la maladie de se répandre, ou pour protéger les habitants des zones endémiques, incluent la prophylaxie par la prise de médicaments, l'éradication des moustiques et la prévention des piqûres de moustiques. Pour que le paludisme puisse exister de façon continue à un endroit, il faut une combinaison de facteurs : forte densité de population, fort taux de transmission des humains aux moustiques et réciproquement. Si un de ces facteurs diminue, le parasite finit par disparaitre, comme en Amérique du Nord et en Europe. Inversement, le parasite peut être réintroduit dans une région et y survivre si ces facteurs y sont réunis.
Il n'existe pas de vaccin à l'heure actuelle contre le paludisme, mais la recherche d'un vaccin est un secteur très actif.
Certains chercheurs affirment que la prévention du paludisme serait plus efficace financièrement que son traitement à long terme ; mais les frais à engager pour cela sont trop importants pour les plus pauvres. L'économiste Jeffrey Sachs estime ainsi que le paludisme pourrait être contrôlé avec 3 milliards de dollars US par an. Afin d'atteindre les objectifs du millénaire pour le développement, l'argent actuellement alloué à la lutte contre le Sida devrait être réaffecté à la prévention du paludisme, ce qui bénéficierait davantage à l'économie africaine[135].
Certains pays comme le Brésil, l'Érythrée, l'Inde ou le Viêt Nam ont réussi à réduire le fléau du paludisme. L'analyse de ces programmes montre que de nombreux facteurs ont dû être réunis pour lutter avec succès contre la maladie, qu'il s'agisse des financements, de l'action de l'État et des ONG, ou de l'action concrète des travailleurs sociaux[136].
Moyens de combattre le moustique ou de s'en protéger
On peut combattre le vecteur du paludisme (l'anophèle femelle) par plusieurs moyens de prévention, qui peuvent s'avérer efficaces s'ils sont bien mis en œuvre.
Le véritable problème de cette prévention est le coût très élevé des traitements pour les populations touchées. En effet, elle peut être efficace chez les voyageurs, mais les pays en voie de développement, qui sont les principales victimes de cette maladie, peinent à organiser des actions très efficaces. On peut donner pour preuve l'exemple de l'île de la Réunion où le paludisme sévissait comme dans les autres îles de la région (Madagascar et île Maurice) notamment. La Réunion étant un territoire français d'outre-mer, le problème du coût trop élevé n'existait pas et on a pu éradiquer la malaria de cette île sans difficulté.
Deux modes de prévention sont appliqués dans les pays concernés. Ils visent d'une part à protéger les populations contre les piqûres de moustiques et, d'autre part, à éliminer ces derniers par la mise en place de moyens divers. Le but principal de cette prophylaxie est de limiter la population de moustiques vecteurs de la maladie et ainsi de tenter d'éradiquer ce fléau.
Dans les années 1960, la principale méthode utilisée pour éradiquer les anophèles femelles était l'utilisation massive d'insecticides. Le plus utilisé était le DDT (Dichloro-Diphényl-Trichloréthane). Cette méthode porta ses fruits dans de nombreuses régions où le paludisme fut totalement éradiqué. L'utilisation intensive du DDT a favorisé la sélection de moustiques résistants. Cette résistance a été nommée KDR (Knock Down Resistance : résistance à l'effet de choc). En outre, il peut engendrer intoxications et maladies dans la population comme ce fut le cas en Inde où il fut utilisé de manière abusive en agriculture. Bien que ce produit soit totalement interdit en Europe depuis 1972 et que, depuis 1992, il est classé par l'OMS comme POP (polluant organique persistant), cette même OMS semble revenir sur sa position en prônant de nouvelles recommandations concernant l'utilisation de ce pesticide (usage exclusif destiné à la lutte contre le paludisme à l'intérieur des bâtiments)[137]. Et pourtant, incontestablement, le DDT est :
- persistant : sa demi-vie est de 15 ans, c'est-à-dire que si l'on pulvérise 10 kg dans un champ, 15 ans après, il en restera 5 kg, après 30 ans 2,5 kg et ainsi de suite ;
- dispersif : on en a retrouvé dans les neiges de l'Arctique ;
- bio cumulatif : les animaux qui en absorbent n'en meurent pas, mais ne parviennent pas à l'éliminer. Ils le stockent dans leurs graisses et on en retrouve de grandes concentrations chez les animaux du sommet de la chaîne alimentaire. Par contre, sa toxicité est sujette à débat bien qu'une ingestion de 35 g peut être létale pour une personne de 70 kg.
Pour remplacer le DDT, qui s'avère dangereux et de moins en moins efficace, des moyens alternatifs sont possibles afin de combattre le vecteur du paludisme[138] :
- assèchement des marais (sans bouleverser le système écologique), drainage des eaux stagnantes où se développent les larves des anophèles (un vieux pneu abandonné et rempli d'eau par les pluies est suffisant au moustique pour y pondre ses œufs) ;
- lutte anti-larvaire par épandage de pétrole ou d'huile végétale et utilisation d'insecticides solubles répandus à la surface des eaux stagnantes, pour tenter de limiter les naissances d'anophèles ou empêcher les larves de venir respirer à la surface. Mesures fort peu recommandables car totalement anti-écologiques ;
- ensemencement des eaux avec des prédateurs des anophèles ou de leurs larves comme certains mollusques ou poissons (tilapias, guppys, gambusies, aphanius)[139] ;
- réintroduction, et protection, des variétés de chiroptères insectivores là où elles ont disparu (une chauve-souris peut avaler près de la moitié de son poids en insectes en une nuit)[140] ;
- ciblés à partir du séquençage du génome du moustique[141]. Ce génome offre, entre autres, un catalogue de l'accroissement des gènes de détoxification et des gènes mutants qui codent les protéines visées par les insecticides ainsi que les variations des nucléotides individuels, appelés polymorphismes nucléotidiques qui se trouvent dans le génome :
- emploi d'insectifuges et d'insecticides ciblés uniquement contre l'anophèle ;
- dispersion de mâles anophèles stériles dans la nature ;
- interventions génétiques sur les espèces vectrices ou, dans un avenir indéterminé, avec des vaccins bloquant la transmission en induisant des anticorps empêchant la maturation des stades sexués du parasite chez l'anophèle.
Ces mesures ne sont efficaces que sur un territoire limité. Il est très difficile de les appliquer à l'échelle d'un continent tel que l'Afrique.
Chacun, à titre individuel, peut éviter les piqûres d'anophèles par des mesures mécaniques, physiques et chimiques : rappelons avant tout que l'anophèle a une activité nocturne, commençant à piquer à la tombée de la nuit, et se reposant la journée dans les habitations.
- installation de moustiquaires (mailles inférieures à 1,5 mm) imprégnés de perméthrine ou de dérivés de pyréthrinoïde. De plus en plus ces moustiquaires sont fournis à prix très démocratiques (maximum 1,70 USD) voire gratuitement aux populations des zones d'endémie. Ces moustiquaires sont efficaces pendant 3 à 5 ans selon le modèle et les conditions d'utilisation ;
- installation de grillage moustiquaire aux fenêtres ;
- utilisation d'insecticides à petite échelle : pulvérisation d'insecticides intradomicilaires (pyréthrinoïdes, DDT, ...) dans les habitations (chambres à coucher) ;
- installation d'air conditionné dans les habitations pour faire baisser la température et brasser l'air (le moustique a horreur des déplacements d'air qui le perturbent dans ses déplacements et dans sa faculté sensorielle à trouver sa cible) ;
- après le coucher du soleil : port de vêtements amples, longs et de couleur claire et abstinence d'alcool (les anophèles sont aussi bien attirés par les couleurs foncées, plus spécialement le noir, que par les vapeurs d'alcool) ;
- application de crème répulsive sur la peau ou les vêtements dès le coucher du soleil. De tous les répulsifs de synthèse, ceux qui contiennent du DEET (N, N-diethyl-m-toluamide) sont les plus efficients. Le DEET ne tue pas les insectes mais ses vapeurs les découragent de se poser ou de grimper sur la personne.
Généralement, les produits concentrés entre 25 et 30 % de DEET sont les plus efficaces sur la plus longue période (± 8 h contre les insectes rampants et de 3 à 5 h contre les anophèles). Ils sont également considérés comme inoffensifs pour des personnes adultes ou des enfants de plus de 2 ans si la concentration ne dépasse pas 10 % pour ces derniers. À proscrire chez la femme enceinte et le nourrisson de moins de 3 mois. Les produits concentrés à plus de 30 % ne sont plus homologués.
Les produits commercialisés sont à appliquer à même la peau ou sur les vêtements ou les moustiquaires. Attention cependant à ce qu'ils altèrent les matières plastiques, certains tissus synthétiques comme le nylon, le caoutchouc, le cuir et les surfaces peintes ou vernies. Prendre également attention aux yeux et à l'inhalation directe avec les produits en atomiseur ainsi qu'à l'ingestion. Les applicateurs munis d'une bille seront donc préférés.
La résorption transcutanée est de 50 % en 6 h et l'élimination sera urinaire. La partie non éliminée (30 %) sera stockée dans la peau et les graisses.
Répulsifs
Les études ont montré que les produits répulsifs à base d'eucalyptus qui contiennent de l'huile naturelle d'eucalyptol sont une alternative efficace et non-toxique au DEET. En outre, les plantes telles que la citronelle ont prouvé leur efficacité contre les moustiques. Une étude ethnobotanique[142] conduite dans la région du Kilimandjaro (Tanzanie) montre que les répulsifs les plus largement utilisés, par les populations locales, sont des lamiacées du genre ocimée l' Ocimum kilimandscharicum et lOcimum suave. L'étude portant sur l'utilisation d'huiles essentielles extraites de ces ocimées montre que la protection vis-à-vis des piqûres de certains anophèles vecteurs du paludisme augmente dans 83 à 91 % des cas et inhibe, chez l'insecte, son envie de succion dans 71,2 à 92,5 % des cas.
L'icaridin aussi connu sous le nom de KBR 3023 est un nouveau répulsif de la famille chimique des pipéridines et de force comparable au DEET, mais il est moins irritant et ne dissout pas les plastiques. Il a été développé par la société chimique allemande Bayer AG et commercialisé sous le nom de SALTIDIN®[143]. La forme en gel avec 20 % de produit actif est actuellement la meilleure. Attention, malgré tout, tous les effets secondaires possibles vis-à-vis des enfants ne sont pas encore tous connus.
Un essai de divers répulsifs, lancés sur le marché, par une organisation indépendante du consommateur a constaté que les produits répulsifs synthétiques, y compris DEET, étaient plus efficaces que des produits répulsifs avec les substances actives de naturelles.
- utilisation de perméthrine ((3-phenoxyphenyl)methyl) ou de dérivés de pyréthrinoïde. Ce sont des révulsifs mais peuvent aussi être classés parmi les insecticides. S'ils repoussent et irritent le moustique, ils créent, sur celui-ci, une action de choc (Knock Down) qui le tue ou le neutralise directement.
Ne pas utiliser directement sur la peau mais imprégner les vêtements ou les moustiquaires en prenant garde de ne pas irriter les muqueuses nasales ni d'en ingérer lors de la manipulation. La durée d'efficacité est d'environ 6 mois (moins sur les vêtements qui subissent frottements, pluie, etc…). La réimprégnation se fait après lavage au savon.
Précaution : Ne pas porter des vêtements imprégnés de perméthrine sur la peau déjà traitée au DEET.
Femmes enceintes
Le dernier moyen mis en application est beaucoup plus ciblé. En effet il ne s'applique qu'aux femmes enceintes, et il a pour but d'éviter une grossesse émaillée de problèmes dus à des contractions prématurées et de permettre aux nourrissons de naître en bonne santé et non avec un poids trop faible (surtout s'il s'agit d'un primipare) ou encore atteint de nombreuses maladies comme le paludisme placentaire (l'infection congénitale, ou non, est en relation directe avec le nombre de parasites dans le placenta), l'anémie grave et la malformation du bébé.
Afin de prévenir et d'empêcher de graves complications, une prise en charge globale qui comporte une prévention de l'infection palustre et la protection sanitaire a été mise en place. Ces actions ont pour but de limiter les infections et leurs conséquences pouvant être très graves pour l'enfant et pour la mère. Il s'agit notamment du recours aux moustiquaires imprégnées d'insecticide et de l'utilisation d'antipaludéens, soit à titre prophylactique primaire, soit comme traitement intermittent. L'administration aux femmes enceintes de quantités supérieures à la normale journalière de multivitamines (B, C et E) ainsi que du fer et de l'acide folique (selon l'OMS, l'UNICEF et d'après les recherches de l'université Johns-Hopkins) pourrait constituer une protection efficace[144]. Une étude précédemment menée montre que la vitamine A serait néfaste et que le zinc n'apporte aucun bénéfice hormis qu'il aide à éviter les diarrhées.
Par contre, il a été, non seulement, prouvé que le traitement intermittent des femmes enceintes par l'association médicamenteuse de SP (sulphadoxine-pyriméthamine) une fois pendant le deuxième trimestre et une seconde fois pendant le troisième trimestre réduisait le risque d'anémie chez la mère, de parasitémie placentaire et d'insuffisance pondérale à la naissance mais aussi que le traitement systématique par la SP des nourrissons aux âges de 2, 3 et 9 mois, lors des vaccinations, réduisait de 60 % les épisodes de paludisme clinique et de 50 % les épisodes d'anémie pernicieuse.
Il a été prouvé que dans les zones d'endémies, une prévention efficace du paludisme pendant la grossesse permet de réduire l'incidence d'anomalies comme un faible poids à la naissance ou une anémie maternelle grave (diminution de la concentration en hémoglobine du sang - en dessous de 0,13 g/ml chez l'homme et de 0,12 g/ml chez la femme).
L'application de ces quelques règles suffirait à faire baisser considérablement le nombre de personnes touchées par cette maladie et ainsi le nombre de victimes, mais le manque de moyens entrave leur application. De nombreux habitants n'ont même pas les moyens de se procurer des moustiquaires, susceptibles de réduire les risques d'infections.
Prophylaxie
Afin de prévenir toute contamination chez les touristes se rendant dans des pays où sévit le paludisme, les chercheurs ont mis en place une technique prophylactique. Cette technique consiste à utiliser un arsenal thérapeutique de médicaments préventifs (se limitant à la chloroquine, au proguanil, à l'association pyriméthamine-dapsone, à l'association proguanil-atovaquone, à l'association chloroquine-proguanil chlorhydrate, à la méfloquine et la doxycycline) afin d'éviter l'infection en cas de pénétration du parasite dans l'organisme.
Il est très dangereux de partir en zone de transmission intense de paludisme sans prise régulière d'un traitement préventif, en particulier pour les enfants et les femmes enceintes qui ont un risque accru d'accès de paludisme grave.
Mais en raison de l'accroissement de la pharmacorésistance parasitaire (résistance des parasites aux produits constituant l'arsenal thérapeutique) et des effets secondaires propres aux différents produits, il est de plus en plus difficile d'établir des directives chimioprophylactiques (recherche de médicament de façon rationnelle). Le touriste doit, avant de s'aventurer dans des pays touchés par ce fléau, consulter son médecin généraliste ou le médecin d'un centre de médecine du voyage qui lui indiquera les contre-indications éventuelles des antipaludéens. Et pour qu'il n'y ait aucune disparité, il serait souhaitable de voir apparaître une harmonisation des directives chimioprophylactiques nationales et internationales.
Les médicaments antipaludéens ne garantissent pas une protection absolue contre l'infection et il est aussi important de se protéger des piqûres de moustiques (moustiquaires, produits antimoustiques) car même si un traitement adapté a été correctement suivi, il est possible de faire une crise de paludisme, parfois d'apparition tardive à cause de la forme hypnozoïte que peut prendre le Plasmodium.
En Belgique, des cas de décès dus à la malaria surviennent, chaque année, chez les voyageurs de retour au pays[145].
Cas particulier de la France
Selon un rapport[Lequel ?] français du Centre national de référence pour l'épidémiologie du paludisme d'importation et autochtone, fondé sur une étude auprès des 8 000 Français ayant contracté la maladie en l'an 2000, près de la moitié n'avait eu recours à aucune prophylaxie.
En 2002, seuls 10 % des voyageurs français en déplacement dans une zone à risque ont suivi un schéma thérapeutique correct. En 1990, ce pourcentage était d'un tiers : cela explique, en partie, la forte recrudescence des cas de paludisme d'importation (environ 5 000 cas en 1999 et 7 000 en 2000 rapportés par l'Institut de veille sanitaire). la France est un cas atypique en Europe alors, que partout ailleurs, la contamination est stable ou en régression[réf. nécessaire].
Schémas prophylactiques antipaludéens
Au 9 mars 2006, la prévention du risque paludéen s'organise en trois niveaux, classés selon le niveau de chimio-résistance. Chaque pays à risque se trouvant ainsi classé dans un groupe. Bien avant de partir en voyage, il convient de demander l'avis de son médecin car ces traitements sont généralement à commencer à l'avance.
- Pays du groupe 0
- Zones sans paludisme : Pas de chimioprophylaxie.
-
- Afrique : le Lesotho, la Libye, le Maroc, La Réunion, l'île Sainte-Hélène, les Seychelles et la Tunisie ;
- Amérique : toutes les villes, Antigua-et-Barbuda, les Antilles néerlandaises, les Bahamas, la Barbade, les Bermudes, le Canada, le Chili, Cuba, la Dominique, les États-Unis, la Grenade, les îles Caïmans, les îles Malouines, les îles Vierges, la Jamaïque, la Martinique, Porto Rico, Sainte-Lucie, la Trinité-et-Tobago et l'Uruguay ;
- Asie : toutes les villes, Brunei, la Géorgie, Guam, Hong Kong, l'île Christmas, les îles Cook, le Japon, le Kazakhstan, le Kirghizistan, Macao, les Maldives, la Mongolie, le Turkménistan, Singapour et Taïwan ;
- Europe : tous les pays y compris l'Arménie, les Açores, les îles Canaries, Chypre, la Russie, les pays baltes, l'Ukraine, la Biélorussie et la Turquie d'Europe ;
- Proche et Moyen-Orient : toutes les villes, Bahreïn, Israël, la Jordanie, Koweït, le Liban et le Qatar ;
- Océanie : toutes les villes, l'Australie, les Fidji, Hawaii, les îles Mariannes, les Marshall, la Micronésie, la Nouvelle-Calédonie, la Nouvelle-Zélande, l'île de Pâques, la Polynésie française, les Samoa, les Tonga et les Tuvalu.
- Cas particulier des zones de transmission faible
- Compte tenu de la faiblesse de la transmission dans ces pays, il est admissible de ne pas prendre de chimioprophylaxie quelle que soit la durée du séjour. Il est cependant indispensable d'être en mesure, dans les mois qui suivent le retour, de consulter en urgence en cas de fièvre.
-
- Afrique : l'Algérie, le Cap-Vert, l'Égypte et Maurice ;
- Asie : l'Azerbaïdjan, la Corée du Nord, la Corée du Sud, et l'Ouzbékistan ;
- Proche et Moyen-Orient : les Émirats arabes unis, Oman, la Syrie et la Turquie.
- Pour tous les autres pays, il est nécessaire de prendre une chimioprophylaxie adaptée à la zone visitée.
- Pays du groupe 1
- Zones sans chloroquinorésistance : chloroquine 100 mg : un comprimé chaque jour (il est possible aussi de prendre 300 mg. deux fois par semaine) pour une personne pesant au moins 50 kg (à utiliser avec prudence chez les épileptiques et, chez tout un chacun, car pouvant provoquer des troubles de la vue voire la cécité avec des prises de trop longue durée).
- Pays du groupe 2
- Zones de chloroquinorésistance : chloroquine 100 mg, (un comprimé chaque jour) et proguanil 100 mg, (deux comprimés chaque jour).
- L'association chloroquine-proguanil, sera ingérée, au cours d'un repas, en une prise ou par demi dose matin et soir en débutant 1 semaine avant le départ et jusqu'à 1 mois après le retour pour une personne pesant au moins 50 kg (pour une personne de moins de 50 kg, se référer au chapitre sur l'enfant voyageur).
- L'association atovaquone-proguanil peut être conseillée en alternative à l'association chloroquine-proguanil (voir le paragraphe "Pays du groupe 3" pour plus de détail sur l'association atovaquone-proguanil).
- Pays du groupe 3
- Zones de prévalence élevée de chloroquinorésistance ou multirésistance[146]
La doxycycline[147] (principe actif)
- 1 comprimé de 100 mg. par jour, 1 jour avant le départ (prise doublée le 1er jour) et jusqu'à 28 jours après le retour ou après avoir quitté la zone d'endémie de malaria (à prendre en position assise avec une grande quantité de liquide ou pendant le repas). Les doses sont à diviser par deux pour les enfants de plus de huit ans.
- La doxycycline peut être prise pendant plusieurs mois mais peut provoquer une phototoxicité (réaction chimique provoquée par la présence trop grande de substance photoréactive dans la peau et réagissant sous l'action des rayons UV ou visibles) et des mycoses buccales et génitales ; elle est à proscrire aux femmes enceintes (troubles hépatiques) ou allaitantes ainsi que chez les enfants de moins de 8 ans (ralentissement réversible de la croissance osseuse et coloration jaune irréversible des dents avec un risque accru de caries)
- Il s'agit d'un dérivé de la tétracycline (antibiotique à 4 cycles accolés capable de pénétrer les cellules eucaryotes dont font partie le Plasmodium) parfois utilisé contre le paludisme en association avec la quinine pour des traitements d'urgence par voie intraveineuse.
La méfloquine comme le Lariam®[148] (Roche)
- Composition : 250 mg. méfloquine
- Boite de 8 comprimés - 34,26 EUR (Prix en Belgique en 2010)
- 1 comprimé par semaine, quelques semaines avant le départ et jusqu'à 4 semaines après le retour
- Pour obtenir une concentration dans le sang efficace de Lariam® dès l'arrivée, il est nécessaire d'initier le traitement 2 à 3 semaines avant le départ. Les personnes qui n'ont jamais pris ce produit auparavant doivent débuter le traitement 2-3 semaines avant le départ, pour déceler d'éventuels effets secondaires (vertige, insomnie, cauchemar, excitation, angoisse inexplicable, palpitations). Il ne sera pas prescrit si le médecin juge qu'il existe une contre-indication (souhait de grossesse, premier trimestre de grossesse, épilepsie, dépression, ou troubles du rythme pour lesquels un traitement est en cours avec des médicaments tels que des bêta-bloquants, des antagonistes calciques, ou de la digitaline), ou s'il n'a pas été supporté dans le passé. Il faut poursuivre le traitement jusqu'à 4 semaines après le retour. Si le Lariam® est bien supporté, il peut être pris pendant des mois voire des années si nécessaire.
- Pour les séjours prolongés (durée supérieure à 3 mois), la chimioprophylaxie doit être maintenue aussi longtemps que possible et il est recommandé aux voyageurs de prendre rapidement contact avec un médecin sur place pour évaluer la pertinence et le rapport bénéfice/risque de la chimioprophylaxie.
L'association atovaquone-proguanil comme le Malarone®[149] (GlaxoSmithKline) peut être conseillée en alternative à la méfloquine.
- Composition pour adulte : 250 mg. atovaquone + 100 mg. proguanil chlorhydrate
- Boite de 12 comprimés - 43,31 EUR (prix en Belgique en 2010)
- Composition pour junior : 62,5 mg. atovaquone + 25 mg. proguanil chlorhydrate
- Boite de 12 comprimés - 18,48 EUR (prix en Belgique en 2010)
- 1 comprimé par jour, 1 jour avant le départ et jusqu'à 7 jours après le retour.
- Si la première prise ne débute que durant le séjour, il convient de le prendre jusqu'à 4 semaines après le retour.
- Pour un voyage de courte durée, la prise de Malarone®, habituellement très bien toléré, est un excellent choix. Elle peut être utilisée pendant plusieurs mois (mais il faudra alors prendre en compte son coût élevé). La durée d'administration continue de l'atovaquone-proguanil dans cette indication devra, cependant, être limitée à 3 mois, faute de disposer à ce jour d'un recul suffisant en traitement prolongé.
En tout état de cause, l'avis d'un médecin est plus que souhaitable avant toute médication.
Gestion des stocks de médicaments
Une technologie utilisant le SMS vient d'être testée avec succès en Tanzanie.
Cette opération appelée SMS for Life consiste à éviter les ruptures de stocks en médicaments contre le paludisme, le Sida et la tuberculose dans un endroit donné, même le plus reculé, par l'interaction entre un serveur informatique et des téléphones mobiles[150]
Avenir
Les recherches tant en pharmacologie pour les traitements (cf. section détaillée « Le futur - La pharmacologie ») qu'en vaccination pour la prophylaxie (cf. section détaillée « Le futur - Les vaccins ») vont à un rythme de plus en plus accéléré grâce à des sponsors comme le Malaria Vaccine Initiative ou des ONG comme MSF.
Précautions à prendre
La prise de médicaments antipaludéens, même en respectant un schéma thérapeutique correct, ne suffit pas à protéger à 100 % contre le risque de paludisme. Il faut aussi se protéger des moustiques, les empêcher de rentrer en contact avec leurs victimes, afin d'éviter la piqûre de l'insecte.
- Éviter les déplacements en zone à risque sans protection, toujours dormir avec une moustiquaire dont les mailles sont inférieures à 1,5 mm, même à la belle étoile ;
- Porter des vêtements longs, amples et de couleur claire, serrés aux poignets et aux chevilles, avec des chaussures fermées, imprégnées de répulsif (attention, le moustique anophèle vole souvent au raz du sol et peut piquer à travers les chaussettes) ;
- Appliquer des répulsifs cutanés sur toutes les parties non couvertes du corps (à base de DEET mais à éviter pour les nourrissons de moins de 3 mois et les femmes enceintes ou allaitantes) ;
- Utiliser des insecticides, à l'intérieur, mais aussi à l'extérieur ;
- Dormir avec l'air conditionné ou sous une moustiquaire (de préférence imprégné d'insecticide lorsque le corps, la nuit, peut être en contact avec cette moustiquaire) : l'homme agit ainsi comme un appât et outre la barrière mécanique de la moustiquaire empêchant la piqûre, elle provoque la mort du moustique qui est entré au contact de l'insecticide;
- Protéger toutes les ouvertures par des moustiquaires appropriées.
L'utilisation de produits répulsifs ou anti-insectes (tels le DEET ou le DDT) et de moustiquaires réduit les risques d'infection, mais une chimioprophylaxie reste indispensable (Nivaquine, Savarine, LARIAM®, MALARONE®). Il est déconseillé de boire de l'alcool en ayant pris ces médicaments.
Conséquences économiques
Selon la Ligue contre le paludisme, une famille touchée ne récolterait que 40 % de sa production agricole, du fait des journées de travail perdues. L'OMS a même calculé que le PIB africain dépasserait de 115 milliards d'euros son niveau actuel, soit 32 % supplémentaires, si l'on avait éliminé le paludisme il y a 35 ans.
Sur le plan de la lutte, l'UNICEF estime que le coût moyen annuel des programmes antipaludéens dans chaque pays d'Afrique se monterait à environ 345 000 euros, soit, pour un pays de 5 millions d'habitants, moins de sept centimes d'euros par habitant.
Les populations localisées dans des zones impaludées vivant dans leur immense majorité dans la pauvreté, les nouveaux médicaments, nettement plus efficaces mais plus coûteux que les anciens, sont bien souvent au-delà de leurs moyens.
Il arrive même parfois qu'un patient ne suive pas entièrement son traitement et, se sentant guéri, qu'il aille vendre ce qui lui reste au marché noir, accélérant ainsi l'apparition de résistances aux traitements (voir chapitre sur la résistance du parasite).
D'après les chiffres, le secteur privé consacrait, en 1990 et par victime, 789 dollars pour combattre l'asthme, 3 274 pour le sida (dont le virus concerne autant les pays en voie de développement que les pays développés) et seulement 65 dollars en ce qui concerne le paludisme. Autrement dit, la somme consacrée à la recherche de vaccins et au développement de médicaments antipaludéens est ridicule lorsque l'on sait que près de 50 % de la population mondiale est menacée.
De plus, la grande majorité des pays touchés par la malaria n'ont ni les moyens économiques ni les moyens technologiques de développer dans leur pays une réelle recherche dans le domaine médical. Des pays aux moyens financiers très limités (le plus souvent croulant sous le poids de la dette extérieure), un manque de solide volonté politique, un budget recherche bien inférieur aux attentes et une aide internationale dérisoire comparée aux besoins des populations et au nombre de personnes touchées, rappellent que les conséquences aussi désastreuses de cette maladie du sous-développement ne sont pas entièrement dues à la nature, que l'être humain y est pour beaucoup.
Cependant l'OMS a fondé en 2001 un Fonds mondial pour lutter contre la malaria mais aussi contre le SIDA et la tuberculose.
Depuis 2003, la fondation Bill-et-Melinda-Gates (Bill & Melinda Gates Foundation), a également versé plusieurs centaines de millions de dollars, entre autres à la Malaria Vaccine Initiative, pour lutter contre la maladie.
Créé en 2002, le Fonds mondial de lutte contre le SIDA, la tuberculose et le paludisme, ou Fonds mondial, regroupe des financements internationaux en faveur du traitement du paludisme.
Divers
- En France, cette maladie est sur la liste des Maladies infectieuses à déclaration obligatoire.
- Le paludisme a été souvent illustré sur des timbres. Le premier exemple est un timbre de bienfaisance du Mexique émis en 1939 qui montre un être humain victime d'un moustique géant. Mais le plus spectaculaire fut l'émission de 1962 simultanée dans une centaine de pays célébrant la campagne de l'OMS intitulée éradication du paludisme. L'OMS a fait de l'éradication du paludisme l'une de ses principales priorités.
- Le roman Le Chromosome de Calcutta d'Amitav Ghosh (éd. Seuil 1998, coll. Cadre vert, fait une large place au récit, dans une atmosphère fantastique, de la découverte de Ronald Ross sur le paludisme.
Notes et références
- (en) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en anglais intitulé « Malaria » (voir la liste des auteurs)
- Définitions lexicographiques et étymologiques de « paludisme » du CNRTL.
- Définitions lexicographiques et étymologiques de « malaria » du CNRTL.
- World Malaria Report 2010 [lire en ligne]
- Joy D, Feng X, Mu J, et al, « Early origin and recent expansion of Plasmodium falciparum », dans Science, vol. 300, issue 5617, pp. 318-21, 2003.
- Escalante A, Freeland D, Collins W, Lal A, The evolution of primate malaria parasites based on the gene encoding cytochrome b from the linear mitochondrial genome, Proc Natl Acad Sci U S A, vol. 95, issue 14, pp. 8124-9, 1998 [lire en ligne].
- Weimin Liu, Yingying Li, Learn GH et Als. Origin of the human malaria parasite Plasmodium falciparum in gorillas, Nature, 2010;467:420–425
- F. Cox, « History of human parasitology », dans Clin Microbiol Rev, vol. 15, n°4, pp. 595-612, 2001 [lire en ligne].
- Le Monde Toutânkhamon aurait succombé au paludisme et à une maladie des os - article du 17 février 2010 [(fr) lire en ligne]
- JAMA. 2010 Feb 17;303(7):638-47 [(en) lire en ligne]
- Kaufman T, Rúveda E, « The quest for quinine: those who won the battles and those who won the war », dans Angew Chem Int Ed Engl, vol. 44, n°6, pp.854-85, 2005.
- Kyle R, Shampe M, « Discoverers of quinine », dans JAMA, vol. 229, n°4, p. 462, 1974.
- Biography of Alphonse Laveran, The Nobel Foundation [lire en ligne].
- Page sur Ettore Marchiafava.
- Lénaick Ollivier de l'Institut de médecine tropicale du service de santé des armées (IMTSSA Marseille), cité par Le Figaro du 10 juin 2008, page 16.
- Biography of Ronald Ross, The Nobel Foundation [lire en ligne].
- Ross and the Discovery that Mosquitoes Transmit Malaria Parasites
- Raju T, « Hot brains: manipulating body heat to save the brain », dans Pediatrics, vol. 177, n°2, p. e320-1, 2006 [(en) lire en ligne]
- En 1991 puis de nouveau en 2001 , Charles Gilks , rappelant les expérimentations ayant recouru à l'injection de sang de singes infectés à des humains, émettait l'hypothèse qu'elles auraient pu être à l'origine du virus du Sida . Il s'y désolait que cette piste n'ait suscité aucune recherche Man, monkeys and malaria 2001
- Organisation mondiale de la santé, Applications actuelles de la malariathérapie, bulletin n° 50, p. 15 à 167, 1974 [lire en ligne]
- Chimiothérapie du paludisme, sous la direction de R. H. Black, Craig J. Canfield, D. F. Clyde, W. Peters et W. H. Wernsdorfer, 2e éd., Organisation mondiale de la santé, Genève, 1984, p.13 [lire en ligne]
- Rhodoquine embonate [lire en ligne]
- E. Fourneau, M. et Mme. Tréfouël, Mlle Benoît, « Préparations en vue d’essais thérapeutiques. IV. Dérivés quinoléiques et quinoléine arsinique », Ann. Inst. Pasteur, 1930, 44, 719
- Marcel Delépine, Ernest Fourneau (1872-1949). Sa vie et son œuvre, Masson et Cie, Paris, 1949, pp. 61-63
- Choloroquine diphosphate [lire en ligne]
- Anthony Sutton, Wall Street and the Rise of Hitler, chap. 2 « The Empire of I.G. Farben », The Modern History Project, 1976 [lire en ligne].
- Hempelmann E., « Hemozoin biocrystallization in Plasmodium falciparum and the antimalarial activity of crystallization inhibitors », dans Parasitol Research, vol. 100, n°4, pp. 671-676, 2007.
- Linus Pauling, Harvey Itano, S. J. Singer et Ibert Wells, « Sickle Cell Anemia, a Molecular Disease », dans Science, novembre 1949 [lire en ligne].
- Trager & Jensen, « Human malaria parasites in continuous culture », dans Science, vol. 193, n°4254, pp. 673-5, août 1976.
- Krotoski W, Collins W, Bray R, et al, « Demonstration of hypnozoites in sporozoite-transmitted Plasmodium vivax infection », dans Am J Trop Med Hyg, vol. 31, n°6, pp. 1291-3, 1982. Voir aussi Meis J, Verhave J, Jap P, Sinden R, Meuwissen J, « Malaria parasites -- discovery of the early liver form », dans Nature, vol. 302, n°5907, pp. 424-6, 1983.
- Centre d'études et de recherche des médecins d'Afrique associé avec le centre hospitalier universitaire et le Laboratoire de Chimie de la Coordination (CNRS) de Toulouse
- université Paul-Sabatier de Toulouse, le CNRS, l'IRD, et le Muséum national d'histoire naturelle
- Communiqué de presse du CNRS du 11 septembre 2006 - La tisane de Quassia : un antipaludique efficace[(fr) lire en ligne]
- Stout EP, Hasemeyer AP, Lane AL, Davenport TM, Engel S, Hay ME, Fairchild CR, Prudhomme J, Le Roch K, Aalbersberg W, Kubanek J. ; Org Lett. (2009) ; Antibacterial neurymenolides from the Fijian red alga Neurymenia fraxinifolia; Jan 1;11(1):225-8 (Résumé)
- Smyrniotopoulos V, Vagias C, Rahman MM, Gibbons S, Roussis V. ; Structure and antibacterial activity of brominated diterpenes from the red alga Sphaerococcus coronopifolius. Chem Biodivers. 2010 Jan; 7(1):186-95.(Résumé)
- L'article du Microbe Magazine de septembre 2009 sur le potentiel antipaludique de l'algue rouge [(en) lire en ligne]
- Lin AS, Stout EP, Prudhomme J, Le Roch K, Fairchild CR, Franzblau SG, Aalbersberg W, Hay ME, Kubanek J. ; Bioactive bromophycolides R-U from the Fijian red alga Callophycus serratus. J Nat Prod. 2010 Feb 26; 73(2):275-8. (Résumé)
- Le communiqué de presse de GlaxoSmithKline du 20 janvier 2010 [(en) lire en ligne]
- Examiner.com, « Mosquito gut bacteria shown to kill malaria parasite », article du 12 mai 2011 [(en) lire en ligne]
- Sciencemag.org, « Natural Microbe-Mediated Refractoriness to Plasmodium Infection in Anopheles gambiae », article du 13 mai 2011 [(en) lire en ligne]
- Cochrane Reviews publié le 19 avril 2006 [(en) lire en ligne]
- Fact Sheet: RTS,S Malaria Vaccine Clinical Trials. Dossier de presse du 17 octobre 2007 émis conjointement par The PATH Malaria Vaccine Initiative (PATH/MVI) et GlaxoSmithKline Biologicals (GSK Bio) [(fr) lire en ligne]
- Informations données par le Professeur Alonso sur le RTS,S dans le The Lancet du 10 décembre 2005[(en) lire en ligne]
- Malaria Vaccine Initiative - Sites choisis pour les essais cliniques de la phase III du RTS, S/AS02A[(en) lire en ligne]
- L'article 58 de l'Agence européenne des médicaments est une disposition pour une procédure qui permet à l'AEM, en collaboration étroite avec l'OMS, de publier une opinion scientifique concernant la qualité, l'efficacité et la sûreté d'un produit médical qui est prévu pour l'usage exclusivement en dehors de l'Union européenne
- Article du Sunday Nation du 26 avril 2010 - Le Kenya plus proche du vaccin contre la maladie mortelle [(en) lire en ligne]
- Article de la revue scientifique PLoS One du 2 octobre 2009 sur le PfCS102/AS02A [(en) lire en ligne]
- Communiqué de presse de l'Institut Pasteur[(fr) lire en ligne]
- Institute of Medicine -Rapport du 25 mai 2006 - Battling Malaria: Strengthening the U.S. Military Malaria Vaccine Program[(en) lire en ligne]
- U.S. National Institute of Health Phase I des essais du FMP2.1/AS02A au Mali - 1e édition : 27 juillet 2006 [(en) lire en ligne]
- guinee24.com Un nouveau vaccin expérimental - article du 4 février 2010 (source AFP) [(fr) lire en ligne]
- U.S. National Institute of Health Phase I des essais du FMP2.1/AS02A au Mali - 1e édition : 12 avril 2007 [(en) lire en ligne]
- University of Central Florida, communiqué du 26 janvier 2010 - Vaccine Could Be Lethal Weapon Against Malaria, Cholera[(en) lire en ligne]
- Davoodi-Semiromi A, Schreiber M, Nalapalli S, Verma D, Singh ND, Banks RK, Chakrabarti D, Daniell H. ; Chloroplast-derived vaccine antigens confer dual immunity against cholera and malaria by oral or injectable delivery. ; Plant Biotechnol J. 2010 Feb;8(2):223-42. Epub 2009 Dec 28. PMID:20051036 (Résumé)
- Une plante transplastomique est un végétal dont les chloroplastes ont été transformés génétiquement afin de multiplier les transgènes par cellule
- Curriculum vitæ du Professeur Crisanti[(en) lire en ligne]
- Science Daily du 21 février 2003[(en) lire en ligne]
- Site Web du Genoscope - Article sur le séquençage complet du génome d’Anopheles gambiae[(fr) lire en ligne]
- Académie des Sciences de l'Institut de France - Article du 12 juin 2007[(fr) lire en ligne]
- Site Web du Genoscope - Article sur Anopheles gambiae[(fr) lire en ligne]
- The University of Arizona - Communication du 15 juillet 2010 par Daniel Stolte - Le premier moustique résistant à la malaria [(en) lire en ligne]
- J. Breman, « The ears of the hippopotamus: manifestations, determinants, and estimates of the malaria burden », dans Am J Trop Med Hyg, vol. 64, n°1-2, pp. 1-11, 2001 [lire en ligne].
- L'estimation est difficile du fait du manque de fiabilité des statistiques dans les pays concernés ; en 2005, des chercheurs estimaient dans la revue Nature à 515 millions le nombre de malades en 2002 (dans une fourchette allant de 300 à 660 millions), alors que l'estimation de l'OMS en 1999 dans son rapport sur la santé dans le monde était de 273 millions. L'OMS a déclaré avoir révisé ce chiffre dès l'année suivante et travailler depuis avec une fourchette allant de 300 à 500 millions. Cf. la dépêche de John Bonner du 10 mars 2005 (15:18), « Row erupts over WHO's malaria 'miscalculation' », sur le site du New Scientist [(en) lire en ligne]
- Greenwood BM, Bojang K, Whitty CJ, Targett GA, « Malaria », dans Lancet, vol. 365, p. 1487-1498, 2005.
- Hay S, Guerra C, Tatem A, Noor A, Snow R, « The global distribution and population at risk of malaria: past, present, and future », dans Lancet Infect Dis, vol. 4, n°6, pp. 327-36, 2004.
- Korenromp E, Williams B, de Vlas S, Gouws E, Gilks C, Ghys P, Nahlen B, « Malaria attributable to the HIV-1 epidemic, sub-Saharan Africa », dans Emerg Infect Dis, vol. 11, n°9, pp. 1410-9, 2005 [lire en ligne]
- Abu-Raddad L, Patnaik P, Kublin J, « Dual infection with HIV and malaria fuels the spread of both diseases in sub-Saharan Africa », dans Science, vol. 314, n°5805, pp. 1603-6, 2006.
- Layne SP, Principles of Infectious Disease Epidemiology, EPI 220, UCLA Department of Epidemiology [lire en ligne]
- Greenwood B, Mutabingwa T, « Malaria in 2002 », dans Nature, vol. 415, n°670-2, 2002.
- Grover-Kopec E, Kawano M, Klaver R, Blumenthal B, Ceccato P, Connor S, « An online operational rainfall-monitoring resource for epidemic malaria early warning systems in Africa », dans Malar J., vol. 4, p. 6, 2005 [lire en ligne]
- Van Benthem B, Vanwambeke S, Khantikul N, Burghoorn-Maas C, Panart K, Oskam L, Lambin E, Somboon P, « Spatial patterns of and risk factors for seropositivity for dengue infection », dans Am J Trop Med Hyg, vol. 72, n°2, pp. 201-8, 2005 [lire en ligne]
- Trung H, Van Bortel W, Sochantha T, Keokenchanh K, Quang N, Cong L, Coosemans M, « Malaria transmission and major malaria vectors in different geographical areas of Southeast Asia », dans Trop Med Int Health, vol. 9, n°2, pp. 230-7, 2004.
- Keiser J, Utzinger J, Caldas de Castro M, Smith T, Tanner M, Singer B, « Urbanization in sub-saharan Africa and implication for malaria control », dans Am J Trop Med Hyg, vol. 71, n°2, pp. 118-27, 2004 [lire en ligne]
- Hay SI, Snow RW, « The Malaria Atlas Project: Developing Global Maps of Malaria Risk », dans PLoS Medicine, vol. 3, n°12, p. e473, 2006 [lire en ligne]
- J. Callot, Un problème complexe : la régression du paludisme en France , 1947.
- posdcast de le Figaro
- [ http://moustiquesinfos.sante.gouv.fr/spip.php?rubrique47 moustiquesinfos.sante.gouv.fr]
- Simon I. Hay et al., « The global distribution and population at risk of malaria : past, present, and future », in The Lancet Infectious Diseases, vol. 4, n° 6, juin 2004, p. 327-336 [(en) lire en ligne]
- Le Figaro du 10 juin 2008, page 16
- (en) The American Journal of Tropical Medecine & Hygiene - POPULATION GENETIC STRUCTURE OF THE AFRICAN MALARIA MOSQUITO ANOPHELES FUNESTUS IN KENYA - 2003 [lire en ligne]
- Sachs J, Malaney P, « The economic and social burden of malaria », dans Nature, vol.415, p. 680-5, 2002.
- Roll Back Malaria, Le Paludisme en Afrique, infosheet n°3, [lire en ligne].
- Article du The Seattle Times du 13 juin 2008 - « Rétablir les solutions de basse technologie » [(en) lire en ligne]
- Roll Back Malaria, Economic costs of malaria, OMS [lire en ligne]
- Mendis K, Sina B, Marchesini P, Carter R, « The neglected burden of Plasmodium vivax malaria », dans Am J Trop Med, vol. 64, n°1-2, pp. 97-106, 2001 [lire en ligne].
- Escalante A, Ayala F, « Phylogeny of the malarial genus Plasmodium, derived from rRNA gene sequences », dans Proc Natl Acad Sci U S A, vol. 91, n° 24, pp. 11373-7, 1994.
- PCC Garnham, Malaria parasites and other haemosporidia, Blackwell Scientific Publications, Oxford, 1996.
- Permin A. et Madsen M., Investing in Animal Health Research to Alleviate Poverty, International Livestock Research Institute, 2001, Appendix 2: review on disease occurrence and impact (smallholder poultry) [lire en ligne].
- Atkinson CT, Woods KL, Dusek RJ, Sileo LS, Iko WM, « Wildlife disease and conservation in Hawaii: pathogenicity of avian malaria (Plasmodium relictum) in experimentally infected iiwi (Vestiaria coccinea) », dans Parasitology, vol. 111 Suppl, pp. S59-69, 1995.
- Science & Vie du 6 décembre 2009 : L'anophèle piégé par une chaussette sale [(fr) lire en ligne]
- Talman A, Domarle O, McKenzie F, Ariey F, Robert V, « Gametocytogenesis: the puberty of Plasmodium falciparum », dans Malar J, vol. 3, p. 24.
- Entomologie du paludisme et contrôle des vecteurs; Trans. du paludisme (pages 7 et 8)-OMS 2003[lire en ligne]
- MEDECINE/SCIENCES 2005 (Trafic protéique dans le globule rouge infecté par Plasmodium)[lire en ligne]
- Université Paris Val de Marne - 2000 - Thèse pour le diplôme d'État de docteur en médecine (Titre 1.2.2.)[lire en ligne]
- Marcucci C, Madjdpour C, Spahn D, « Allogeneic blood transfusions: benefit, risks and clinical indications in countries with a low or high human development index », dans Br Med Bull, vol. 70, pp. 15-28.
- Malaria life cycle & pathogenesis. Malaria in Armenia.
- Critères de paludisme grave retenus par l'OMS [lire en ligne], p. 15.
- Trampuz A, Jereb M, Muzlovic I, Prabhu R, « Clinical review: Severe malaria », dans Crit Care, vol. 7, n°4, pp. 315-23, 2003 [lire en ligne]
- Kain K, Harrington M, Tennyson S, Keystone J, « Imported malaria: prospective analysis of problems in diagnosis and management », dans Clin Infect Dis, vol. 27, n°1, pp. 142-9, 1998.
- R. Idro et al., « Decorticate, decerebrate and opisthotonic posturing and seizures in Kenyan children with cerebral malaria », dans Malaria Journa, vol. 4, n°57 [lire en ligne]
- M.J. Boivin, « Effects of early cerebral malaria on cognitive ability in Senegalese children », dans Journal of Developmental and Behavioral Pediatrics, vol. 23, n°5, oct. 2002: p353-64 [lire en ligne]
- Holding, P.A. et Snow, R.W., « Impact of Plasmodium falciparum malaria on performance and learning: review of the evidence », dans American Journal of Tropical Medicine and Hygiene, vol. 64, n°1-2, janv.-fév. 2001: p68-75 [lire en ligne]
- Carter JA et al., « Developmental impairments following severe falciparum malaria in children », dans Trop Med Int Health, vol. 10, pp. 3-10, 2005.
- Redd S et al., « Clinical algorithm for treatment of Plasmodium falciparum malaria in children », dans Lancet, vol. 347, n°8996, pp. 223-7, 1996.
- Les « Community Health Worker » ou « CHW » sont des membres de la communauté ayant reçu une formation de base leur permettant de prodiguer les soins élémentaires en l'absence de personnel médical professionnel.
- American Journal of Public Health - Community Health Worker Performance in the Management of Multiple Childhood Illnesses: Siaya District, Kenya, 1997–2001 - octobre 2001 [(en) lire en ligne]
- Beare NA et al. Am J Trop Med Hyg. 2006 Nov;75(5):790-797.
- Sanofi Aventis-L'actualité du paludisme destinée aux professionnels-Section 4F2 (Microscopie : Détection des parasites) [lire en ligne]
- Warhurst DC, Williams JE, « Laboratory diagnosis of malaria », dans J Clin Pathol, vol. 49, pp. 533-38, 1996.
- Directives pour le traitement du paludisme-annexe 5.2 (page 166)- 2006 [lire en ligne]
- Pattanasin S et al., « Evaluation of a new Plasmodium lactate dehydrogenase assay (OptiMAL-IT®) for the detection of malaria », dans Transact Royal Soc Trop Med, vol. 97, pp. 672-4, 2003.
- RollBackMalaria - Consommables et produits non médicaux pour le paludisme - Séminaire du 5 au 9 mars 2006 à Dakar[lire en ligne]
- Ling IT. et al., « Antibodies to the glutamate dehydrogenase of Plasmodium falciparum », dans Parasitology, vol. 92, pp. 313-24, 1986
- Malaria Journal - Operational accuracy and comparative persistent antigenicity of HRP2 rapid diagnostic tests for Plasmodium falciparum malaria in a hyperendemic region of Uganda - 29/10/2008 (en)[lire en ligne]
- Mens PF, Schoone GJ, Kager PA, Schallig HDFH, « Detection and identification of human Plasmodium species with real-time quantitative nucleic acid sequence-based amplification », dans Malaria journal, vol. 5, n° 80, 2006.
- Adak T, Sharma V, Orlov V, « Studies on the Plasmodium vivax relapse pattern in Delhi, India », dans Am J Trop Med Hyg,vol. 59, n°1, pp. 175-9, 1998
- (en) Résultats d'une étude chez la souris DOI:10.1038/nm.2368
- NCBI - Taxonomy browser (Navigateur sur les codes génétiques des différences espèces de Plasmodium falciparum) [(en) lire en ligne]
- CNRS - Paludisme - Le parasite P. vivax infecte des populations considérées jusqu'à présent comme résistantes - 16 mars 2010 [(fr) lire en ligne]
- Carolina Lopez, Carolina saravia et al, « Mechanisms of genetically-based resistance to malaria », dans Gene, vol. 467, issue 1-2, pp. 1-12, 2010.
- Mockenhaupt F et al., « Manifestation and outcome of severe malaria in children in northern Ghana », dans Am J Trop Med Hyg, vol.71, n°2, pp. 167-72, 2004.
- Les médicaments obsolètes retardent la victoire contre le paludisme - Article du Daily Nation du 30/06/2009 [(en) lire en ligne]
- Des cliniques privées utilisent toujours les anciens traitements - Article du Daily Nation du 23/04/2009 [(en) lire en ligne]
- BEH - Chimiosensibilité du paludisme importé en France en 2001 et 2002 (article du 3 février 2004) [(en) lire en ligne]
- (en)Malaria — Time to Act, Nicholas J. White, New Eng. J. Med., 9/11/2006,355:1956-1957.
- (en)Return of Chloroquine Antimalarial Efficacy in Malawi, Miriam K. Laufer, Phillip C. Thesing, Nicole D. Eddington, Rhoda Masonga, Fraction K. Dzinjalamala, Shannon L. Takala, Terrie E. Taylor, Christopher V. Plowe, New Engl. J. Med., 9/11/2006;355:1959-1966.
- Rev Prescrire 2007;27(290):913-920 reprenant World Health Organisation "Guideline for the treatment of malaria" Geneva 2006:261p
- (en)Afonso A, Hunt P, Cheesman S, Alves AC, Cunha CV, do Rosário V,1 and Cravo P, « Malaria parasites can develop stable resistance to artemisinin but lack mutations in candidate genes », dans Antimicrob. Agents Chemother., vol. 50, no 2, 2006, p. 480-489 [lien PMID, lien DOI]
- L'Asaq : un nouveau médicament. Dossier "Malaria" de MSF Belgique [[id=3&uw_vars[table]=tx_uwazg_theme&cHash=ed97c7781e lire en ligne]]
- Récapitulatif de la politique de l'OMS - mai 2010 [(fr) lire en ligne]
- Rapport 2007 de l'OMS sur les suppositoires à l'artémisinine [lire en ligne]
- Lon CT, Tsuyuoka R, Phanouvong S, et al., « Counterfeit and substandard antimalarial drugs in Cambodia », dans Trans R Soc Trop Med Hyg, vol. 100, n°11, pp. 1019-24, 2006.
- U. S. Pharmacopeia, Fake antimalarials found in Yunan province, China, 2004 [lire en ligne]
- Newton PN, Green MD, Fernández FM, Day NPJ, White NJ, « Counterfeit anti-infective drugs », dans Lancet Infect Dis, vol. 6, n°9, pp. 602-13, 2006
- BBC News du 17 août 2007 [lire en ligne]
- Kevin Hull, Malaria: Fever Wars, documentaire PBS, 2006 [lire en ligne]
- Barat, « Four malaria success stories: how malaria burden was successfully reduced in Brazil, Eritrea, India, and Vietnam », dans Am J Trop Med Hyg, vol. 74, n°1, pp.12-16, 2006.
- OMS-Position sur l'utilisation du DDT 2005 [lire en ligne]
- Préfecture de la Réunion - Direction des Affaires Sanitaires et Sociales - La lutte contre les moustiques - 2006 [lire en ligne]
- Organisation mondiale de la santé, La planification de programmes de lutte contre le paludisme : guide du stagiaire, éd. provisoire, OMS, Genève, 2003, p. 128 [lire en ligne]
- Société Française pour l'Etude et la Protection des Mammifères-Nuit européenne des chauves-souris 2008 [lire en ligne]
- Eurekalert.org - Le séquençage du génome du moustique, publié dans la revue Science, ouvre la voie à de nouveaux moyens de lutte contre le paludisme - 02/10/2002[lire en ligne]
- Ethnobotanical study of some of mosquito repellent plants in north-eastern Tanzania - Eliningaya J Kweka, Franklin Mosha, Asanterabi Lowassa, Aneth M Mahande, Jovin Kitau, Johnson Matowo, Michael J Mahande, Charles P Massenga, Filemoni Tenu, Emmanuel Feston, Ester E Lyatuu, Michael A Mboya, Rajabu Mndeme, Grace Chuwa and Emmanuel A Temu - Malaria Journal 2008, 7:152doi:10.1186/1475-2875-7-152 publié le 7 août 2008
- Saltidin - Informations techniques [(en) lire en ligne]
- Johns Hopkins University-Tests de traitement de l'anémie 2003 [lire en ligne]
- Institut de Médecine Tropicale Anvers-Conseils de santé pour voyageurs;édition destinée au corps médical 2007-2008 [[
- http://www.itg.be/ITG/Uploads/MedServ/fmedasso.pdf lire en ligne]]
- ITG (Instituut voor Tropische Geneeskunde-Votre santé durant le voyage-Malaria (version août 2008) [lire en ligne]
- Centre Belge d'Information Pharmacothérapeutique-Commentaires, posologie des tétracyclines [lire en ligne]
- Centre Belge d'Information Pharmacothérapeutique-Commentaires, posologie des antipaludéens-Répertoire "nom de la spécialité" débutant par "L" [lire en ligne]
- Centre Belge d'Information Pharmacothérapeutique-Commentaires, posologie des antipaludéens-Répertoire "nom de la spécialité" débutant par "M" [lire en ligne]
- Article du The Standard du 8 mai 2010 - Combattre la malaria par des SMS [(en) lire en ligne]
Voir aussi
Bibliographie
- Jacques Verdrager, L'OMS et le paludisme : mémoires d'un médecin spécialiste de la malaria. – L'Harmattan, coll. « Acteurs de la science », Paris, 2005 (ISBN 2-7475-8246-9)
- « Santé des voyageurs et recommandations sanitaires 2005 », Bulletin épidémiologique hebdomadaire, no 24-25/2005 (14 juin 2005) [lire en ligne]
- Robert W. Snow et al. « The global distribution of clinical episodes of Plasmodium falciparum malaria », Nature, vol. 434, n° 7030 (10 mars 2005), pp. 214-217 [(en) présentation en ligne]
- Marie Josserand Debacker, Paludisme : historique, mythes, croyances et idées reçues, thèse d'exercice, Médecine, Paris XII, 2000 [lire en ligne]
- Serge Paul Eholié, Emmanuel Bissagnéné et Pierre-Marie Girard (dir.), Mémento thérapeutique du paludisme en Afrique, Doin, IMEA, Paris, 2008, 139 p. (ISBN 978-2-7040-1253-4)
- Christian Lengeler, Jacqueline Cattani et Don de Savigny (dir.), Un mur contre la malaria : du nouveau dans la prévention des décès dus au paludisme, Centre de recherches pour le développement international, Ottawa ; Organisation mondiale de la santé, Genève, 1997, 220 p. (ISBN 0-88936-831-7)
- Jean Mouchet, Pierre Carnevale, Marc Coosemans et al., Biodiversité du paludisme dans le monde, J. Libbey Eurotext, Montrouge, 2004, 428 p. (ISBN 2-7420-0528-5)
Filmographie
- Paludisme, l'hécatombe silencieuse, documentaire réalisé par Bernard Germain et Jean Vercoutère, produit par Mosaïque Films (Paris) et distribué par ADAV, 2000, 54' (VHS)
Articles connexes
- Journée mondiale du paludisme
- Paludisme aviaire
- Malaria Control
- Fonds mondial de lutte contre le SIDA, la tuberculose et le paludisme
- DNDi (Drugs for Neglected Diseases Initiative)
Liens externes
- (fr) Page de l'OMS
- (fr) Malaria Atlas Project
- (en) Projets de la Banque mondiale
- (en) Site européen BIOMALPAR, dédié au paludisme;Projets de la Banque mondiale
Catégories :- Paludisme
- Maladie tropicale
- Maladie infectieuse en hématologie
- Parasitologie médicale
- Zoonose
Wikimedia Foundation. 2010.