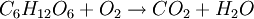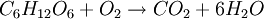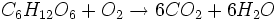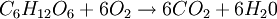- Equilibrage d'une equation chimique par la methode des tatonnements
-
Équilibrage d'une équation chimique par la méthode des tâtonnements
Équilibrer une réaction chimique, c'est ajuster le nombre de moles des espèces chimiques composant les réactifs et les produits de la réaction étudiée.
En effet, lorsqu'on considère une réaction chimique, on le fait d'un point de vue qualitatif : on sait que tels et tels réactifs ont réagi pour former tels et tels produits. Mais la fameuse règle « Rien ne se perd, rien ne se crée, tout se transforme »[1] impose d'équilibrer les deux membres de la réaction pour qu'elle soit correcte.
Ainsi, prenons l'exemple de la dégradation de la molécule du glucose (C6H12O6) dans l'organisme, équation très courante. D'un point de vue qualitatif, elle s'écrit :
Mais si l'on recompte le nombre de moles des espèces chimiques mises en jeu de part et d'autre de l'équation, on s'aperçoit par exemple qu'il y a 12 moles d'hydrogène dans les réactifs, et que seulement 2 moles d'hydrogène sont formées, soit 6 fois moins.
Il va donc falloir appliquer des nombres stoechiométriques aux réactifs et aux produits pour parvenir à une égalité. Tout d'abord, nous venons de remarquer qu'il y avait 6 fois plus d'hydrogène à gauche de l'équation qu'à droite ; pour compenser ce déficit, nous allons ajouter le coefficient 6 à la molécule d'eau (H2O), ce qui va donner :
De même, il y a 6 moles de carbone (C) à gauche pour une à droite ; on va donc ajouter le nombre 6 au dioxyde de carbone (CO2) :
Enfin, il faut équilibrer l'oxygène (O), 18 moles à droite et 6 à gauche : il va donc falloir en ajouter 12 au membre de gauche ; pour cela, on ajoute 6 au dioxygène (O2), ce qui revient au même. On obtient finalement l'équation équilibrée:
Pour équilibrer les nombres stoechiométriques d'une équation, il faudra toujours utiliser une méthode de ce type, en gardant à l'esprit qu'il faut partir des espèces chimiques apparaissant le moins souvent dans la réaction.
Attention ! L'équilibrage d'une équation chimique peut parfois imposer une certaine gymnastique des nombres, puisqu’il est nécessaire de parvenir à une égalité sans pour autant modifier les entités chimiques de la réaction. Vous pourrez constater que dans certains cas, l'équilibrage d'une espèce chimique en déséquilibrera une autre de la réaction, et ainsi de suite, ce qui pourra parfois vous contraindre à utiliser des nombres stoechiométriques élevés, et donc plus difficiles à manipuler.
Références
Voir aussi
- Équilibrage d'une équation chimique par la méthode algébrique
- Équilibrage d'une équation chimique par la méthode électronique
- Équilibrage d'une équation chimique par la méthode des demi-réactions en milieu acide
- Portail de la chimie
Catégories : Chimie générale | Réaction chimique
Wikimedia Foundation. 2010.