- Césium 137
-
Le césium 137, noté 137Cs, est l'un des 39 isotopes connus du césium, élément qui a le plus grand nombre d'isotopes après le francium.
 Diagramme présentant les retombées des 10 principaux essais nucléaires qui ont le plus exposés la population nord américaine au Césium 137
Diagramme présentant les retombées des 10 principaux essais nucléaires qui ont le plus exposés la population nord américaine au Césium 137
C'est l’isotope du césium dont le nombre de masse est égal à 137 : son noyau atomique compte 55 protons et 82 neutrons avec un spin 7/2+ pour une masse atomique de 136,9070835 g/mol.
Il est caractérisé par un défaut de masse de 86 551 145 ± 2 985 eV/c2 et une énergie de liaison nucléaire de 1 149 292 932 ± 2 991 eV[1].
Origine
C’est l'un des nombreux produits de fission de l'uranium et sans doute le plus connu pour avoir été utilisé dans les études hydrologiques et écologiques suite à une contamination générale de l'atmosphère induite, à partir de 1945, par l'utilisation des bombes atomiques et des essais nucléaires (puis l'accident de Tchernobyl), et, dans une moindre mesure, à cause des rejets de centrales nucléaires ou de sites de retraitement, Entreposage nucléaire (provisoire) ou stockage durable des déchets radioactifs, etc.
Son suivi a par exemple permis de mesurer à quelle vitesse l'eau des nappes se renouvelait, la cinétique environnementale du césium (notamment dans la chaîne alimentaire) ou si une grotte était ou non isolée du monde extérieur.
Apparence
Quand il est pur, il se présente comme un métal alcalin argent-doré.
Son point de fusion est assez proche de la température ambiante (CATP) pour qu'il soit possible de l'obtenir à l'état liquide à cette température grâce à la surfusion (comme pour le gallium et rubidium)Radioactivité
Un gramme de césium 137 pur présente une radioactivité de 3,26 TBq.
Le césium 137 se désintègre en baryum 137 (de courte durée produit de la dégradation), puis en une forme de baryum non-radioactif.Dans l'environnement, on le trouve rarement seul. Les déchets radioactifs, ou les retombées d'essais nucléaires atmosphériques ou de l'accident de Tchernobyl ainsi que de celui de la Centrale nucléaire de Fukushima Daiichi peuvent également contenir du césium 135 (à très longue période radioactive), du césium 134 (période de 2 ans), mais le césium 137 (période de 30 ans) compose l'essentiel des formes du césium libérées à ces occasions.
Désintégration
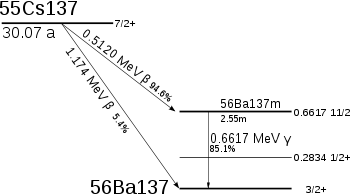
Dans 94,6 % des cas, il donne l’isomère 137mBa du baryum 137 par désintégration β- avec une énergie de désintégration de 512 000 eV et une période radioactive de 30,07 ans, lequel retombe à son état fondamental par transition isomérique émettant un rayonnement γ de 661 700 eV avec une période de 2,552 minutes :
Dans les 5,4 % des cas restants, il se désintègre directement en 137Ba avec une énergie de désintégration de 1 174 000 eV.
Le rayonnement γ émis par le 137mBa peut être utilisé à des fins médicales ou industrielles, par exemple pour l’irradiation des aliments, mais le césium 137 n’est en fait que très peu utilisé en raison de son instabilité chimique bien plus grande que celle du cobalt 60, isotope bien meilleur pour ce type d’applications car chimiquement plus simple à contrôler et émettant un rayonnement plus puissant. On le trouve dans certains appareils de mesure de densité ou d’humidité, des débitmètres et divers détecteurs.
Sources de contamination, normes alimentaires en situation normale ou de crise nucléaire
C’est un produit de fission de l’uranium et, comme tel, des quantités plus ou moins importantes de cet isotope ont été relâchées dans l’atmosphère d'abord dans les années 1940 et 1950 lors des essais nucléaires à l’air libre, puis lors d’accidents nucléaires (Voir la Liste des accidents nucléaires).
Les dernières contaminations générales ou importantes de la biosphère a été induite par la Tchernobyl, le 26 avril 1986 qui reste aujourd’hui la principale contamination radioactive de la zone interdite et de certaines zones contaminées par le passage du nuage, puis par la Catastrophe de Fukushima.Normes : Elles ont varié selon les pays et les époques et selon les produits (plus sévères pour le lait que la viande car le lait est plus consommé par les enfants qui sont plus vulnérable au Césium 134 ou 137).
A titre d'exemple, pour la viande :- 600 Bq/kg est la norme européenne actuellement en vigueur [2] à ne pas dépasser pour la venaison et la viande d'animaux d'élevage ;
- 500 Bq/kg est la norme pour le Japon[3]
- 3.700 Bq/kg est la norme, beaucoup plus laxiste, édictée en URSS suite à l'accident de Tchernobyl[4] avant d'être redescendue à 740 Bq/kg en Russie en 1990[4].
- 592 Bq/kg est la norme actuelle pour les pommes de terre et la viande en Bélarus, décidée par le gouvernement, une fois la république devenue indépendante.
Toxicité
Le césium 137 est particulièrement toxique et écotoxique. Il affecte a priori tous les êtres vivants et d'autant plus qu'ils sont jeunes.
Sa toxicité est chimique, mais elle résulte surtout et probablement presque essentiellement de ses propriétés radiologiques [5].
Pour ce qui concerne les effets radiatifs et ionisants, on peut distinguer l'exposition externe, et l'exposition interne. Cette dernière est beaucoup plus dangereuse, car la toxicité du césium inhalé ou ingéré est fortement exacerbée par le fait que le césium 137 est un analogue du potassium ; Ceci fait qu'il est rapidement assimilé, dans n'importe quelle partie de l’organisme, d’où il ne sera éliminé qu’avec une période biologique de 70 jours environ[6]. Dans un même environnement, l'enfant, qui a des besoins en potassium plus important que l'adulte, en absorbe et en fixe plus que ce dernier.Cinétique dans l'organisme humain
Sur le long terme, la contamination se fait surtout par ingestion et absorption gastro-intestinale.
Le césium est ensuite transporté par le sang et tend à se fixer à la place de son analogue chimique, le potassium, principalement dans le squelette.Effets
Les effets des faibles doses d'irradiation sont discutés, mais les effets avérés des « fortes » doses sont
- insuffisance médullaire et atteinte du système immunitaire ;
- délétion de la fonction de reproduction (stérilisation);
- effets hépatotoxiques ;
- affections rénales ;
- troubles de la minéralisation osseuse ;
- lésions cérébrales, éventuellement associées à des troubles neurologiques ;
À doses plus faibles, et à plus long terme, on lui reconnait aussi les impacts suivants :
- perturbations du cycle veille-sommeil, sans troubles comportementaux importants
- atteinte du système cardiovasculaire
- troubles du métabolismes de la vitamine D, du cholestérol et des hormones stéroïdiennes, sans symptomatologie clinique
- malformations congénitales et fœtales,
- risque accru de cancers de la thyroïde
D'autres effets, à plus long terme sont suspectés sur le cœur, la paroi de l'estomac.
Un risque accru de trisomie 21 est également suspectée. Un nombre statistiquement anormalement élevé de trisomies 21 a en effet été constatée en janvier 1987[7] dans des pays très touchés et pour les bébés conçus au moment du passage du nuage. Une nette augmentation (plus que doublement) a été constatée en Belarus avec 26 cas observés par le registre national des malformations congénitales pour 9,84 cas attendus[8],[9] (pays le plus touché par les retombées), mais aussi à Berlin Ouest où la quasi intégralité des trisomies signalées à la naissance mais aussi en diagnostiqués prénatal, est consignée dans un registre, avec la distribution de l'âge maternel. Ce registre montre une augmentation significative du nombre de cas en janvier 1987, soit neuf mois exactement après la catastrophe de Tchernobyl. Mais dans les deux cas ce phénomène ne s'est pas prolongé dans le temps. Il pourrait donc aussi être du à l'Iode radioactif (dont la décroissance radioactive est très rapide). Ce type de statistiques est par ailleurs d'utilisation délicate depuis, en raison du manque de registres précis et homogènes dans de nombreux pays, en raison du fait que de nombreux avortements volontaires ont suivi l'accident dans certains pays (Bélarus ou l'ont précédé comme en Suède[10] par exemple), que les populations des zones contaminées on fait beaucoup moins d'enfant (le Belarus est l'un des pays où la natalité a le plus décliné dans le monde, Aux environs de Tchernobyl la première naissance déclarée a eu lieu 17 ans après l'explosion) et enfin parce que les moyens de détecter la trisomie précocement, et la possibilité d'alors déclencher un avortement médical ont beaucoup évolué. La présence d'un pic de trisomies en janvier 1987 9 mois après le passage du panache, ainsi que des données expérimentales montrant une phase radiosensibles de l'ovogenèse autour du temps de conception chez les mammifères suggèrent que ce « pic de janvier » peut être liée au panache de Tchernobyl, mais pas nécessairement au seul Césium 137[7].
Thérapies
En cas d'absorption de 137Cs, le traitement chélateur préconisé par la médecine nucléaire est le bleu de Prusse (Radiogardase®) qui permet de décorporer le 137Cs ingéré et disponible. L’administration interne de pectine est également testée, notamment chez les enfants et sur le long terme dans certaines zones contaminées, mais son degré d'efficacité est encore discuté.
Contamination de l'environnement
Les essais nucléaires et certains accident (dont celui de Tchernobyl) ont été sources d'importantes contamination de l'environnement. Le césium peut être bio-accumulé, par exemple par les mousses et lichens dans un premier temps, et éventuellement localement (concentré par le réseau trophique).
Les champignons jouent à ce propos un rôle particulier, et en particulier certaines espèces trouvées en surface ou sous le sol tels que les champignons à fructification hypogée (sous le sol) (ex : truffes, dont [la truffe du cerf (Elaphomyces granulatus), très consommée par les sangliers et les écureuils). Grâce à leur vaste zone de prospection dans les 30 premiers cm du sol, via leur réseau mycélien souterrain ou capable de coloniser le bois mort (lui-même éventuellement contaminé), ces champignons peuvent concentrer le césium retombé avec les pluies ou dépôts secs ayant suivi les essais nucléaires ou certains accidents.
Par exemple, après le passage du nuage de Tchernobyl, leur contamination a en France varié de 15 à 50 000 Bq/kg, selon les sources officielles[11]En cas d'accident nucléaire suivi de redéposition importante de césium 137, les seuils à ne pas dépasser dits « niveaux d'intervention » (activité massique des produits alimentaires, doses individuelles pour les populations ne dépassant pas 1 mSv/a) pourraient ils être respectés ? C'est la question posée en 1993 par un exercice de crise franco-russe qui s'est déroulé à Saint-Pétersbourg (21-25 juin 1993)[12], avec un scénario de radioactivité surfacique maximale de 3.700 kBq/m2 (100 Ci/km2). Les résultats ont montré que 5 ans après, avec une agriculture limitée aux zones à moindre risque, et pour les produits les plus consommés ; c'est pour la viande de porc et de bœuf et pour les champignons qu'il serait le plus difficile (impossibilité même) de respecter les normes européennes.
Cinétique environnementale
Après dépôt du Césium 137 au sol (pluie, neige, dépôts secs...), il y percole lentement ou circule horizontalement plus ou moins vite selon la nature du sol, la présence d'eau et l'acidité (pH) de cette eau, et selon qu'il reste à l’état libre ou qu'il soit plus ou moins durablement piégé dans les complexes argilo-humiques, les mousses ou lichens ou les tourbes (qui peuvent, en zone contaminée, brûler comme on l'a vu lors des incendies de forêt et de tourbières en Russie en 2010). Après Tchernobyl en Bélarus, la plus grande partie des matières radioactives s'est d'abord concentrée dans la couche superficielle du sol. « Aujourd'hui, 90 % de la radioactivité a migré vers la litière et les horizons supérieurs. La strate herbacée, la litière et les couches de sol les plus superficielles forment conjointement le «champ d'absorption» [13] ou «couverture d'absorption» [14] le plus intense »[15].
Selon l'IRSN [16]« Dans les sols non labourés, et plus particulièrement en forêt, cette couche peut encore contenir, 20 ans après, 70 % de l’activité en césium 137 déposée en 1986. Ceci explique que la contamination des champignons est aujourd’hui (en 2004) 100 à 10 000 fois plus élevée que celle des produits agricoles. En fonction de la contamination du sol et de l’espèce, elle varie de moins de 1 Bq/kg à quelques centaines de Bq/kg ». Les sangliers et écureuils ou d'autres mycophages peuvent ainsi se contaminer (toujours selon l'IRSN [16], en 1996, 10 ans après l'accident, « des activités en césium 137 de quelques centaines à 2 000 Bq/kg étaient mesurées dans de la viande de sanglier des Vosges »). par le jeu de la bioconcentration, les doses de radioactivité de champignons et du sol (dans les creux, en montagne et forêt pour des zones où il a plu lors du passage du nuage) la radioactivité a même pu continuer à localement s'accroître dans les 15 ans ayant suivi le passage du nuage.
La richesse du sol en vers de terre, en champignons ou son remaniement influent sur les mouvements de ce radionucléide dans le sol[17]. En moyenne, il s'enfonce dans la couche humique à raison de 1 cm par an environ et une partie peut périodiquement être extraite du sol par les racines de plantes, puis y revenir via les feuilles mortes, les bois mort, les excréments des animaux, etc. Ce n'est donc qu'après un certain temps (15 à 25 ans ?) que les champignons le collecteront probablement le plus facilement.
Lysikov a montré (en 1995) près de la centrale de Tchernobyl que les activités de fouissage du sanglier interféraient avec la circulation des radionucléides (dont Césium) dans l'environnement[18]. Le césium est un cation chimiquement toxique[19], très soluble dans le bol alimentaire et qui traverse facilement la barrière intestinale au niveau du petit intestin[20]. d'où il gagne facilement toutes les parties du corps (comme s'il avait été inhalé)[21],[22]. L'excrétion du Césium via l'urine (des sangliers, écureuils) devient alors une source de recontamination de l'environnement, en surface. Le vers de terre peuvent aussi en remonter une certaine quantité.
L'INRA de Montpellier a tenté de modéliser la circulation du césium via les plantes et le sol dans les années 1990, sur la base de données montrant que le taux et la vitesse d'absorption par les plantes dépendaient des espèces considérées, mais aussi comme on pouvait s'y attendre de la concentration en potassium du sol, de la densité racinaire et de la distribution profonde des racines.
La présence de matière organique dans l'argile diminue la fixation du césium dans le sol et favorise son transfert vers la plante (jusqu'à 90 % en plus). Siobhan Staunton de l'INRA (ENSAM) notait néanmoins en 1996[23] qu'une grande part du césium pompé par la plante est excrétée et non transférée vers les parties supérieures.
Peu après une pollution de surface, ce sont les plantes à racines superficielles qui sont contaminées, puis 20 ans après en moyenne, ce sont les plantes se nourrissant plus profondément ou certains champignons.
On ignore encore si les symbioses arbre-champignons peuvent via la mycorhization faciliter la pénétration du Césium dans les arbres quand le césium sera le plus accessibles à la couche racinaire et à la zone la plus explorée par les mycéliums d'espèces symbiotes des arbres (truffes en particulier, symbiotes du chêne et du noisetier).Contamination de l'alimentation du bétail
Depuis la catastrophre de Tchernobyl, en Finlande (pays fortement touchée par le passage du nuage de Tchernobyl où il a fallu abattre de nombre rennes contaminés), on a efficacement testé chez le renne[24] l'adjonction de bentonite puis de plusieurs formes d'hexacyanoferrates (dont ammonium-iron-hexacyanoferrate ou ammonium ferric hexacyanoferrate (AFCF, un dérivé du Bleu de Prusse) dans l’alimentation animale (Ex : lichens donnés à mangé aux Rennes en Finlande), comme agent complexant (mais non chélateur, présentant une certaine toxicité, mais limitant les transferts de la nourriture vers l'organisme de l'animal qui la mange ; Ex : le lait et alors jusqu'à 5 fois moins radioactif. Le taux de césium des globules rouges des rennes est diminué de 50% avec un e doses quotidienne de 1 mg/kg de ammoniumironhexacyanoferrate par kg (selon poids de l'animal), soit le même résultat qu'avec 500 mg/kg of bentonite[24]. 3 mg/kg d'AFCF ou 2 g/kg de bentonite réduisent à la fois l'excrétion urinaire et les taux RBC de plus de 80%[24]. Des zéolites[25] et de la vermiculite a aussi été testé comme contre mesure, avec le ferricyanure d'ammonium, en supplément alimentaire du bétail[26]. Au début des années 1960, on avait déjà identifié la capacité de complexation du Cyanoferrate ferrique pour le Césium[27].
Le cas particulier des forêts et produits forestiers
En raison de leur richesse en champignons, parce qu'elles ont mieux capté le césium lors du passage du nuage, et parce qu'elles protègent les sols de l'érosion, les forêts sont devenues des « réservoirs et sources de radiations » [15].
En effet, elles ont stocké et localement même reconcentré le césium, ce qui fait que les aliments d'origine forestière (champignons, fruits, gibier) sont beaucoup plus contaminés que ceux provenant des champs cultivés. par exemple, après la catastrophe de Tchernobyl, on a estimé que les forêts bélarusses ont « capturé plus de 80 % des radionucléides dispersés par la centrale de Tchernobyl (ceux dont la durée de vie est la plus longue étant le césium 137, le strontium 90 et le plutonium 239, 240 et 241) ». Une grande partie de ces radionucléides sont ensuite intégrés dans le cycle forestier (ligneux → bois mort + feuilles mortes → champignons → humus → plantes ligneuses, etc[15]. Dans un cycle parallèle, la faune en capte une partie, qu'elle rend au sol via ses excréments et les cadavres [13]. Seuls les oiseaux et poissons migrateurs contribuent à exporter (et/ou à importer ce césium radiotoxique).
Ceci explique les très fortes teneurs en césium 137 des aliments forestiers (baies, champignons et gibier, régulièrement consommés par les villageois en Bélarus et Ukraine), qui était de 20 à 50 fois supérieure à celle des produits agricoles des mêmes régions[15].
Le monde scientifique cherche depuis plus de 20 ans à réduire les risques et dangers liés à ce fait, « mais aucune solution à ce problème n'a encore été trouvée » selon Victor A. Ipatyev (Directeur de l'Institut forestier de l'Académie nationale des sciences du Bélarus, à Gomel (Bélarus), relayé par la FAO[15]. les forêts humides (écologiquement très riches) semblent les plus vulnérables.Le cas particulier des tourbières et marais
Les tourbières alcalines sont des zones de stockage de radionucléïdes. Les tourbières acides sont supposées au contraire favoriser la circulation des métaux dans l'eau.
A titre d'exemple, le tableau ci dessous rapporte la radioactivité de fruits (mûres, myrtilles, airelles) et champignons (Paxillus et Russula) récoltés en Bélarus à environ à 120 km de la centrale nucléaire de Tchernobyl, en zone expérimentale (zone humide eutrophe-mésotrophe, comprenant une zone drainée (nappe à - 56 cm) et non drainée (nappe à -27 cm)) en 2000 étaient beaucoup moins contaminés (2 à 3 fois moins) dans les zones où ces marais avaient été drainées[15]. Il montre que le drainage a limité l'accès de ces plantes au radionucléides, mais comme on l'a vu en 2010, le drainage rend néanmoins les tourbières et forêts plus vulnérables aux incendies et peut-être à la fuite de radionucléides vers les nappes ou cours d'eau qui reçoivent les exutoires de drains et fossés de drainage.Aliment Avec nappe phréatique à
-27 cmnappe phréatique drainée
(à -56 cm)Mûres 617 000 Bq/m² 312 000 Bq/m² Myrtilles 709 000 Bq/m² 205 000 Bq/m² Airelles (fruit) 888 000 Bq/m² 234 000 Bq/m² Airelles (plante) 6 724 000 Bq/m² 630 000 Bq/m² Champignons Paxillus 29 680 000 Bq/m² 10 640 000 Bq/m² Champignons Russula 7 509 000 Bq/m² 3 683 000 Bq/m² Notes et références
- (en)Matpack – Periodic Table of the Elements Properties of Nuclides: 55-Cs-137.
- Selon l'IRSN, Au Japon comme en Europe, les niveaux maximaux de césiums radioactifs admissibles dans les denrées alimentaires sont de 500 Bq.kg-1 pour les légumes, les céréales, la viande, les œufs et le poisson, et de 200 Bq.kg-1 pour le lait, les produits laitierset les aliments liquides (Source : IRSN, Synthèse des informations disponibles sur la contamination radioactive de l’environnement terrestre japonais provoquée par l’accident de Fukushima Dai-ichi ; 27 septembre 2011, voir note page 8/11)
- Voir chapitre REPERE 1 : les normes de contamination des aliments en vigueur au JAPON, in Japon : chronique d’une contamination annoncée, CRIIRAD, Comm. Dimanche 20 mars 2011, consulté 2011-10-08
- ASN, Les normes de consommation et de commercialisation des produits alimentaires, page mise à jour le 10 Décembre 2009, consultée 2011-19-08
- P. Lestaevel, R. Racine, H. Bensoussan, C. Rouas, Y. Gueguen, I. Dublineau, J.-M. Bertho, P. Gourmelon, J.-R. Jourdain and M. Souidi Césium 137 : propriétés et effets biologiques après contamination interne Caesium 137: Properties and biological effects resulting of an internal contamination ; Médecine Nucléaire Volume 34, Issue 2, February 2010, Pages 108-118 doi:10.1016/j.mednuc.2009.12.003
- (en) Biological Half-life
- K Sperling, J Pelz, RD Wegner, I Schulzke and E Struck ; Frequency of trisomy 21 in Germany before and after the Chernobyl accident ; Biomedecine & Pharmacotherapy Volume 45, Issue 6, 1991, Pages 255-262 ; doi:10.1016/0753-3322(91)90026-P
- Ivan Zatsepina, Pierre Vergerb, Elisabeth Robert-Gnansiac, Corresponding Author Contact Information, E-mail The Corresponding Author, Bertrand Gagnièred, Margot Tirmarchee, Rostislav Khmela, Irina Babichevaa and Gennady Lazjukf ; Down syndrome time-clustering in January 1987 in Belarus: Link with the Chernobyl accident? ; in Reproductive Toxicology, Volume 24, Issues 3-4, Nov-Decr 2007, Pages 289-295 ; doi:10.1016/j.reprotox.2007.06.003
- Registre national du Bélarus des malformations congénitales (1981-2001)
- V Odlind, A Ericson ; Incidence of legal abortion in Sweden after the Chernobyl accident Biomedecine & Pharmacotherapy, Volume 45, Issue 6, 1991, Pages 225-228 ; doi:10.1016/0753-3322(91)90021-K
- SFEN, Accident de Tchernobyl - Conséquences dans d'autres pays européens - cas de la France (voir le paragraphe intitulé Activités des productions agricoles et produits naturels ; société française d'énergie nucléaire
- H. Maubert, D. Robeau, P. Renaud, I. Linge, O. Pavlovski et I. Ossipiants (Institut de protection et de sûreté nucléaire, CE Cadarache, Institut de Sûreté nucléaire de Moscou, ), Réflexions sur le respect des niveaux d'intervention dans un territoire contaminé par un dépôt accidentel de césium 137 , Radioprotection 1995, Vol. 30, n° 4, pages 495 à 508 ; Accepté : 4 Avril 1995 et révisé : 7 Février 1995, PDF, 14 pages (Résumé)
- Krivolutsky, D.A. 1994. Faune des sols et lutte écologique. Moscou, Fédération de Russie, Nauka. (en russe)
- Ipatyev, V. 2001. La construction de la «barrière biologique» dans les zones forestières contaminées par les radiations. Questions of Forest Sciences, 53: 153-158. (en russe)
- V.A. Ipatyev ; Réparer les dégâts de Tchernobyl: les forêts contaminées par les radiations et leur récupération ; les scientifiques cherchent à réduire les dangers des peuplements forestiers contaminés par les radiations, mais aucune solution à ce problème n'a encore été trouvée (lire l'article en ligne, en français) ; Revue UNASYLVA, FAO.
- Les conséquences de l'accident de Tchernobyl en France ; la contamination des produits agricoles Quelques cas particuliers de produits plus sensibles; Fiche information n° 8 : Direction de l’environnement et de l’intervention
- Samira Faroussi, Said Belali, Ahmed Fahli, Said Fakhi, Mustapha Khomsi and Said Laachir ; Modélisation de profil du 137Cs par un modèle applicable à différents types de sols non remaniés ; Comptes Rendus Geosciences, Volume 339, Issue 2, February 2007, Pages 143-149
- Lysikov, A.B. (1995): Der Einfluss der Wühl aktivität von Schwarzwild auf den Prozeß der Wanderung von Radionukliden im Boden nahe des Kernkraftwerks Tschernobyl. Schriftenreihe für Ökologie, Jagd und Naturschutz, Band 3, 99-105
- Département de la santé des Etats-Unis, Toxicological profile for cesium, U.S. Department of health and humain services, Public Health Service Agency for Toxic Substances and Disease Registry April 2004
- Ulf Hohmann and Ditmar Huckschlag, 2005, Investigations on the radiocaesium contamination of wild boar (Sus scrofa) meat in Rhineland-Palatinate: a stomach content analysis ; European Journal of Wildlife Research Volume 51, Number 4, 263-270, DOI: 10.1007/s10344-005-0108-x (Résumé en anglais)
- Stara JF. 1965. Tissue distribution and excretion of cesium-137 in the guinea pig after administration by three different routes. Health Phys 11:1195-1202.
- Stara JF, Thomas RG. 1963. The tissue distribution and excretion of cesium-137 following inhalation: Preliminary data for rats. AEC Res Dev Rep LF-4.
- Paris, Le sol, un patrimoine menacé ? Le point scientifique, Congrès : Forum, Paris, 24 octobre 1996
- Knut Hove, Hans Staaland & Øyvind Pedersen, Hexacyanoferrates and bentonite as binders of radiocaesium for reindeer, 6 pages
- Åhman, B., Forberg, S. & Åhman, G. Zeolite and bentonite as caesium binders in reindeer feed. - Rangifer, Special issue No. 3: 73-82.
- Daburon, F., Archimbaud, Y., Cousi, J. , Fayart, G., Hoffschir, D., Chevallereau, I. & Le Creff, H. 1991. Radiocaesium transfer to ewes fed contaminated hay after the Chernobyl Accident: Effect of vermiculite and AFCF (Ammonium Ferricyaferrate) as countermeasures. - Journal of Environmental Radioctivity, 14: 73-84
- Nigrovic, V. 1963. Enhancement of the excretion of radiocesium in rats by ferric cyanoferrate (II). - International Journal of Radiation Biology 7: 307-309.
Voir aussi
Articles connexes
- Césium
- Radioisotope
- Table des isotopes
- Essai nucléaire
- Catastrophe de Tchernobyl
- Radioactivité
- Toxicologie nucléaire
- Incendies de forêts en Russie en 2010
Liens externes
- (en) Argonne National Laboratory - Cesium [PDF]
- (en) Toxicological Profile for Cesium, ATSDR, U.S. Department of Health and Human Services.
s1 s2 g f1 f2 f3 f4 f5 f6 f7 f8 f9 f10 f11 f12 f13 f14 d1 d2 d3 d4 d5 d6 d7 d8 d9 d10 p1 p2 p3 p4 p5 p6 1 H He 2 Li Be B C N O F Ne 3 Na Mg Al Si P S Cl Ar 4 K Ca Sc Ti V Cr Mn Fe Co Ni Cu Zn Ga Ge As Se Br Kr 5 Rb Sr Y Zr Nb Mo Tc Ru Rh Pd Ag Cd In Sn Sb Te I Xe 6 Cs Ba La Ce Pr Nd Pm Sm Eu Gd Tb Dy Ho Er Tm Yb Lu Hf Ta W Re Os Ir Pt Au Hg Tl Pb Bi Po At Rn 7 Fr Ra Ac Th Pa U Np Pu Am Cm Bk Cf Es Fm Md No Lr Rf Db Sg Bh Hs Mt Ds Rg Cn Uut Uuq Uup Uuh Uus Uuo 8 Uue Ubn * Ute Uqn Uqu Uqb Uqt Uqq Uqp Uqh Uqs Uqo Uqe Upn Upu Upb Upt Upq Upp Uph Ups Upo Upe Uhn Uhu Uhb Uht Uhq Uhp Uhh Uhs Uho ↓ g1 g2 g3 g4 g5 g6 g7 g8 g9 g10 g11 g12 g13 g14 g15 g16 g17 g18 * Ubu Ubb Ubt Ubq Ubp Ubh Ubs Ubo Ube Utn Utu Utb Utt Utq Utp Uth Uts Uto Métalloïdes Non-métaux Halogènes Gaz rares Métaux alcalins Métaux alcalino-terreux Métaux de transition Métaux pauvres Lanthanides Actinides Superactinides Éléments non classés -
Wikimedia Foundation. 2010.

![\mathrm{^{137}_{\ 55}Cs\ \xrightarrow[30,07\ ans]{\beta^-\ 512,0\ keV}\ ^{137m}_{\ \ \ 56}Ba\ \xrightarrow [2,552\ min] {\gamma\ 661,7\ keV}\ ^{137}_{\ 56}Ba}](9/009fb48182ed49b16460f14bcba78d5e.png)