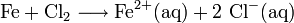- Corrosive
-
Corrosion
La corrosion désigne l'altération d'un matériau par réaction chimique avec un oxydant (le dioxygène et le cation H+ en majorité). Il faut en exclure les effets purement mécaniques (cela ne concerne pas, par exemple, la rupture sous l'effet de chocs) mais la corrosion intervient dans certaines formes d'usure des surfaces dont les causes sont à la fois physicochimiques et mécaniques.
Les exemples les plus connus sont les altérations chimiques des métaux dans l'eau, telles la rouille du fer et de l'acier ou la formation de vert-de-gris sur le cuivre et ses alliages (bronze, laiton). Cependant, la corrosion est un domaine bien plus vaste qui touche toutes sortes de matériaux (métaux, céramiques, polymères) dans des environnements variables (milieu aqueux, atmosphère, hautes températures).
L'étude fondamentale des phénomènes de corrosion relève essentiellement de l'électrochimie. L'étude appliquée des phénomènes de corrosion est un domaine de la science des matériaux, qui comporte à la fois des notions de chimie et de physique (physico-chimie).
La corrosion est un problème industriel important : le coût de la corrosion, qui recouvre l'ensemble des moyens de lutte contre la corrosion, le remplacement des pièces ou ouvrages corrodés et les conséquences directes et indirectes des accidents dus à la corrosion, est estimé à 2% du produit brut mondial) [1]. Chaque seconde, ce sont quelques 5 tonnes d'acier qui sont ainsi transformées en oxydes de fer...
Sommaire
Corrosion des métaux
La corrosion des métaux est un phénomène naturel.En effet, à quelques rares exceptions près (l'or et plus généralement tous les métaux nobles (platine, or, iridium, osmium, ruthénium, rhodium, palladium et argent) que l'on trouve à l'état natif naturellement, ce qui est du à leur potentiel standard d'oxydo-réduction positif, (cuivre, argent, fer de provenance météoritique), le métal est présent sur Terre sous forme d'oxyde, dans les minerais (bauxite pour l'aluminium, hématite pour le fer). Depuis la préhistoire, le travail de métallurgie a consisté à réduire ces oxydes dans des bas-fourneaux puis des hauts-fourneaux pour fabriquer le métal. La corrosion n'est qu'un retour à l'état d'oxyde naturel.
La corrosion des métaux est dans la grande majorité des cas une réaction électrochimique (une oxydo-réduction) qui fait intervenir la pièce manufacturée et l'environnement.
Exemples de corrosion de contact (à propos de ce phénomène, voir la page de discussion) :
Le matériau dont est fait la pièce n'est pas le seul facteur conditionnant la vitesse du processus d'oxydation, puisque la forme de la pièce et les traitements subis (mise en forme, soudure, vissage) jouent un rôle primordial. Ainsi, un assemblage de deux métaux différents (par exemple deux nuances d'acier, ou le même acier traité différemment) peut créer une corrosion accélérée ; on voit d'ailleurs souvent des traces de rouille au niveau des écrous. Si la pièce présente un interstice (par exemple entre deux plaques), cela pourra former un milieu confiné qui évoluera différemment du reste de la pièce et donc pourra aboutir à une corrosion locale accélérée. Toute hétérogénéité peut conduire à une corrosion locale accélérée, comme par exemple aux cordons de soudure. L'hétérogénéité de l'environnement auquel est soumis une pièce métallique de composition régulière peut susciter une corrosion dite par 'pile de concentration'. Il en est de même pour une pièce métallique localisée dans une solution de composition identique mais connaissant des agitations non-uniformes. Une plaque métallique partiellement immergée subira une corrosion localisée dite 'à la ligne d'eau'.
Approche de la protection contre la corrosion
La corrosion est donc un phénomène qui dépend du matériau utilisé, de la conception de la pièce (forme, traitement, assemblage) et de l'environnement. Le processus de corrosion peut également être ralenti en agissant sur la réaction chimique en elle-même.
Exemple de formule de corrosion
Cette formule correspond par exemple à la réaction de corrosion des canalisations métalliques d'eau potable par le dichlore gazeux servant initialement à détruire les microorganismes. Il ne faut pas faire l'amalgame avec l'effet des ions chlorures de l'eau de mer sur la vitesse de corrosion (cf. article passivation).
L’atmosphère contient des acides HNO3, H2SO4, etc., résidus de combustion. Ces acides attaquent les métaux :
Ces phénomènes sont à la base de la corrosion atmosphérique qui n'a d'ailleurs pas lieu en absence d'humidité dans l'air.
L’oxygène de l’air, en présence d’eau, oxyde le fer et peut former divers oxydes. Selon les conditions chimiques, il forme divers oxydes ou hydroxydes qui peuvent être soit non-protecteurs, soit modérément protecteurs. Par exemple Fe(OH)3, n H2O : la rouille, cet hydroxyde est poreux et ne protège pas le fer. Mais en milieu réducteur (peu ou pas d'oxygène) neutre ou modérément basique, c'est l'eau qui oxyde le fer ; on peut alors obtenir la magnétite Fe3O4, qui elle est modérément protectrice. L’acier inoxydable, communément désigné par "acier inox", contient du chrome, au minimum 12 % poids : les oxydes qui se forment en surface de l’alliage (avec une forte proportion d'oxyde de chrome de type Cr2O3) gênent la progression de l’oxygène ou le transfert d'électrons nécessaire à l'oxydation, on parle alors de passivation. Le terme indique un net ralentissement de la vitesse de corrosion par rapport à la cinétique initiale de corrosion. Toutefois, la corrosion n'est pas annulée mais fortement ralentie, de quelques ordres de grandeur. L'effet protecteur du chrome croit en général avec sa teneur. Un minimum de 12 % est nécessaire, mais les aciers destinés à des environnement agressifs, par exemple en présence de chlorures ou vers les milieux acides, ont des teneurs plus élevées, jusqu'à 25 % par exemple. L'ajout de molybdène a aussi un effet passivant très élevé, plus même que celui du chrome (1% Mo ~ 2,5% Cr).
Choix du matériau
La première idée est de choisir un matériau qui ne se corrode pas dans l'environnement considéré. On peut utiliser des aciers inoxydables, des aluminiums, des céramiques, des polymères (plastiques)... Le choix doit aussi prendre en compte les contraintes de l'application (masse de la pièce, résistance à la déformation, à la chaleur, capacité à conduire l'électricité…). Dans l'absolu, il n'existe pas de matériau réellement inoxydable.
Le terme d'«acier inoxydable» est impropre pour deux raisons : ce type d'acier contient des éléments d'alliage (chrome, nickel) qui s'oxydent (c'est cette couche d'oxyde qui protège l'acier), et d'autre part, il n'est protégé que pour certains types d'environnement, et sera corrodé dans d'autres environnements.
Il existe de multiples nuances d'aciers dits «inoxydables» désignés par des noms tels que «304», «304L», «316N» etc., qui correspondent à la norme américaine AISI, appelés aussi sous la norme AFNOR respectivement Z6CN18-10, Z3CN18-10 Z6CN17-12Mo. Z indique la teneur en carbone (Z6 = 0.06 %) C le pourcentage en chrome et N en nickel. Le Z6CN17-12Mo contient du molybdène, il est plus passif que le Z6CN18-10. Chaque acier correspond à certains types d'environnements, son utilisation dans d'autres environnements pourraît être catastrophique.
Conception de la pièce
Dans la conception, il faut s'attacher à éviter les zones de confinement, les contacts entre matériaux différents et les hétérogénéités en général.
Il faut aussi prévoir l'importance de la corrosion, et le temps au bout duquel il faudra changer la pièce (maintenance préventive).
Maîtrise de l'environnement
Dans un environnement fermé (par exemple un circuit fermé d'eau), il devient possible de maîtriser les paramètres ayant une influence sur la corrosion : composition chimique (notamment acidité), température, pression... Il existe également des produits dits « inhibiteurs de corrosion ».
Ce type de solutions est inapplicable en milieu ouvert (atmosphère, mer, bassin en contact avec le milieu naturel, circuit ouvert).
Empêcher la réaction chimique
Il existe deux moyens d'empêcher la réaction chimique d'avoir lieu :
- On peut tout d'abord isoler la pièce de l'environnement (par une couche de peinture, de matière plastique, ou par un traitement de surface : nitruration, chromatation, projection plasma).
- Il est aussi possible d'introduire une autre pièce pour ralentir ou empêcher la réaction ; c'est le principe de la protection cathodique. Un premier moyen de la réaliser est d'utiliser une « anode sacrificielle ». Cette nouvelle pièce (souvent en zinc ou magnésium) abaisse en effet le potentiel électrochimique de la pièce protégée en dessous du potentiel ou il peut s'oxyder, et va se corroder à la place de la pièce à protéger. En milieu aqueux, il suffit de visser ou de mettre en contact l'anode sacrificielle sur la pièce à protéger. Si la pièce est de grande dimension, il faut cependant tenir compte d'une déperdition de protection liée à la chute ohmique. Celle-ci est provoquée par la résistance au passage du courant dans le milieu environnant, et elle augmente avec la distance du point de la pièce protégée au contact avec l'anode sacrificielle. Au-delà d'une certaine distance, qui dépend de la conductivité du milieu, la pièce n'est plus protégée. Il faut donc positionner les anodes à distance régulière de manière à ce que tout point se situe en dessous du potentiel ou le métal peut de corroder. C'est ce qui est réalisé sur les grandes structures, par exemple les plateformes pétrolières offshore. Ces anodes sacrificielles se consomment et ont donc une durée de vie limitée, et nécessitent un remplacement périodique. À l'air, il faut entièrement recouvrir la pièce de zinc, c'est le principe de la galvanisation. Un deuxième moyen de réaliser la protection cathodique est d'abaisser le potentiel du métal avec une source électrique externe, en imposant un potentiel ou un courant entre la pièce et une anode externe positionnée au regard de la surface, mais sans contact direct avec le métal. Dans ce cas, l'anode ne se consomme pas et n'a pas besoin d'être remplacée.
Dans l'industrie automobile, on protège le fer en créant un réaction chimique avec celui-ci. Le produit, imperméable, protègera le métal: c'est la parkérisation.
Le chromage a été complètement abandonné[2]. En effet, le chrome en lui-même ne se corrodait pas, donc protégeait la pièce, mais la moindre rayure était catastrophique car la pièce jouait alors le rôle d'anode sacrificielle pour le chrome et se corrodait très rapidement. Les peintures anti-corrosion au plomb ont été également abandonnées en raison de leur impact sur l'environnement.
Notes
- ↑ Bernard Normand, Nadine Pébère, Caroline Richard, Martine Wery, Prévention et lutte contre la corrosion : une approche scientifique et technique, PPUR, 2004, 798 p. (ISBN 2-88074-543-8)
- ↑ attention à ne pas confondre le chromage, un dépôt de chrome, la chromatation, qui est la formation d'une couche de métal combiné à des ions chrome VI, et la chromisation, parfois appelée cémentation au chrome, qui est une diffusion d'atomes de chrome dans les couches superficielles d'un acier
Voir aussi
- Corrosion
- acier inoxydable
- Revêtement
- Protection cathodique
Liens externes
- Le livre multimedia de la corrosion (INSA Lyon)
- Le Forum International de Corrosion de Polymères et Composites
Bibliographie
- [ASM96] : Corrosion 5è éd., vol. 13 de ASM Handbook, éd. ASM International (American Society for Materials), 1996
- [Ben62] : L'Oxydation des métaux, J. Bénard et coll., éd. Gauthier-Villars, 1962
- [Kof88] : High Temperature Corrosion, P. Kofstad, éd. Elsevier, 1988
- [Lan93] : Corrosion et chimie de surfaces des métaux, D. Landolt, vol. 12 de Traité des matériaux, éd. Presses Polytechniques et Universitaires Romandes, 1993
- [Now92] : Diffusion in Solids and High Temperature Oxidation of Metals, éditeur J. Nowotny, éd. Trans Tech Publications, 1992
- [Phi98] : Métallurgie, du minerai au matériau, J. Philibert et coll., éd. Masson, 1998
- Portail de la physique
- Portail de la chimie
Catégories : Corrosion | Électrochimie -
Wikimedia Foundation. 2010.