- Calorimétrie différentielle à balayage
-
La calorimétrie différentielle à balayage (en anglais, Differential Scanning Calorimetry ou DSC) est une technique d'analyse thermique. Elle mesure les différences des échanges de chaleur entre un échantillon à analyser et une référence (par exemple alumine, mais peut aussi être de l'air).
Elle permet de déterminer les transitions de phase :
- la température de transition vitreuse (Tg) des polymères et des verres métalliques ;
- les températures de fusion et de cristallisation ;
- les enthalpies de réaction, pour connaître les taux de réticulation de certains polymères.
Les analyses sont réalisées sous balayage d'un gaz inerte (par exemple, l'azote ou l'argon) pour éviter toute réaction du matériau à étudier avec l’atmosphère du four.
L'appareil subit des changements de température importants. Par conséquence, la position de certains éléments de la DSC va varier. L'ensemble des calculs réalisés par l'interface informatique se fait par rapport au thermocouple positionné entre l'échantillon et la référence. En bougeant, les résultats vont être faussés. Il est donc nécessaire de calibrer régulièrement en vérifiant par exemple les températures de fusion à l'aide de l'indium, du zinc ou du plomb (généralement, on utilise l’indium - Tf = 156,6 °C ; ΔH = 28,45 J·g−1).
Sommaire
Fonctionnement
Principe
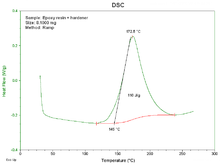 Thermogramme DSC : visualisation du pic exothermique correspondant à la réticulation d'un matériau polymère thermodurcissable, et calcul du taux de réticulation.
Thermogramme DSC : visualisation du pic exothermique correspondant à la réticulation d'un matériau polymère thermodurcissable, et calcul du taux de réticulation.
Cette technique se base sur le fait que lors d'une transformation physique, telle qu'une transition de phase, une certaine quantité de chaleur est échangée avec l'échantillon pour être maintenu à la même température que la référence. Le sens de cet échange de chaleur entre l'échantillon et l'équipement dépend de la nature endothermique ou exothermique du processus de transition. Ainsi, par exemple, un solide qui fond va absorber plus de chaleur pour pouvoir augmenter sa température au même rythme que la référence. La fusion (passage de l'état solide à l'état liquide) est en effet une transition de phase endothermique car elle absorbe la chaleur. De même, l'échantillon peut subir des processus exothermiques, tels que la cristallisation, lorsqu'il transmet de la chaleur au système.
En mesurant la différence de flux de chaleur entre l'échantillon et la référence, un calorimètre différentiel à balayage peut mesurer la quantité de chaleur absorbée ou libérée au cours d'une transition. Cette technique peut également être utilisée pour observer des changements de phase plus subtils, comme les transitions vitreuses.
La DSC est largement utilisée en milieu industriel en contrôle qualité en raison de son applicabilité dans l'évaluation de la pureté d'échantillons ou dans l'étude du durcissement de polymères[1],[2].Méthode par compensation
Dans cette méthode (initialement inventée par PerkinElmer), l'échantillon et la référence sont placés dans deux fours différents mais dans la même enceinte calorifique. La variation de température entre les deux fours se fait simultanément par la même quantité de calories. La température est maintenue toujours égale dans les deux fours, et varie de manière linéaire.
Les différences des énergies absorbées ou dégagées par l'échantillon et la référence sont mesurées. Lorsqu'une transition se produit, selon qu'elle soit endothermique ou exothermique, l'échantillon va absorber ou dégager de l'énergie. Un générateur de puissance fournit plus ou moins d'énergie par rapport à la référence. C'est cette variation d'énergie qui est enregistrée en fonction du temps ou de la température.Méthode des flux de chaleur
Pour cette méthode (mise au point par Du Pont de Nemours-Mettler), l'échantillon et la référence sont placés dans un même four. Une sonde de platine permet de contrôler et d'enregistrer l'évolution de la température de l'appareil. Le signal température est ensuite converti en signal de puissance calorifique.
Cette technique mesure les différences de flux de chaleur entre l'échantillon et la référence pendant un cycle de température. La température de chauffe, fournie par une résistance électrique, varie linéairement.
Comparaison avec l'analyse thermique différentielle
La calorimétrie différentielle à balayage et l'analyse thermodifférentielle (ATD) sont très souvent confondues. Il existe pourtant une différence fondamentale entre ces deux méthodes. Avec un appareil de DSC, on mesure des différences d'énergie, tandis qu'avec l' ATD, on mesure des différences de température.
L'ATD est très peu utilisée pour la caractérisation de polymères car les signaux issus des changements de phase ou d'état de la matière sont de très faible amplitude[3].Notes et références
- John A. Dean, The Analytical Chemistry Handbook, New York, McGraw-Hill, 1995, p. 15.1–15.5
- Erno Pungor, A Practical Guide to Instrumental Analysis, Boca Raton, 1995, p. 181–191
- Douglas A. Skoog, F. James Holler et Timothy Nieman, Principles of Instrumental Analysis, New York, 1998, p. 905
Annexes
Articles connexes
Techniques d'Analyse Thermique :
Wikimedia Foundation. 2010.

