- Chlorure de benzalkonium
-
Chlorure de benzalkonium 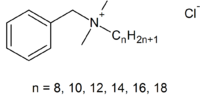
Général No CAS No EINECS Propriétés physiques Solubilité très sol. dans l'eau, l'alcool, l'acétone;
Presq'insol dans l'éther;
1g d'anhydre dans 6ml de benzène, 100ml d'éther[1]Masse volumique 0,9884 g·cm-3 (50%, 20 °C)[1] Unités du SI & CNTP, sauf indication contraire. Le chlorure de benzalkonium, aussi connu sous le nom de chlorure d'alkyldiméthylbenzylammonium et ADBAC, est un mélange de chlorures d'alkylbenzyldiméthylammonium avec des chaînes carbonées de longueur variable[2]. Ce produit est un agent de surface cationique de la famille des ammoniums quaternaires.
Sommaire
Propriétés physico-chimiques
Le chlorure de benzalkonium est facilement soluble dans l'éthanol et l'acétone. Bien que la dissolution dans l'eau soit lente, les solutions aqueuses sont plus faciles d'emploi et sont plus largement utilisées. Les solutions devraient être neutres à légèrement basiques avec une couleur allant de l'incolore au jaune pâle. Les solutions moussent fortement lorsqu'elles sont secouées[1], ont un goût amer et ont une odeur d'amande détectable seulement dans les échantillons concentrés.
Utilisation
Les applications sont très variées, allant de la formulation de désinfectants à l'inhibition de corrosion microbienne dans les huiles[3]. Il est utilisé dans les produits pharmaceutiques tels que les solutions cutanées antiseptiques ou les lingettes. Il est utilisé comme conservateur dans les cosmétiques tels que les gouttes pour les yeux et le nez. On a reporté des cas de sensibilisations associées à l'utilisation continue et prolongée du produit. En tant qu'antiseptique il a l'avantage de ne pas brûler les plaies à l'application, contrairement aux antiseptiques à base d'éthanol ou d'eau oxygénée.
Disponibilité
Les concentrés standard sont fabriqués sous forme de solutions à 50 et 80%m. Les solutions à 50% sont purement aqueuses, tandis que les solutions plus concentrées requièrent l'incorporation d'additifs tels que des alcools, du polyéthylène glycol, etc. pour éviter l'augmentation de la viscosité ou la formation de gels à basse température.
Activité biologique
L'activité biocide la plus importante est associée aux dérivés alkylés en C12 à C14. On pense que le mécanisme bactéricide est dû à la disruption des interactions intermoléculaires. Ceci peut causer la dissociation des lipides dans la membrane cellulaire, ce qui compromet la perméabilité de la cellule et induit une fuite de son contenu. D'autres complexes biomoléculaires à l'intérieur de la cellule bactérienne peuvent aussi se dissocier. Les enzymes, qui contrôlent les activités respiratoire et métaboliques de la cellule sont particulièrement susceptibles d'être désactivées.
Les solutions de chlorure de benzalkonium sont des agents bactéricides à action rapide et de durée modérément longue. Ils sont actifs contre certains et certaines bactéries, virus, fungi et protozoaires. Les spores des bactéries sont considérées comme résistantes. Les bactéries à Gram positif sont généralement plus sensibles que les Gram négatif. L'activité n'est pas grandement influencée par le pH, mais augmente aux températures élevées et avec la durée d'exposition.
De nouvelles formulations utilisant du benzalkonium mélangé à d'autres ammoniums quaternaires peuvent être utilisées pour étendre le spectre biocide et augmenter l'efficacité du désinfectant. Cette technique a été utilisée pour améliorer l'activité virucide.
L'utilisation d'excipients appropriés peut améliorer l'efficacité et les propriétés détergentes, et éviter la désactivation lors de l'utilisation. La formulation requiert beaucoup de soin car les solutions de benzalkonium peuvent être désactivées en présence de contaminants organiques et inorganiques. Les solutions sont incompatibles avec les savons, les nitrates[1] et ne doivent pas être mélangées avec des surfactants anioniques. Les sels des eaux dures peuvent aussi réduire l'activité biocide. Comme pour tous les désinfectants, il est recommandé de traiter des surfaces sans saletés visibles.
Bien que des niveaux dangereux ne puissent être atteints dans les conditions d'utilisation normale, le benzalkonium et les autres détergents peuvent être néfastes aux organismes marins. Les désinfectants à base d'ammoniums quaternaires sont actifs à faible concentration, si bien que des doses excessives devraient être évitées.
Le chlorure de benzalkonium a aussi une activité spermicide
Sécurité
Le chlorure de benzalkonium est hautement toxique pour les poissons (CL50 = 280 μg ai/L), très toxique pour les invertébrés aquatiques (CL50 = 5,9 μg ai/L), modérément toxique pour les oiseaux (DL50 = 136 mg par kg de poids corporel), et légèrement toxique pour les mammifères (DL50 = 430 mg/kg pc)[4]. Les solutions de chlorure de benzalkonium de 10% ou plus sont toxiques pour les humains, causant l'irritation de la peau et des muqueuses. Elles peuvent provoquer la mort après ingestion[5]
Le chlorure de benzalkonium est un allergène[6],[7],[8],[9],[10],[11],[12] et quelques études ont jeté le doute sur sa réputation de composé sans danger[13],[14]. Quelques produits ont été reformulés en tenant compte de ces études mais il est toujours utilisé pour laver les yeux, dans les sprays pour laver le nez, les mains, le visage, dans les bains de bouche, les crèmes spermicides et dans d'autres produits de nettoyage, de désinfection... Certains fabricants de gouttes pour les yeux, concernés par les problèmes d'allergies lors de l'usage à long terme du benzalkonium, l'ont remplacé par de l'EDTA. D'autres ont créé des gouttes pour les yeux dans des emballages individuels à usage unique sans conservateur[15].
Les solutions des lentilles de contact contiennent typiquement 0,002% à 0,01% de chlorure de benzalkonium[16]. K. C. Swan[17] a trouvé que l'usage répété de chlorure de benzalkonium à des concentrations de 1:5000 (0,02%) ou supérieures peuvent dénaturer la protéine cornéenne et causer des dommages irréversibles aux yeux. Les désavantages de l'utilisation du chlorure de benzalkonium avec les lentilles de contact sont aussi discutés dans la littérature[18],[19]
D'après une étude menée en 2009, le chlorure de benzalkonium induit une résistance de la bactérie Pseudomonas aeruginosa à l'antibiotique ciprofloxacine[20].
Notes et références
- Benzalkonium chloride sur Hazardous Substances Data Bank. Consulté le 20 février 2010
- U.S. Environmental Protection Agency : Reregistration Eligibility Decision for Alkyl Dimethyl Benzyl Ammonium Chloride (ADBAC)
- Benzalkonium Chloride Solutions, QuatChem Limited, 2009. Consulté le 2009-03-06
- Modèle:Cite report
- (en) Seymour Stanton Block, Disinfection, sterilization, and preservation, Lippincott Williams & Wilkins, 2001, 5, illustratede éd. [lire en ligne], p. 311
- Park HJ, Kang HA, Lee JY, Kim HO, « Allergic contact dermatitis from benzalkonium chloride in an antifungal solution », dans Contact Derm., vol. 42, no 5, 2000, p. 306–7 [lien PMID]
- Liu H, Routley I, Teichmann KD, « Toxic endothelial cell destruction from intraocular benzalkonium chloride », dans J Cataract Refract Surg, vol. 27, no 11, 2001, p. 1746–50 [lien PMID, lien DOI]
- Chiambaretta F, Pouliquen P, Rigal D, « [Allergy and preservatives. Apropos of 3 cases of allergy to benzalkonium chloride] », dans J Fr Ophtalmol, vol. 20, no 1, 1997, p. 8–16 [lien PMID]
- Wong DA, Watson AB, « Allergic contact dermatitis due to benzalkonium chloride in plaster of Paris », dans Australasian J. Dermatology, vol. 42, no 1, 2001, p. 33–5 [lien PMID, lien DOI]
- Kanerva L, Jolanki R, Estlander T, « Occupational allergic contact dermatitis from benzalkonium chloride », dans Contact Derm., vol. 42, no 6, 2000, p. 357–8 [lien PMID]
- Oiso N, Fukai K, Ishii M, « Irritant contact dermatitis from benzalkonium chloride in shampoo », dans Contact Derm., vol. 52, no 1, 2005, p. 54 [lien PMID, lien DOI]
- Basketter DA, Marriott M, Gilmour NJ, White IR, « Strong irritants masquerading as skin allergens: the case of benzalkonium chloride », dans Contact Derm., vol. 50, no 4, 2004, p. 213–7 [lien PMID, lien DOI]
- Graf P, « Benzalkonium chloride as a preservative in nasal solutions: re-examining the data », dans Respir Med, vol. 95, no 9, 2001, p. 728–33 [lien PMID, lien DOI]
- Marple B, Roland P, Benninger M, « Safety review of benzalkonium chloride used as a preservative in intranasal solutions: an overview of conflicting data and opinions », dans Otolaryngol Head Neck Surg, vol. 130, no 1, 2004, p. 131–41 [lien PMID, lien DOI]
- Use of benzalkonium in ocular preparations and eye drops
- U.S. Patent 5,725,887, column 2, line 8
- Swan, K. C., "Reactivity of the Ocular Tissues to Wetting Agents", Am. J. Ophthalmol., 27, 118 (1944),
- M. Orton, et al., "Measurement of Preservative Binding with Polymacon Contact Lens", Aust J Optom, 59, 277 (1976)
- M Akers, "Consideration in selecting antimicrobial preservative agents for parenteral product development", Pharmaceutical Technology, May, p. 36 (1984).
- DOI:10.1099/mic.0.029751-0
- Bernstein IL: Is the use of benzalkonium chloride as a preservative for nasal formulations a safety concern? J Allergy Clin Immunol 2000 Jan; 105(1 Pt 1): 39-44.
- Graf P: Adverse effects of benzalkonium chloride on the nasal mucosa: allergic rhinitis and rhinitis medicamentosa. Clin Ther 1999 Oct; 21(10): 1749-55.
- Graf P, Hallen H, Juto JE: Benzalkonium chloride in a decongestant nasal spray aggravates rhinitis medicamentosa in healthy volunteers. Clin Exp Allergy 1995 May; 25(5): 395-400.
Wikimedia Foundation. 2010.
