- TLRs
-
Récepteur de type Toll
 Pour les articles homonymes, voir TLR.
Pour les articles homonymes, voir TLR.Les récepteurs de type Toll (ou Toll-like receptors ou TLRs) appartiennent à la grande famille des PRRs (1-3) (Pattern-Recognition Receptors).
En tant que tels, ils interviennent au cours des mécanismes de l’immunité innée en reconnaissant des « motifs moléculaires conservés » chez de nombreux pathogènes.
Ces motif appelés PAMPs (Pathogen-Associated Molecular Patterns) sont d’origine très diverse (bactérie, virus, parasite) et de nature variée (protéine, ose, acide nucléique).Sommaire
Phylogénie
Les TLRs sont présents chez les mammifères et de nombreux vertébrés (poissons osseux ou cartilagineux, amphibiens, reptiles et oiseaux), mais également chez les invertébrés et chez certaines plantes sous des formes structurales cependant légèrement différentes.
Ainsi, du point de vue évolutif, les TLRs semblent constituer un des plus anciens composants du système immunitaire et serait apparu avant même la séparation entre les animaux et les végétaux.
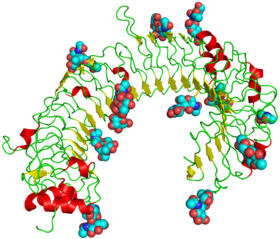
Structure
La structure des TLRs est assez simple. Ce sont des protéines transmembranaires de type I comportant :
- Un domaine extracellulaire récepteur du signal de danger et composé de nombreux motifs LRRs (Leucin-Rich Repeats)
- Un domaine transmembranaire
- Un domaine intracellulaire contenant un Death Domain permettant la transduction du signal d’activation
Découverte
Le nom de TLR vient de l’homologie avec une famille de molécules retrouvée chez la drosophile Drosophila melanogaster, dont le principal membre est Toll. (« Toll » en allemand signifie « étonnant » ou « cool »). Chez la drosophile, Toll a initialement été identifié comme un gène important lors de l’embryogenèse, et en particulier, lors de la mise en place de l’axe dorso-ventral (4). En 1996, Jules Hoffmann et son équipe montre que Toll participe également à l‘immunité anti-fongique chez la drosophile (5).
A l’époque de cette découverte, les TLRs sont connus chez les mammifères grâce à l’identification chromosomique de TIL (maintenant appelé TLR1) en 1996 par l’équipe de Taguchi (6). A l’époque, étant donné ce qui est connu de Toll chez la drosophile, des hypothèses avancent un rôle de TIL dans le développement embryonnaire des mammifères. Par ailleurs, une autre molécule avec un rôle évident dans l’immunité des mammifères, le récepteur à l’interleukine 1 (IL-1R) a au préalable été décrite par Nick Gay en 1991 et en particulier, l’homologie du domaine cytoplasmique avec celui de Toll (7).
Charles Janeway et ses collaborateurs identifient un second paralogue TLR en 1997 qu’ils appellent « h-Toll » (maintenant TLR4) (8). En reprenant les travaux d’Hoffmann, ils suggèrent que chez les mammifères, h-Toll pourrait « activer l’immunité adaptative ». La fonction précise de TLR4 est découverte en 1998 par le groupe de Bruce Beutler qui, par l’utilisation d’une technique génétique appelée « clonage positionnel », prouve le rôle de TLR4 en tant que récepteur du lipopolysaccharide bactérien (connu également comme « endotoxine » ou LPS). Jusqu’alors, le LPS était connu depuis plus de cent ans pour ses puissants effets inflammatoires et immunomodulateurs. En étudiant les conséquences de la perte de ce TLR chez des souris invalidées pour le TLR4, Beutler conclue à la spécificité de reconnaissance du LPS par TLR4. Cette observation suggère fortement que chez les Mammifères, chaque TLR pourrait reconnaître une molécule bien particulière témoignant d’une infection en cours.
Il apparaît maintenant que cette proposition était correcte et que les TLRs représentent chez les mammifères des protéines clés permettant de détecter une infection et de déclencher la réponse immune.
Diversité
La plupart des espèces de mammifères ont entre dix et quinze types de TLRs. Treize TLRs (appelés simplement TLR1 à TLR13) ont été identifiés chez l’Homme et la Souris tandis que des formes équivalentes ont été trouvées chez d’autres espèces. Cependant, certains TLRs sont spécifiques de l’Homme. Par exemple, un gène codant un analogue de TLR10 chez l’Homme est présent chez la Souris mais semble avoir été endommagé dans le passé par un rétrovirus. La Souris exprime par contre TLR11, TLR12 et TLR13, TLRs inexistants chez l’Homme (3).
Les TLRs apparaissent sous la forme de dimère. Alors que la plupart des TLRs sont des homodimères, TLR2 a la particularité de s’associer en hétérodimère avec TLR1 ou TLR6, chaque hétérodimère présentant une spécificité de ligand différente. Quand un TLR est activé, il recrute une molécule adaptatrice pour propager le signal au niveau du Death Domain. A ce jour, quatre adaptateurs sont connus dans la signalisation TLR : MyD88, TIRAP (aussi appelé MAL), TRIF et TRAM. Ces adaptateurs activent d’autres molécules au sein de la cellule, y compris certaines protéines kinases (IRAK1, IRAK4, TBK1 et IKKi) qui amplifient le signal et finalement conduisent à l’induction ou la suppression de gènes qui orchestrent la réponse inflammatoire. Ainsi, des milliers de gènes sont activés par la signalisation TLR qui contient un potentiel de modulation de gènes à la fois puissant et extrêmement fin.
Les TLRs peuvent aussi dépendre d’autres co-récepteurs pour la sensibilité totale au ligand, comme dans le cas de la reconnaissance du LPS par le TLR4 qui requiert MD-2. CD14 et les protéines liant le LPS (LBP pour LPS Binding Protein) sont par ailleurs connus pour faciliter la présentation du LPS par MD-2.
Parce que la spécificité des récepteurs Toll-like (et d’autres récepteurs de l’immunité innée) ne peut pas être facilement changée au cours de l’évolution, ces récepteurs doivent reconnaître des molécules qui sont constamment associées à des menaces microbiennes, non sujettes à des mutations, et spécifiques de ces menaces (i.e qu’on ne peut normalement pas trouver dans l’hôte où le TLR est présent). Ces PAMPs sont essentiels à la biologie du pathogène et ne peuvent être éliminés ou changés par mutation, ils sont donc conservés du point de vue évolutif. Les motifs conservés chez les pathogènes incluent les lipopolysaccharides de la paroi des bactéries (LPS), les lipoprotéines, les lipopeptides et les lipoarabinomannanes ; les protéines comme la flagelline des flagelles bactériens ; l’ARN double brin des virus ou de trématode comme Schistosoma mansoni (9) et les îlots CpG non-méthylés de l’ADN bactérien et viral. Voir le tableau ci-dessous pour un résumé de l’activité TLR décrite jusqu’à présent.
Bilan des récepteurs Toll-like connus chez les Mammifères
Récepteurs Ligand(s) naturel(s) Adaptateurs TLR1 triacyl des lipoprotéines MyD88/MAL TLR2 lipoprotéines, peptidoglycane des bactéries Gram+, acides lipotéichoïques, champignons, glycoprotéines virales MyD88/MAL TLR3 ARN double brin d’origine virale ou parasitaire TRIF TLR4 lipopolysaccharide, glycoprotéines virales MyD88/MAL/TRIF/TRAM TLR5 flagelline MyD88 TLR 6 diacyl des lipoprotéines MyD88/MAL TLR 7 ARN simple brin MyD88 TLR 8 ARN simple brin MyD88 TLR 9 ADN CPG non-méthylés MyD88 TLR 10 inconnu inconnu TLR 11 profiline MyD88 TLR 12 inconnu inconnu TLR 13 inconnu inconnu Activation et effets
Suivant l’activation par des ligands d’origine microbienne, diverses réactions sont possibles. Les cellules de l’immunité peuvent produire des facteurs de signalisation appelés cytokines qui induisent une inflammation. Dans le cas d’un facteur bactérien, le pathogène peut être phagocyté et digéré ; ces antigènes sont alors présentés aux cellules T CD4+. Dans le cas d’un facteur viral, la cellule infectée peut éteindre sa synthèse protéique et rentrer dans la mort cellulaire programmée (apoptose). Les cellules de l’immunité qui ont détecté un virus peuvent aussi relarguer des facteurs anti-viraux appelés interférons.
La découverte des récepteurs Toll-like a finalement identifié les récepteurs de l’immunité innée comme responsable de nombreuses fonctions de l’immunité découvertes auparavant. Les TLRs semblent être seulement impliqués dans la production en cytokine et l’activation cellulaire en réponse aux microbes et ne jouent aucun rôle dans l’adhésion ou la phagocytose des micro-organismes.
Modèle de danger
Plus récemment, les TLRs ont été suspectés de se lier à des facteurs non-pathogènes produits durant la maladie, le stress ou un traumatisme. On peut citer par exemple le fibrinogène (impliqué dans le processus de coagulation) et les protéines de choc thermique (HSPs pour Heat Shock Proteins) (générées lors d’un stress thermique comme la fièvre). Ceci est la base du modèle immunitaire du « Model de Danger » de Polly Matzinger. Cet auteur suggère que ces signatures moléculaires sont reconnues et associées à un risque accru de maladie ou la maladie elle-même, et mettent le système immunitaire en alerte via l’activation des TLRs. Cependant, ce modèle est controversé (10-12).
Voir aussi
Articles connexes
Liens externes
Bibliographie
- 1. Akira, S. 2006. TLR signaling. Curr Top Microbiol Immunol 311:1.
- 2. Akira, S., and K. Takeda. 2004. Toll-like receptor signalling. Nat Rev Immunol 4:499.
- 3. Akira, S. 2003. Mammalian Toll-like receptors. Curr Opin Immunol 15:5.
- 4. Lemaitre, B., E. Nicolas, L. Michaut, J. M. Reichhart, and J. A. Hoffmann. 1996. The dorsoventral regulatory gene cassette spatzle/Toll/cactus controls the potent antifungal response in Drosophila adults. Cell 86:973.
- 5. Hoffmann, J. A., J. M. Reichhart, and C. Hetru. 1996. Innate immunity in higher insects. Curr Opin Immunol 8:8.
- 6. Taguchi, T., J. L. Mitcham, S. K. Dower, J. E. Sims, and J. R. Testa. 1996. Chromosomal localization of TIL, a gene encoding a protein related to the Drosophila transmembrane receptor Toll, to human chromosome 4p14. Genomics 32:486.
- 7. Gay, N. J., and F. J. Keith. 1991. Drosophila Toll and IL-1 receptor. Nature 351:355.
- 8. Medzhitov, R., P. Preston-Hurlburt, and C. A. Janeway, Jr. 1997. A human homologue of the Drosophila Toll protein signals activation of adaptive immunity. Nature 388:394.
- 9. Aksoy, E., C. S. Zouain, F. Vanhoutte, J. Fontaine, N. Pavelka, N. Thieblemont, F. Willems, P. Ricciardi-Castagnoli, M. Goldman, M. Capron, B. Ryffel, and F. Trottein. 2005. Double-stranded RNAs from the helminth parasite Schistosoma activate TLR3 in dendritic cells. J Biol Chem 280:277.
- 10. Matzinger, P. 2002. An innate sense of danger. Ann N Y Acad Sci 961:341.
- 11. Matzinger, P. 2002. The danger model: a renewed sense of self. Science 296:301.
- 12. Matzinger, P. 2001. Introduction to the series. Danger model of immunity. Scand J Immunol 54:2.
- 13. Beutler, B., Z. Jiang, P. Georgel, K. Crozat, B. Croker, S. Rutschmann, X. Du, and K. Hoebe. 2006. Genetic analysis of host resistance: Toll-like receptor signaling and immunity at large. Annu Rev Immunol 24:353.
- 14. Hasan, U., C. Chaffois, C. Gaillard, V. Saulnier, E. Merck, S. Tancredi, C. Guiet, F. Briere, J. Vlach, S. Lebecque, G. Trinchieri, and E. E. Bates. 2005. Human TLR10 is a functional receptor, expressed by B cells and plasmacytoid dendritic cells, which activates gene transcription through MyD88. J Immunol 174:2942.
- 15. Lauw, F. N., D. R. Caffrey, and D. T. Golenbock. 2005. Of mice and man: TLR11 (finally) finds profilin. Trends Immunol 26:509.
Notes et références
- Article “Toll-like receptors” de la version anglaise de Wikipedia.
- Portail de la biologie cellulaire et moléculaire
Catégories : Immunologie | Récepteur (cellule)
Wikimedia Foundation. 2010.