- Principe de Pauli
-
Principe d'exclusion de Pauli
En 1925,[1] Wolfgang Pauli proposa un principe selon lequel les fermions (particules de spin semi-entier telles que les électrons, protons ou neutrons), ne peuvent pas se trouver au même endroit dans le même état quantique.
Ce principe devint un théorème en mécanique quantique relativiste, inventée par Dirac en 1930 : les particules de spin demi-entiers sont des fermions et obéissent à la statistique de Fermi-Dirac, donc au principe d'exclusion de Pauli.
Sommaire
Énoncé en mécanique quantique
L'état quantique d'une particule est défini par des « nombres quantiques ». Le principe d'exclusion interdit à tout fermion appartenant à un système de fermions d'avoir les mêmes nombres quantiques qu'un autre fermion du système.
Par exemple, dans l'atome, les électrons sont caractérisés par les nombres correspondant aux lettres n, l, ml et ms : si un électron présente la combinaison (1, 0, 0, ½), il est nécessairement le seul.
Cela limite donc le nombre d'électrons par couche : dans la première couche caractérisée par n = 1, (l = 0, donc ml= 0), il n'y a que deux possibilités, correspondant aux états ms=±½. Cette couche ne peut donc accepter que deux électrons.
De même, dans la seconde couche caractérisée par n = 2, l vaut 0 ou 1 :
- pour l = 0, ml = 0 ;
- pour l = 1, ml = -1, 0 ou 1 ;
on a alors 4 possibilités et pour chacune, ms=±½, donc la seconde couche peut accepter huit électrons (deux pour l = 0 et six pour l = 1); et ainsi de suite. La n-ième couche accepte 2n² configurations.
Dérivation des principes de la mécanique quantique
Lorsque Pauli a proposé le principe d'exclusion (1925), les principes fondamentaux de la mécanique quantique n'étaient pas encore bien établis. En fait, il apparait que le principe d'exclusion n'est pas un principe fondamental et peut se dériver des principes fondamentaux de la mécanique quantique.
Voici une dérivation du principe d'exclusion de Pauli[2] :
Soit un hamiltonien total, représentant l'état de 2 particules (l'extension à N particules est immédiate) :
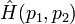 .
.Si p1 et p2 sont deux particules indiscernables, alors
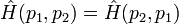 . On dit alors que le hamiltonien est invariant par permutation, et si l'on considère
. On dit alors que le hamiltonien est invariant par permutation, et si l'on considère 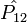 qui est l'opérateur de permutation de la particule p1 et p2, alors le commutateur de ces deux opérateurs est nul :
qui est l'opérateur de permutation de la particule p1 et p2, alors le commutateur de ces deux opérateurs est nul : ![[\hat{H},\hat{P_{12}}] = 0](/pictures/frwiki/48/05c53138d6cbff790d588f10fbd4611b.png) .
.Le commutateur étant nul, il est possible de trouver une base dans laquelle ces deux opérateurs sont diagonaux : les solutions de
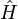 sont donc les vecteurs propres de
sont donc les vecteurs propres de 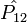 .
.Comme
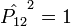 , les valeurs propres de cet opérateur sont +1 ou -1. Il y a donc deux familles de solution possibles du hamiltonien total :
, les valeurs propres de cet opérateur sont +1 ou -1. Il y a donc deux familles de solution possibles du hamiltonien total :Les solutions symétriques : ψ(x1,x2) = ψ(x2,x1) ; x1 et x2 étant les coordonnées (position ainsi que spin) des particules 1 et 2[3]. C'est le cas pour les bosons ou particules de spin entier.
Les solutions antisymétriques : ψ(x1,x2) = − ψ(x2,x1). C'est le cas pour les fermions ou particules de spin demi-entier, et donc pour le principe d'exclusion de Pauli.
Si on décompose la fonction d'onde totale des deux particules ψ(x1,x2) en intrication des états propres φa(xi) et φb(xi) de chaque particule, les solutions antisymétriques sont alors de la forme :
- ψ(x1,x2) = φa(x1)φb(x2) − φb(x1)φa(x2).
Si les particules 1 et 2 sont dans le même état quantique, alors φa = φb. La probabilité de trouver deux fermions identiques dans le même état quantique avec le même spin est nulle.
Ceci est le principe d'exclusion de Pauli : deux fermions identiques ne peuvent être dans le même état quantique avec le même spin.
Une autre conséquence de cette antisymétrie fait que la probabilité de trouver deux électrons de même spin à une même position instantanée est nulle, même sans supposer qu'ils occupent un même état quantique. Pour voir ceci on remarque que ψ(x1,x2) tend vers 0 quand x1 tend vers x2.
Utilisation en astrophysique
En astrophysique, l'effondrement d'étoiles à neutrons, qui demande aux neutrons un même mouvement, donc une même énergie, est limité par le principe d'exclusion qui explique en partie la cohésion de ces étoiles mortes extrêmement massives, qui autrement devraient s'effondrer sous l'effet de la gravitation.
Cependant, lorsque l'étoile est trop massive, le principe d'exclusion ne tient plus et alors l'étoile devient un trou noir.
Énoncé relativiste
La version relativiste de la physique quantique prévoit l'existence de niveaux d'énergie négatifs : le principe d'exclusion permet d'expliquer pourquoi toutes les particules ne disparaissent pas dans ces niveaux-là — en effet, toute particule tend à aller vers l'état d'énergie le plus bas possible, donc devrait s'y précipiter. Si l'on considère comme le fit Dirac que tous les états d'énergie sont occupés, ils ne peuvent pas être habités par d'autres fermions identiques.
Particules échappant au principe d'exclusion
Seuls les fermions sont soumis à ce principe. Les particules indiscernables, de spin entier, satisfont à la statistique de Bose-Einstein et ne satisfont pas le principe d'exclusion de Pauli. Au contraire, on observera même un comportement « grégaire. »
Enfin, il existe des situations (particulièrement à deux dimensions), où l'on peut introduire des anyons, qui ne sont ni des fermions, ni des bosons.
D'autre part la supersymétrie quantique associe à tout boson son supersymétrique fermion : ainsi au graviton, boson de spin 2, devrait être associé un gravitino de spin 3/2. En 2006, il n'existe aucune trace expérimentale de cette supersymétrie.
Références
- ↑ Conférence Nobel de W. Pauli
- ↑ Cette dérivation est fondée sur les documents suivants : Cours de Jean Dalibard, Support de cours du Laboratoire Leprince-Ringuet et une Lecture de l'ETH Zurich
- ↑ Les particules étant, par hypothèse, non distinguables, la seule manière de les différencier est d'utiliser leur position comme "label". L'échange de x1 et x2 est physiquement non significatif.
Voir aussi
- Portail de la physique
Catégories : Mécanique quantique | Principe physique
Wikimedia Foundation. 2010.