- 14362-44-8
-
Iode
L'iode est un élément chimique de la famille des halogènes, de symbole I et de numéro atomique 53.
 Échantillon de diiode solide.
Échantillon de diiode solide.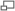
Sommaire
Histoire
L'iode a été découvert en 1811 par le chimiste et fabricant de salpètre Bernard Courtois dans des cendres d'algues marines.
Il a été nommé ainsi par Gay Lussac du grec iodes (violet), en raison de sa couleur.Propriétés
L'iode est aux conditions normales de température et de pression un solide violet-noir brillant composé de molécules homonucléaires I2. Il se sublime rapidement en un gaz violet très irritant, le diiode I2.Il peut également se trouver sous forme de I3-(triiodure).
Isotopes
L'iode naturel est composé de l'isotope stable 127I.
Les autres isotopes de l'iode sont tous radioactifs. L'iode 129 était présent sur Terre à sa formation (dû à sa demi-vie relativement longue, de 15,7 millions d'années) mais est aujourd'hui éteint.Ses isotopes radioactifs sont produits en grande masse dans les produits de fission de l'uranium et du plutonium de l'industrie nucléaire.
Bien qu'il ait une faible durée de demi-vie, l'iode 131 émis lors des accidents nucléaires (dont celui de Tchernobyl) pose problème en raison du fait que la thyroïde fixe une grande partie de l'iode absorbé via l'alimentation, l'eau ou l'inhalation. L'iode est alors facteur de cancer ou troubles graves de la thyroïde.Utilisations
Lampe halogène
Lampe à incandescence qui contient un gaz inerte et de l'iode ou de l'iodure de méthyle. Due à sa température très élevée, une partie du filament en tungstène s'évapore et un dépôt métallique se forme sur la paroi de l'ampoule. Celui-ci réagit alors avec l'iode, pour former des iodures métalliques volatils. Ces composés sont détruits au contact du filament, permettant ainsi le retour du métal à sa source. Ce qui permet d'augmenter la durée de vie et d'augmenter la température de fonctionnement.
Un filament à température plus élevée donne une lumière plus blanche (avantage) mais émet une proportion importante d'ultraviolet (inconvénient). L'ampoule étant en quartz, transparent aux UV, l'écran en verre ordinaire (qui filtre les UV) est indispensable autour de l'ampoule « halogène ».
On utilise également du bromure de méthyle CH3Br ou le dibromure de méthyle CH2Br2.
Lampes à halogénures métalliques
Lampes contenant des halogénures (en particulier des iodures) de terres rares (yttrium, dysprosium, scandium, thallium), ainsi que certains métaux (indium, lithium) et du mercure sous pression. L'arc électrique produit excite la combinaison d'atomes métalliques permettant de recréer la « lumière du jour ».
Autres utilisations
- Examen aux rayons X : L'iode possède une forte opacité aux rayons X. Il est utilisé en tant qu'agent de contraste (sous une forme injectable).
- Scintigraphie et Imagerie médicale : des isotopes radioactifs (131I ou 123I) de l'iode sont utilisés comme traceur dans le corps humain pour des examens médicaux (scintigraphie de la thyroïde).
- Traitement anticancéreux ; Contre le cancer de la thyroïde par radiothérapie : L'iode131 radioactif se fixe préférentiellement sur la thyroïde malade et les cellules métastasiques en les détruisant, mais il expose les autres cellules à un rayonnement interne et il a récemment été remis en cause pour le traitement des cancers de petites taille, car il augmente le risque de développer un second cancer suite au traitement[2].
- Pluie : l'iode peut aider, sous forme d'iodure d'argent AgI à déclencher une pluie artificielle, plus exactement à l’ensemencement des nuages.
- Microscopie et indicateur coloré : Les amidonniers ont appris depuis longtemps à utiliser la réaction spécifique de l'iode avec l'amidon pour colorer les grains de celui-ci. La coloration obtenue varie selon le ratio d'amylose et d'amylopectine contenu dans le grain.
Chez l'être humain
Comme oligo-élément
L'essentiel de l'iode est d'origine maritime. Du fait des précipitations, il se retrouve de manière inégale dans les terres, et donc, dans les différentes plantes consommées[3]. La source de l'iode alimentaire dans les pays européens et aux États-Unis se trouve principalement dans les laitages et le pain[3].
L'iode est absorbé sous forme d'ions au niveau de l'estomac et du duodénum. Il est stocké principalement dans la thyroïde et excrété dans les urines.
L'iode est un oligo-élément essentiel à la vie humaine. Les besoins journaliers chez l'adulte sont d'environ 150 µg, davantage chez la femme enceinte. Il sert à fabriquer diverses hormones, dont la thyroxine. Il est souvent ajouté au sel de cuisine pour éviter toute carence (voir aussi le tableau des aliments riches en iode). L'absorption quotidienne se situe entre 0,05 et 0,1 mg[4]. Pour toute une vie les besoins en iode sont d'environ 2 à 4 grammes[5], à peine l'équivalent d'une cuillère à café. C'est assez faible mais cela reste redoutable car notre organisme ne sait pas stocker cet oligo-élément de manière prolongée[6].
Son absence provoque une turgescence de la glande, qui se manifeste par un goitre. La carence en iode entraine un retard de croissance et divers troubles mentaux.
Les populations montagnardes n'ont jamais pu se procurer aisément du sel de mer en raison de son prix. Les cas de difformité et de nanisme étaient donc fréquents parmi les populations paysannes alpines. Dans les Alpes, la population isolée des vallées était beaucoup plus souvent atteinte de désordres liés à la carence en iode. Du reste, Diderot est le premier à consigner le nom de "crétin" dans son encyclopédie raisonnée des sciences, des arts et des métiers (1754). L'expression "crétin des Alpes" est usuelle. Le crétinisme est une forme de débilité mentale et de dégénérescence physique en rapport avec une insuffisance thyroïdienne.
Le risque est également chez le fœtus, notamment sur le développement cérébral.
En 2007, près de deux milliards de personnes, dont un tiers d'âge scolaire, ont un déficit en iode[7], ce qui en fait un des problèmes majeurs de santé publique. L'une des façons de lutter contre cela est l'ajout d'iode dans le sel de consommation.
En tant qu'antiseptique
Le diiode dissout dans l'alcool (« teinture d'iode » ) ou dans une solution aqueuse d'iodure de potassium (solution de lugol) est également utilisé en pharmacie comme antiseptique puissant. Elle laisse des traces jaunes sombres caractéristiques sur la peau. Il existe également des composés organiques où l'iode est lié, tels le polyvidone iodée (Bétadine ou Iso-Bétadine)
Prévention de contamination radioactive
L'iode radioactif 131I peut être rejeté accidentellement par un réacteur nucléaire. Il est assimilé avec la nourriture ou l'eau contaminée, se fixe sur la thyroïde. L'ingestion de comprimés d'iodure de potassium (130 mg par jour) sature la glande thyroïde et évite cette fixation. Cette consigne de sécurité est surtout importante pour les enfants et les femmes enceintes ou allaitant, les risques de cancers thyroïdiens étant majeurs. Pour les adultes et les personnes âgées, la prise d'iode stable est discutable. La balance bénéfices/risques n'étant plus aussi importante.
Toxicité
Au travail, l'iode est un agent chimique dangereux car il est nocif par inhalation et par contact avec la peau[8].
L'allergie à l'iode
Certaines personnes peuvent être allergiques à des produits contenant de l'iode, comme par exemple au produit contrastant injecté pour des examens de radiologie ou encore certains fruits de mer ; s'est donc répandue l'idée, fausse, que l'on pouvait être allergique à l'iode. Ceci est parfaitement faux. Les produits susceptibles d'induire une "allergie à l'iode" contiennent tous de l'iode, mais ce sont des substances différentes qui interviennent dans le cas de l'allergie. Pour la bétadine, c'est la povidone (le véhicule de l'iode) qui est responsable, pour les produits de contraste iodés, l'osmolalité est mise en cause, et pour les produits de la mer (poissons et crustacés) ce sont des protéines musculaires. Il n'existe donc aucune réaction croisée ni de facteurs de risques. De plus, il n'y a aucune allergie rapportée dans le cas d'utilisation de solution alcoolique ou aqueuse d'iode (solution de Lugol, teinture d'iode, ...).
Notes et références
- ↑ a et b (fr) Paul Arnaud, Brigitte Jamart, Jacques Bodiguel, Nicolas Brosse, Chimie Organique 1er cycle/Licence, PCEM, Pharmacie , Cours, QCM et applications, Dunod, 8 juillet 2004, Broché, 710 p. (ISBN 2100070355)
- ↑ voir l'article : Cancer de la thyroïde.
- ↑ a et b Zimmermann MB, Jooste PL, Pandav CS, Iodine-deficiency disorders, Lancet, 2008;372:1251-1262
- ↑ J.O Peyrin, J.C Vandroux, Atlas des glandes endocrines, Université Jean Monnet, Saint Étienne, (page consultée le 13 juin 2008).
- ↑ Le Républicain Niger : Lutte contre les troubles dus à la carence en iode
- ↑ Conseil international des infirmières : Les infirmières, les pharmaciens et les médecins du monde demandent à l’Inde de n’utiliser que du sel iodé
- ↑ Iodine deficiency—way to go yet, Lancet, 2008; 372:88
- ↑ L'iode au travail
Voir aussi
Articles connexes
s1 s2 g f1 f2 f3 f4 f5 f6 f7 f8 f9 f10 f11 f12 f13 f14 d1 d2 d3 d4 d5 d6 d7 d8 d9 d10 p1 p2 p3 p4 p5 p6 1 H He 2 Li Be B C N O F Ne 3 Na Mg Al Si P S Cl Ar 4 K Ca Sc Ti V Cr Mn Fe Co Ni Cu Zn Ga Ge As Se Br Kr 5 Rb Sr Y Zr Nb Mo Tc Ru Rh Pd Ag Cd In Sn Sb Te I Xe 6 Cs Ba La Ce Pr Nd Pm Sm Eu Gd Tb Dy Ho Er Tm Yb Lu Hf Ta W Re Os Ir Pt Au Hg Tl Pb Bi Po At Rn 7 Fr Ra Ac Th Pa U Np Pu Am Cm Bk Cf Es Fm Md No Lr Rf Db Sg Bh Hs Mt Ds Rg Cp Uut Uuq Uup Uuh Uus Uuo 8 Uue Ubn * Ute Uqn Uqu Uqb Uqt Uqq Uqp Uqh Uqs Uqo Uqe Upn Upu Upb Upt Upq Upp Uph Ups Upo Upe Uhn Uhu Uhb Uht Uhq Uhp Uhh Uhs Uho ↓ g1 g2 g3 g4 g5 g6 g7 g8 g9 g10 g11 g12 g13 g14 g15 g16 g17 g18 * Ubu Ubb Ubt Ubq Ubp Ubh Ubs Ubo Ube Utn Utu Utb Utt Utq Utp Uth Uts Uto Métalloïdes Non-métaux Halogènes Gaz rares Métaux alcalins Métaux alcalino-terreux Métaux de transition Métaux pauvres Lanthanides Actinides Superactinides Éléments non classés - Portail de la chimie
- Portail de la pharmacie
Catégories : Élément chimique | Halogène | Antiseptique | Minéral alimentaire
Wikimedia Foundation. 2010.

