- 1,3-Diazine
-
Pyrimidine
Pyrimidine 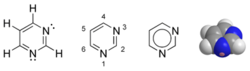
Structure de la pyrimidine Général Nom IUPAC Pyrimidine Synonymes 1,3-diazine No CAS No EINECS PubChem SMILES InChI Propriétés chimiques Formule brute C4H4N2 [Isomères] Masse molaire 80,088 g∙mol-1
C 59,99 %, H 5,03 %, N 34,98 %,
80.08796pKa 1,2 Précautions Transport 33 1993 SIMDUT[1] Produit non contrôlé Unités du SI & CNTP, sauf indication contraire. La pyrimidine (ou 1,3-diazine) est une molécule azotée hétérocyclique aromatique (C4H4N2) voisine de la pyridine et comportant deux atomes d'azote. Elle est aussi isomère de position de la pyridazine (1,2-diazine) et la pyrazine (1,4-diazine). Dans un sens plus large, ses dérivés à bases pyrimidiques sont aussi appelés pyrimidines. Ils se retrouvent notamment dans les bases azotées constituant les molécules d'ADN et d'ARN : cytosine, thymine, uracile.
Dans l'ADN ces bases forment des liaisons hydrogènes avec leurs purines complémentaires :
purine pyrimidine A T G C Dans l'ARN, le complément de A (adénine) est l'uracile au lieu de la thymine :
purine pyrimidine A U G C Sommaire
Synthèse des pyrimidines
La plupart des organismes vivants sont capables de synthétiser naturellement des pyrimidines. On ne connait actuellement qu'une voie de biosynthèse commune ; cette voie part de l'aspartate qui est transformée par trois réactions consécutives en orotate (elle-même une pyrimidine), qui devient ensuite de l'UMP après deux réactions supplémentaires. Les autres nucléotides pyrimidiques peuvent ensuite être créés à partir de l'UMP.
Chez l'homme, la synthèse des pyrimidines se produit dans le cytoplasme des cellules, et plus particulièrement dans celles du foie, voire dans les cellules du cerveau mais dans une moindre mesure. Cette voie de biosynthèse est la cible de nombreux inhibiteurs pharmacologiques.
Les pyrimidines peuvent être obtenues synthétiquement par réaction entre un dérivé β-dicarbonylé (ex. : β-dicétone) et une amidine (ou un composé similaire tel l'urée, la thiourée ou la guanidine) à l'aide de catalyse acide ou basique si les combinaisons de nucléophile-électrophile ne sont pas assez réactives. Certaines de ces combinaisons peuvent conduire à la formation de pyrimidones, analogues des pyridones.Une voie de synthèse intéressante des méthylpyrimidines est l'addition de l'amidure de sodium sur la 2-bromopyridine. Alors que les conditions sont similaires à la réaction de Chichibabin, on a addition en position 4, ouverture de cycle avec élimination du bromure, réarrangement et fermeture de cycle pour donner la 4-méthylpyrimidine, avec un rendement de 80%. Appliquée à la 2-bromopyrimidine, cette réaction mène à une 1,3,5-triazine. Cependant, la 2,6-dibromopyridine, traitée dans les mêmes conditions, ne donne pas de triazine comme l'on pourrait l'imaginer mais à un diazole, par contraction de cycle.
Dimère
Dans l'ADN, lorsque deux bases pyrimidiques (la cytosine ou la thymine) sont empilées consécutivement sur le même brin, elles peuvent réagir sous l'action des rayons uv pour former un dimère covalent. Ce dimère de pyrimidine se forme par cycloaddition sur les doubles liaisons entre les carbones 5 et 6. Il se forme un cycle cyclobutane entre les deux bases consécutives.
Cette modification photochimique induit une déformation et une rigidification de la double-hélice d'ADN, qui interfère avec la réplication. Ce mécanisme peut induire des mutations dans les cellules exposées et constitue la base du pouvoir cancérogène du rayonnement UV. Toutes les cellules vivantes disposent d'un mécanisme de réparation spécifique de cette lésion, basé sur des enzymes appelées photolyases.
Réactivité chimique
Les dérivés pyrimidines ne sont pas très réactifs vis-à-vis de la substitution électrophile dû à leur forte acidité. Une alternative est l'utilisation des N-oxydes ou des pyrimidones induisant un caractère nucléophile au cycle par délocalisation d'électrons π entre N-O ou C-O.
A contrario, les pyrimidines sont propices aux substitutions nucléophiles par délocalisation de la charge sur les atomes d'azotes avec une préférence pour le carbone en position 2.
Voir aussi
- Pyridine
- Diazines : molécules aromatiques avec deux atomes d’azote dans l’anneau
- Pyrimidine
- Pyridazine
- Pyrazine
- Triazines : molécules aromatiques avec trois atomes d’azote dans l’anneau
- 1,2,3-Triazine
- 1,2,4-Triazine
- 1,3,5-Triazine
Références
- ↑ « Pyrimidine » dans la base de données de produits chimiques Reptox de la CSST (organisme canadien responsable de la sécurité et de la santé au travail), consulté le 24 avril 2009
- Portail de la biologie
- Portail de la chimie
Catégories : Noyau aromatique simple | Pyrimidine
Wikimedia Foundation. 2010.

