- Acide α-cétoacétique
-
Acide pyruvique
Acide pyruvique 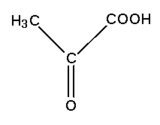
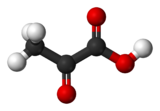
acide pyruvique Général Nom IUPAC acide 2-oxapropanoïque No CAS No EINECS FEMA Apparence liquide incolore Propriétés chimiques Formule brute C3H4O3 [Isomères] Masse molaire 88,0621 g∙mol-1
C 40,92 %, H 4,58 %, O 54,5 %,pKa 2,4 Propriétés physiques T° fusion 12 °C[1] T° ébullition 165 °C (décompostion) [1] Solubilité miscible avec l'eau[1] Masse volumique 1,27 g/cm³ à 20 °C[1] Point d’éclair 82 °C [1] Précautions Directive 67/548/EEC 
CPhrases R : 34, Phrases S : 26, 36/37/39, 45, Transport 88 3265 SIMDUT[2] 
Écotoxicologie DL50 souris, subdermal :
3533mg/kgUnités du SI & CNTP, sauf indication contraire. L'acide pyruvique est un acide carboxylique de formule CH3-CO-COOH. C'est le plus simple des cétoacides. Sa base conjuguée est l'ion pyruvate.
Sommaire
Acide pyruvique
L'acide pyruvique se présente sous la forme d'un liquide incolore, d'odeur similaire à celle de l'acide acétique. Il est miscible dans l'eau, et soluble dans l'éthanol et l'éther.
En laboratoire, l'acide pyruvique peut être préparé en chauffant un mélange d'acide tartrique et de bisulfate de potassium, par oxydation du propylène glycol par un oxydant fort (par exemple du permanganate de potassium ou de l'hypochlorite de sodium), ou encore par hydrolyse du 2-oxopropiononitrile, formé par réaction du chlorure d'éthanoyle sur le cyanure de potassium:
- CH3COCl + KCN → CH3COCN
- CH3COCN → CH3COCOOH
Ion pyruvate
Description
Le pyruvate est le produit final des voies de dégradation du glucose (la glycolyse, voie des pentoses phosphates, voie d'Entner-Doudoroff). Il est le substrat de la fermentation en condition anaérobie, et du cycle de Krebs en condition aérobie.
Devenir du pyruvate en anaérobiose
Ces réactions ont lieu dans le cytoplasme. Dans le muscle (pour la fermentation lactique) ou chez la levure (pour la fermentation alcoolique). D'autres fermentations sont possibles, chez les entérobactéries. Voir voies fermentaires des entérobactéries.
Fermentation lactique
CH3-CO-COO- + NADH + H+ ↔ CH3-CHOH-COO- + NAD+
enzyme : lactate déshydrogénase
Le lactate produit peut être considéré comme un déchet, cependant, les courbatures ne sont pas dues à une accumulation d'acide lactique et de déchets du métabolisme dans les tissus musculaires (lire BIOLOGIE DU SPORT, Weineck, p. 256 chez Vigot). Toutefois, il peut être transporté dans le sang puis dans les cellules hépatiques (cycle de Cory).
Fermentation alcoolique
- CH3-CO-COO- + H+ → CH3CHO + CO2 (enzyme : pyruvate décarboxylase, en présence de thyamine pyrophosphate)
- CH3CHO + NADH + H+ ↔ CH3CH2OH + NAD+ (enzyme : alcool déshydrogénase)
Devenir du pyruvate en aérobiose
Elle a lieu dans la mitochondrie. Le pyruvate y pénètre par la pyruvate translocase. Deux réactions sont possibles qui génèrent les précurseurs du cycle de Krebs :
Décarboxylation oxydative
Cette réaction est catalysée par un complexe multienzymatique (pyruvate déshydrogénase) faisant intervenir cinq coenzymes. Trois coenzymes sont liés aux apoenzymes : le thyamine pyrophosphate (ou TPP), le lipoate et le FAD (ce sont des groupements prosthétiques). Les deux autres sont libres et non liés au complexe : le NAD et le coenzyme A.
BILAN : Pyruvate + HSCoA + NAD+ → AcétylCoA + CO2 + NADH + H+
Le NADH sera par la suite réoxydé par la chaîne respiratoire pour produire de l'ATP.
Carboxylation
La réaction est catalysée en présence de biotine par la pyruvate carboxylase (synthétase), produit de l'oxaloacétate.
BILAN : Pyruvate + ATP + H2 + CO2} → Oxaloacétate + ADP + Pi
Comparaison du rendement énergétique des réactions
À partir d'une molécule de glucose (qui donne 2 molécules de pyruvate) :
- Les fermentations sont moins rentables (elles libèrent 2 molécules d'ATP) ;
- Les utilisations en aérobiose libèrent plus d'énergie (14 ATP pour la décarboxylation oxydative, 6 pour la carboxylation) ; et encore, ce n'est pas terminé (voir cycle de Krebs).
Voir aussi
Références
- ↑ a , b , c , d et e Entrée du numéro CAS « 127-17-3 » dans la base de données de produits chimiques GESTIS de la BGIA (organisme allemand responsable de la sécurité et de la santé au travail) (allemand, anglais), accès le 03/08/09 (JavaScript nécessaire)
- ↑ « Acide pyruvique » dans la base de données de produits chimiques Reptox de la CSST (organisme canadien responsable de la sécurité et de la santé au travail), consulté le 24 avril 2009
- Portail de la chimie
- Portail de la biologie
- Portail de la biochimie
Catégories : Produit chimique corrosif | Glycolyse | Cétoacide | Glucide
Wikimedia Foundation. 2010.

