- Acide phosphorique
-
Acide phosphorique 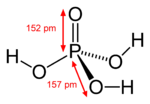
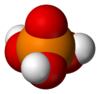
Structure de l'acide phosphorique.Général Nom IUPAC Acide orthophosphorique Synonymes acide phosphorique
phosphate d'hydrogèneNo CAS No EINECS PubChem No E E338 FEMA SMILES InChI Apparence Solide blanc ou liquide visqueux incolore (T>42 °C) Propriétés chimiques Formule brute H3PO4 Masse molaire[1] 97,9952 ± 0,0014 g·mol-1
H 3,09 %, O 65,31 %, P 31,61 %,pKa 2,12 ; 7,21 ; 12,67 Propriétés physiques T° fusion 42,35 °C[2] T° ébullition Se décompose au-dessous du point d'ébullition à 213 °C[3] Solubilité Sol dans l'alcool;
sol dans 8 vol d'un mélange d'éther:alcool à 3:1;
548 g sol dans 100 cm3 d'eau froide[2]
très sol dans l'eau chaude;Masse volumique 1,834 g·cm-3 à 18 °C [2] Pression de vapeur saturante à 20 °C : 4 Pa[3] Viscosité dynamique 3,86 mPa·s (solution à 40%, 20 °C)[2] Précautions Directive 67/548/EEC[4] 
CPhrases R : 34, Phrases S : (1/2), 26, 45, NFPA 704 SIMDUT[5] 
SGH[6] 
DangerInhalation Sensation de brûlure. Toux. Essoufflement. Mal de gorge. Peau Rougeur. Douleur. Brûlures cutanées. Ampoules. Yeux Douleur. Rougeur. Brûlures profondes graves. Ingestion Douleurs abdominales. Sensation de brûlure. Choc ou collapsus. Composés apparentés Autres composés Acide hypophosphoreux, Acide phosphoreux, Acide pyrophosphorique Unités du SI & CNTP, sauf indication contraire. L’acide phosphorique est un composé chimique de formule H3PO4. C'est un oxoacide trifonctionnel (triacide) important en chimie minérale et fondamental en biochimie. Il s'agit d'un acide minéral obtenu par traitement de roches phosphatées ou par combustion du phosphore.
À température ambiante, l'acide phosphorique est un solide cristallin de densité 1,83, qui fond à 42,35 °C. Il constitue la matière première de base pour la production de phosphates (ou sels phosphatés).
Sommaire
Chimie
Il s'agit d'un triacide minéral capable de céder trois protons en formant successivement trois bases conjuguées : dihydrogénophosphate H2PO4-, hydrogénophosphate HPO42-, et orthophosphate PO43-, avec les constantes d'équilibres suivantes :
-
H3PO4 (s) + H2O(l)  H2PO4−(aq) + H3O+(aq),
H2PO4−(aq) + H3O+(aq),Ka1= 7,25×10−3, pKa1= 2,12. H2PO4−(aq) + H2O(l)  HPO42−(aq) + H3O+(aq),
HPO42−(aq) + H3O+(aq),Ka2= 6,31×10−8, pKa2= 7,21. HPO42−(aq) + H2O(l)  PO43−(aq) + H3O+(aq),
PO43−(aq) + H3O+(aq),Ka3= 3,98×10−13, pKa3= 12,67.
Biologie
Les dimères et trimères de l'acide phosphorique interviennent dans de nombreux domaines en biologie comme les transporteurs d'énergie ADP/ATP, l'ADN et dans les os.
Production industrielle
L'acide phosphorique est généralement obtenu par l'attaque dans un réacteur du minerai de fluorophosphate de calcium par de l'acide sulfurique H2SO4, après un certain temps de séjour dans le réacteur (variable selon le type de réacteur utilisé et le minerai traité) il est procédé à une opération de filtration de la bouillie résultante (le liquide et le solide) afin de séparer l'acide phosphorique ainsi fabriqué des cristaux de sulfate de calcium dihydraté (CaSO4,2H2O) ou semi-hydraté (CaSO4,1/2 H2O ) appelé phosphogypse.
Ca5(PO4)3F + 5 H2SO4 + 10 H2O → 3 H3PO4 + 5 (CaSO4,2H2O) + HF.
On peut également le préparer par calcination de la vapeur de phosphore, puis par traitement de l'oxyde résultant avec de la vapeur d'eau.
Utilisations
L'acide phosphorique est très utilisé en laboratoire, car il résiste à l'oxydation, à la réduction et à l'évaporation.
L'acide phosphorique est employé dans les boissons non alcoolisées comme régulateur de pH (E338) : principalement dans les sodas au cola (Coca-Cola, Pepsi Cola)[7].
L'acide phosphorique est employé comme composant des ciments dentaires, comme catalyseur ou dans les métaux inoxydables, et dans la production des phosphates — utilisés dans les adoucisseurs d'eau, les engrais et les détergents.
L'acide phosphorique est souvent utilisé en solution dans des produits utilisés en mécanique pour dérouiller les pièces métalliques. Il sert aussi à "phosphater" les pièces pour les protéger de l'oxydation à l'air libre.
Risques
L'ingestion d'un taux élevé d'acide phosphorique pourrait entraver le fonctionnement des reins et favoriser les calculs rénaux. Des chercheurs américains ont interrogé 465 personnes pour lesquelles une insuffisance rénale avait été récemment diagnostiquée et ont constaté à partir de la description de leur régime alimentaire qu'à partir de deux verres de coca journalier, le risque d'insuffisance rénale est multiplié par deux. Il en est de même avec le Coca "Light". En revanche, aucune association n'a été trouvée avec les autres sodas[8].
Notes et références
- Masse molaire calculée d’après Atomic weights of the elements 2007 sur www.chem.qmul.ac.uk.
- PHOSPHORIC ACID sur Hazardous Substances Data Bank. Consulté le 27 novembre 2009
- ACIDE PHOSPHORIQUE, fiche de sécurité du Programme International sur la Sécurité des Substances Chimiques, consultée le 9 mai 2009
- « acide orthophosphorique » sur ESIS, consulté le 3 mars 2010
- « Acide phosphorique » dans la base de données de produits chimiques Reptox de la CSST (organisme québécois responsable de la sécurité et de la santé au travail), consulté le 23 avril 2009
- Numéro index dans le tableau 3.1 de l'annexe VI du règlement CE N° 1272/2008 (16 décembre 2008)
- Isabelle Eustache, « Pas de coca, c'est mieux pour les reins ! » sur www.e-sante.fr, 23/07/2007. Consulté le 15 mai 2008.
- Saldana TM, Basso O, Darden R, Sandler DP., « Carbonated beverages and chronic kidney disease. » sur http://www.ncbi.nlm.nih.gov, 18/07/2007. Consulté le 16 avril 2009.
Annexes
Articles connexes
Liens et documents externes
Catégories :- Composé du phosphore
- Produit chimique corrosif
- Phosphate
- Oxoacide
- Saveur acide
- Régulateur alimentaire de pH
- ADN
- Séquestrant
-
Wikimedia Foundation. 2010.

