- 75-87-6
-
Chloral
Chloral 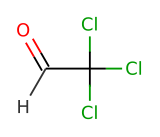
Général Nom IUPAC Trichloroéthanal No CAS No EINECS Propriétés chimiques Formule brute C2HCl3O [Isomères]
CCl3CHOMasse molaire 147,388 g∙mol-1
C 16,3 %, H 0,68 %, Cl 72,16 %, O 10,86 %,Propriétés physiques T° fusion -57,5 °C T° ébullition 97,8 °C Masse volumique 1512 kg·m-3 Pression de vapeur saturante 5200 Pa (20 °C) Précautions SIMDUT[2] Produit non classifié Classification du CIRC Groupe 3 : Inclassable quant à sa cancérogénicité pour l'Homme[1] Unités du SI & CNTP, sauf indication contraire. Le chloral est un composé chimique organique découvert en 1832 par Justus von Liebig (1803-1873).
Sommaire
Propriétés chimiques
- Noms : Chloral, trichloracétaldéhyde ou trichloroéthanal.
- Formule semi-développée : voir figure 1.
- Masse molaire = 147,39 g/mol
Ne pas confondre chloral et chloroforme CHCl3.
Préparation
Le chloral est obtenu par la réaction du dichlore sur l'éthanol selon la réaction chimique suivante :

Le nom chloral tire son origine des premières syllabes des mots chlore et alcool, qui sont les substances utilisées pour sa préparation.
Propriétés physiques
C'est un liquide d'apparence huileuse et lourde.
- Masse volumique = 1,91 g/cm3 (1,541 g/cm3 à 0 °C)
- Température de fusion = -57 °C
- Température d'ébullition = 97 °C
Le chloral est soluble dans l'éthanol et l'éthoxyéthane (éther éthylique).
Dérivé
L'hydrate de chloral est utilisé en thérapeutique depuis de nombreuses années comme sédatif, hypnotique ou analgésique. En pharmacie, la posologie est de 50 à 75 mg/kg de masse corporelle en une seule dose. Pour le fabriquer, il suffit de d'ajouter de l'eau au chloral et il réagira pour donner de l'hydrate de chloral. Réaction:
- Cl3C-CH=O + H20 réagira pour donner du Cl3C2H(OH)2
Risques pour la santé
- Son odeur est piquante et a un effet irritant pour les yeux, pouvant provoquer une conjonctivite.
- Neurotoxique pour les centres bulbo-protubéranciels dans le cerveau.
- Seulement 10 g de chloral peuvent tuer un être humain.
- Le chloral attaque le cerveau en provoquant l'hébétude, la confusion, puis des convulsions musculaires ressemblant aux chorées.
- Le chloral provoque des léthargies ou des insomnies.
- Le chloral provoque aussi des maux de tête terribles.
- Il est nocif pour les organes uro-génitaux et la peau.
- Le chloral a des effets mutagènes et cancérigènes chez l'animal.
- Gastrite irritative pouvant entraîner des vomissements
Dérivé chimique : hydrate de chloral
- L'hydrate de chloral est connu sous la dénomination 2,2,2-trichloroéthan-1,1-diol, trichloracétaldéhyde monohydrate. Il s'agit d'un mélange des deux molécules (figure 2).
Propriétés pharmacologiques de l'hydrate de chloral
- Antimitotique - Anticancéreux
- Psycholeptique
- Sédatif
- Hypnogène
- Analgésique
- Anticonvulsif
Références
- ↑ IARC Working Group on the Evaluation of Carcinogenic Risks to Humans, « Evaluations Globales de la Cancérogénicité pour l'Homme, Groupe 3 : Inclassables quant à leur cancérogénicité pour l'Homme » sur http://monographs.iarc.fr, 16 janvier 2009, CIRC. Consulté le 22 août 2009
- ↑ « Chloral » dans la base de données de produits chimiques Reptox de la CSST (organisme canadien responsable de la sécurité et de la santé au travail), consulté le 25 avril 2009
- Portail de la chimie
- Portail de la médecine
- Portail de la pharmacie
Catégories : Pharmacie | Élément toxique | Composé organo-chloré | Aldéhyde
Wikimedia Foundation. 2010.