- 7158-70-5
-
Leucrose
Leucrose 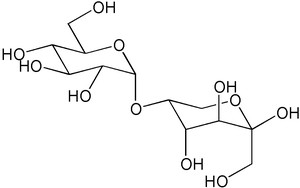
Sturcture chimique du Leucrose. Général Nom IUPAC 5-O-alpha-D-glucopyranosyl-D-Fructose Synonymes D-Glucopyranosyl-alpha(1-5)-D-fructopyranose
Glc α(1→5) FrucNo CAS PubChem SMILES InChI Apparence Solide blanc Propriétés chimiques Formule brute C12H22O11 [Isomères] Masse molaire 342,2965 g∙mol-1
C 42,11 %, H 6,48 %, O 51,42 %,Propriétés physiques T° fusion 161 à 163 °C[1]
156 à 158 °C (monohydrate)[2]Solubilité Soluble dans l'eau. Composés apparentés Isomère(s) Saccharose, Turanose, Isomaltulose, Trehalulose, Maltulose Unités du SI & CNTP, sauf indication contraire. Le leucrose est un diholoside réducteur naturellement présent dans la nature. Il l'isomère du saccharose tout en étant non-cariogène et moitié moins sucré que celui-ci.
Sommaire
Histoire
Le leucrose a été découvert en 1952 par FH Stodola lors d'une synthèse enzymatique par la Leuconostoc mesenteroides en présence de saccharose. Sous certaine conditions 3% du saccharose a été transformé en un diholoside non réducteur composé de glucose et de fructose. FH Stodola a donné le nom de leucrose a ce nouveau sucre afin de rappeler son origine microbienne[1]. Sa structure a été définie en 1956[2].
Depuis le leucrose a été trouvé dans le miel[3] et le pollen de Typha latifolia[4].
En 1986, la société Pfeiffer & Langen a déposé un brevet décrivant la production de leucrose à partir du saccharose ou du fructose par l'utilisation d'une enzyme, la dextransucrase[5],[6].
Depuis peu, Cargill commercialise le leucrose comme ingrédient au pouvoir édulcorant en mélange (13%) avec du fructose (37%) et autre osides (48%)[6].
Structure et propriétés
Structure
Le leucrose, composé de deux oses (une unité de glucose et d'une unité de fructose) et de formule chimique C12H22O11, est un isomère du saccharose. Cependant la nature de la liaison oside reliant les deux unités est différente : une liaison α(1→5) pour le leucrose et α(1→2) pour le saccharose.
Propriétés physiques
Le leucrose est un composé blanc cristallin[2], qui en solution aqueuse existe sous deux formes tautomères : 1,9 % en α-pyranose et 98,1% en β-pyranose (à 20 °C[4],[7]). Il se cristallise sous forme monohydraté sous la forma tautomère β-pyranose[7].
Propriétés chimiques
Le leucrose est un diholoside réducteur résistant a l'hydrolyse acide[2].
L'hydrogénation du leucrose produit le leucritol.
Autre propriétés
Bien que le leucrose soit l'isomère du saccharose son pouvoir sucrant est deux fois plus faible : de 0,4 à 0,5[3] et de 0,5 à 0,6[5].
Le leucrose est considéré comme étant non-cariogène car il n'est pas utilisé par le principal germe mis en cause dans la formation des caries, le Streptococcus mutans[8]. Cependant il a été montré que d'autre germes présent dans la bouche et qui contribue à l'apparition des caries peuvent fermenter le leucrose[9]. Une autre étude a mesuré le pourcentage de germes susceptibles de fermenter les isomères du saccharose, seuls 23% des germes testés ont été capables de fermenter le leucrose, contre 25% pour le turanose, 33% pour le palatinose et 70% pour le isomaltulose[10].
Utilisation
L'utilisation du leucrose comme édulcorant dans les chewing-gum (de 0,1% à 10%) a été breveté pour remplacer les polyols qui ont tendance à être moins bien digérés[11].
Métabolisme
Le leucrose est normalement métabolisé par l'homme. Cependant son hydrolyse par les enzymes est moins rapide (entre 1/5 et 1/3[5]) que pour le saccharose ou bien le maltose. Le niveau de glucose et de fructose est plus faible que lors de la consommation de saccharose, tandis que les niveau d'insuline et de C-peptide sont inchangés[12]. Seulement une infime quantité est excretée par voie urinaire, de 0,05 à 0,08%[13].
Production
Le leucrose est produit par réaction du saccharose avec une glucosyl transférase en présence de saccharose et de fructose[5].
Le leucrose est un produit secondaire produit par la dextrane-saccharase lors de la production d'isomaltulose à partir du saccharose[14].
Notes et références de l'article
- ↑ a et b (en) FH Stodola, HJ Koepsell & ES Sharpe, « A new disaccharide produced by Leuconostoc mesenteroides », dans J. Am. Chem. Soc., vol. 74, 1952, p. 3202-3203 [texte intégral lien DOI (pages consultées le 22/09/2008.)] :
« we believe it advisable, therefore, to assign it the common name of “leucrose” which is suggested by its particular microbial origin. »
- ↑ a , b , c et d (en) FH Stodola, ES Sharpe & HJ Koepsell, « The Preparation, Properties and Structure of the Disaccharide Leucrose », dans J. Am. Chem. Soc., vol. 78, 1956, p. 2514-2518 [texte intégral lien DOI (pages consultées le 22/09/2008.)]
- ↑ a et b Shmuel Yannai, Dictionary of Food Compounds with CD-ROM: Additives, Flavors, and Ingredients, Publié par CRC Press, 2004, 1784 p. (ISBN 9781584884163), p. 547
- ↑ a et b (en) (en) Peter M. Collins, Dictionary of carbohydrates, CRC Press, 2005, 1282 p. (ISBN 0849338298), p. 538
- ↑ a , b , c et d (en) D Schwengers & H Benecke, « US Patent 4693974 - Processes for producing leucrose », 09/29/1986, US patent. Consulté le 22/09/2008.
- ↑ a et b (en) MA Godshall, « The Expanding World of Nutritive and Non-Nutritive Sweeteners » sur http://www.sugarjournal.com, 01/2007, p. 12-20. Consulté le 7 novembre 2008 [pdf]
- ↑ a et b (en) FW Lichtenthaler et S. Rönninger, « -D-Glucopyranosyl-D-fructoses: distribution of furanoid and pyranoid tautomers in water, dimethyl sulphoxide, and pyridine. Studies on ketoses. Part 4 », dans J. Chem. Soc., Perkin Trans. 2, 1990, p. 1489–1497 [résumé, [pdf] texte intégral lien DOI (pages consultées le 07/11/2008)]
- ↑ (en) SC Ziesenitz, G Siebert & T Imfeld, « Cariological assessment of leucrose [D-glucopyranosyl-alpha(1----5)-D-fructopyranose] as a sugar substitute. », dans Caries Res., vol. 23, 1989, p. 351-357 [résumé (page consultée le 22/09/2008.)]
- ↑ (en) H Peltroche-Llacsahuanga, CJ Hauk, R Kock, F Lampert, R Ltticken & G Haase, « Assessment of Acid Production by Various Human Oral Micro-organisms when Palatinose or Leucrose is Utlize », dans J. Dent. Res., vol. 80, 2001, p. 378-384 [texte intégral (page consultée le 22/09/2008.)]
- ↑ (en) J Matsuyama, T Sato, E Hoshino, T Noda & N Takahashi, « Fermentation of Five Sucrose Isomers by Human Dental Plaque Bacteria », dans Caries Res., vol. 37, 2003, p. 410-415 [résumé lien DOI (pages consultées le 22/09/2008.)]
- ↑ (en) JR Muhammad, RJ Yatka, MA Meyers, LC Richey & DW Record, « (WO/1997/010722) Chewing gum containing Leucrose » sur www.wipo.int, 22.09.1995, World patent. Consulté le 22/09/2008.
- ↑ (en) SC Ziesenitz, G Siebert, D Schwengers & R Lemmes, « Nutritional Assessment in Humans and Rats of Leucrose [D-glucopyranosyl-(1 5)-D-fructopyranose] as a Sugar Substitute », dans Journal of Nutrition, vol. 119, 1989, p. 971-978 [résumé (page consultée le 22/09/2008.)]
- ↑ (en) (en) S Bielecki, J Tramper & J Polak, Food Biotechnology, Elsevier, 2000, 430 p. (ISBN 9780444505194), partie Oligosaccharide synthesis with dextransucrase, kinetics and reaction engineering, p. 123-135
- ↑ (en) FB Paul, PF Monsan, MM Remaud & VP Pelenc, « Process for preparing enzymatically a sugar mixture having a high content of isomaltose from sucrose - European Patent EP0252799 » sur /www.freepatentsonline.com, 04/15/1992, European Patent. Consulté le 22/09/2008.
Voir aussi
Articles connexes
Liens et documents externes
- (en) Substance Leucrose NCBI database
- (en) Leucrose sur National Library of Medicine - Medical Subject Headings MeSH
- Portail de la chimie
- Portail de la biochimie
Catégories : Diholoside | Édulcorant - ↑ a et b (en) FH Stodola, HJ Koepsell & ES Sharpe, « A new disaccharide produced by Leuconostoc mesenteroides », dans J. Am. Chem. Soc., vol. 74, 1952, p. 3202-3203 [texte intégral lien DOI (pages consultées le 22/09/2008.)] :
Wikimedia Foundation. 2010.
