- 3,4',5,7-Tétrahydroxyflavone
-
Kaempférol
Kaempférol 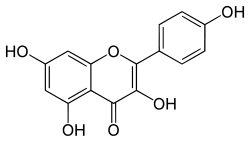
Général Nom IUPAC 3,5,7-trihydroxy-2-
(4-hydroxyphenyl)-4H-1-
benzopyran-4-oneSynonymes Robigenin
Nimbecetin
Populnetin
3,4',5,7-Tetrahydroxyflavone
C.I. 75640No CAS No EINECS DrugBank PubChem SMILES InChI Propriétés chimiques Formule brute C15H10O6 [Isomères] Masse molaire 286,2363 g∙mol-1
C 62,94 %, H 3,52 %, O 33,54 %,Propriétés physiques T° fusion 277 °C[1] Précautions Directive 67/548/EEC 
XnPhrases R : 22, 26, 36, Classification du CIRC Groupe 3 : Inclassable quant à sa cancérogénicité pour l'Homme[2] Composés apparentés Isomère(s) Fisétine, Lutéoline Autres composés Quercétol, Myricétol Unités du SI & CNTP, sauf indication contraire. Le kaempférol est un flavonoïde de type flavonol que l’on trouve dans les fraises, les brocolis et les épinards. C'est un pigment jaune, légèrement soluble dans l'eau et soluble dans l’éthanol chaud et l’éther diéthylénique.
Sommaire
Aliments riches en kaempférol
La quantité de kaempférol trouvée varie considérablement suivant les variétés cultivées, les conditions de croissance et la saison de récolte[3],[4],[5]. Les mesures données sont des moyennes faites sur la forme aglycone après hydrolyse des hétérosides.
- Câpre, en conserve, 1355 mg/kg
- Mure (Morus alba), 284 mg/kg
- Aloe vera, feuilles, 258 mg/kg
- Fraise (Fragaria ananassa), 193 mg/kg
- Ciboulette (Allium schoenoprasum), 120 mg/kg
- Brocoli (Brassica oleracea var italique), 100 mg/kg
- Livèche, céleri perpétuel, (Levisticum officinale), 70 mg/kg
- Epinard (Spinacia oleracea), 60 mg/kg
aucune trace de kaempférol n'a été détectée dans les carottes ou l'ail.
Il a été observé que l’irradiation par des UV de l’arabette induit une synthèse du kaempférol (Lois 1994[6]). Il est généralement considéré que l’accumulation des pigments colorés dans l’épiderme des plantes leur confère une protection contre les méfaits des rayonnements.
Propriétés médicinales
Comme tous les flavonols, le kaempférol a une bonne activité anti-oxydante. Celle-ci peut être mise en évidence par le rôle protecteur qu’il joue lors de l’hémolyse des globules rouges du sang induite par radicaux libres. Mais Dai et als.[7] ont observé que l’efficacité anti-hémolytique du quercétol et de ses hétérosides (flavonols portant des groupes fonctionnels ortho-dihydroxyl) était nettement supérieure à celle portant un seul hydroxyle phénolique en 4’ comme le kaempférol.
Notes et références
- ↑ (en) ChemIDplus, « Kaempferol - RN: 520-18-3 » sur chem.sis.nlm.nih.gov, U.S. National Library of Medicine. Consulté le 23/07/2008.
- ↑ IARC Working Group on the Evaluation of Carcinogenic Risks to Humans, « Evaluations Globales de la Cancérogénicité pour l'Homme, Groupe 3 : Inclassables quant à leur cancérogénicité pour l'Homme » sur http://monographs.iarc.fr, 16 janvier 2009, CIRC. Consulté le 22 août 2009
- ↑ (en) U.S. Department of Agriculture, « USDA Database for the Flavonoid Content of Selected Foods » sur http://www.nal.usda.gov, 2003, National Agricultural Library, p. 1-78. Consulté le 31/10/2008 [pdf]
- ↑ (en) Bushra Sultana et Farooq Anwar, « Flavonols (kaempferol, quercetin, myricetin) contents of selected fruits, vegetables and medicinal plants », dans Food Chemistry, vol. 108, 2008
- ↑ (en) Ulla Justesen et Pia Knuthsen, « Composition of flavonoids in fresh herbs and calculation of flavonoid intake by use of herbs in traditional Danish dishes », dans Food chemistry, vol. 73, 2001
- ↑ (en) R. Lois, « Accumulation of UV-absorbing flavonoids induced by UV-B radiation in Arabidopsis thaliana L.I. Mechanisms of UV-resistance in Arabidopsis », dans Planta, vol. 194, 1994, p. 498-503
- ↑ (en) « Protective effets of flavonols and their glycosides against free radical-induced oxidative hemolysis of red blood cells », dans Life Sciences, vol. 78, no 21, 2006
Voir aussi
Articles connexes
Liens externes
- MSDS Kaempférol
- (en) Flavonoid (myricetin, quercetin, kaempferol, luteolin, and apigenin) content of edible tropical plants.
- (en) Content of the flavonols quercetin, myricetin, and kaempferol in 25 edible berries
- (en) Flavonol and flavone intakes - Fruit and Vegetable Consumption
- (en) Antioxidant flavonols from fruits, vegetables and beverages: measurements and bioavailability
Bibliographie
- Jean Bruneton, Pharmacognosie - Phytochimie, Plantes médicinales, Editions Tec & Doc, Editions médicales internationnales, 1999, 1120 p. (ISBN 2-7430-0315-4)
- Portail de la biologie
- Portail de la chimie
Catégories : Produit chimique nocif | Antioxydant | Flavonol | Hormone végétale | Polyphénol
Wikimedia Foundation. 2010.
